第21届欧洲
要点一览

接受利生奇珠单抗治疗的克罗恩病患者中,透壁愈合的早期动力学:多中心前瞻性SKYNETICS研究结果
摘要编号:OP03
本研究旨在评估真实世界实践中,克罗恩病(CD)患者接受利生奇珠单抗(RZB)治疗对临床结局、生化指标以及透壁动力学的影响。
在这项多中心前瞻性研究中,纳入超声检查有炎症客观证据的成人(≥18岁)CD患者,根据PRO-2在常规实践中开始使用利生奇珠单抗治疗症状性CD。以利生奇珠单抗600mg IV起始,第0、4、8周各用药一次,从第12周起接受360mg,每8周一次。在第0、4、12周进行超声检查以评估透壁反应的动力学。随后对患者进行长期随访。
主要终点是透壁反应,定义为在第4周和第12周时IBUS-SAS评分降低25%。同时也在第4周和第12周使用BUSS评分或us-C评分评估了透壁缓解替代定义。次要终点包括基于PRO-2的临床反应和临床缓解(第4、8、12周)、生化反应(
共纳入101例患者,平均年龄42.9±15.0岁,女性占58%,当前吸烟者占45.9%。蒙特利尔分类如下:病变部位(L1=41%,L2=11%,L3=48%)、表型(B1=28.9%,B2=42.1%,B3=28.9%)和既往肛周CD(37%)。其中,44.9%的患者既往需要肠切除,28%的患者既往使用一种生物制剂,32%和40%的患者分别接受过2种和≥3种先进疗法。
第4周,临床应答率和临床缓解率分别为57.7%和33.9%,第8周分别为70.1%和33.3%,第12周分别为79.2%和38.0%。在第0、4、8、12周,粪便钙卫蛋白中位数水平分别为269、192、200和135µg/g。根据IBUS-SAS评分,第4周和第12周透壁反应率分别为27.3%和28.5%;根据BUSS评分,分别为9.1%和14.3%;根据us-C评分,分别为52.3%和54.3%。在第12周,8.5%的患者达到透壁缓解。无论使用哪种评分系统,回肠和结直肠节段的节段透壁反应均没有差异。
这项前瞻性多中心研究纳入既往至少使用过一种抗TNF药物、未经选择的CD患者,利生奇珠单抗实现了早期临床、生化和透壁疗效,支持在这种临床情况下使用该药物。
利生奇珠单抗治疗中重度克罗恩病患者至第148周的持久疗效:SEQUENCE研究第2部分的事后分析
摘要编号:DOP004
随着时间推移,许多CD患者会失去治疗应答,这凸显了具有持久疗效的治疗方案的重要性。在中重度CD患者中,利生奇珠单抗先前已显示出具有持久的临床和内镜疗效。在进行中的SEQUENCE研究中,研究者评估了既往抗TNF治疗失败的中重度CD患者接受利生奇珠单抗治疗至3年的持久疗效。
在SEQUENCE研究(NCT04524611)中,在第1部分(为期48周,与
在这项事后分析中,疗效持久性定义为:第8周或第48周达到临床缓解(基于CDAI或SF/APS),或第24周或第48周达到内镜应答、内镜缓解或黏膜愈合的患者中,在后续评估时间点仍能达到相应终点的患者比例。对治疗应答不足的患者可接受利生奇珠单抗挽救治疗。利生奇珠单抗挽救治疗和终点定义的详情见图注。
基线后的第8周、第24周以及之后每24周进行一次临床评估,基线后的第24周、48周和148周进行内镜评估。数据涵盖了所有在第2部分中至少接受过一剂利生奇珠单抗的意向性治疗患者,并分别通过观察值(AO)和改良的无应答者填补法(mNRI)进行统计分析。安全性先前已报告。
共有224例患者进入第2部分研究,根据AO数据,大多数在第8周达到临床缓解的患者在后续时间点均保持临床缓解(图1);在第8周达到临床缓解的患者中,分别有98.5%(CDAI)和88.1%(SF/APS)在第148周达到临床缓解。在第48周达到临床缓解的患者中,在后续时间点同样观察到临床缓解的持久性。
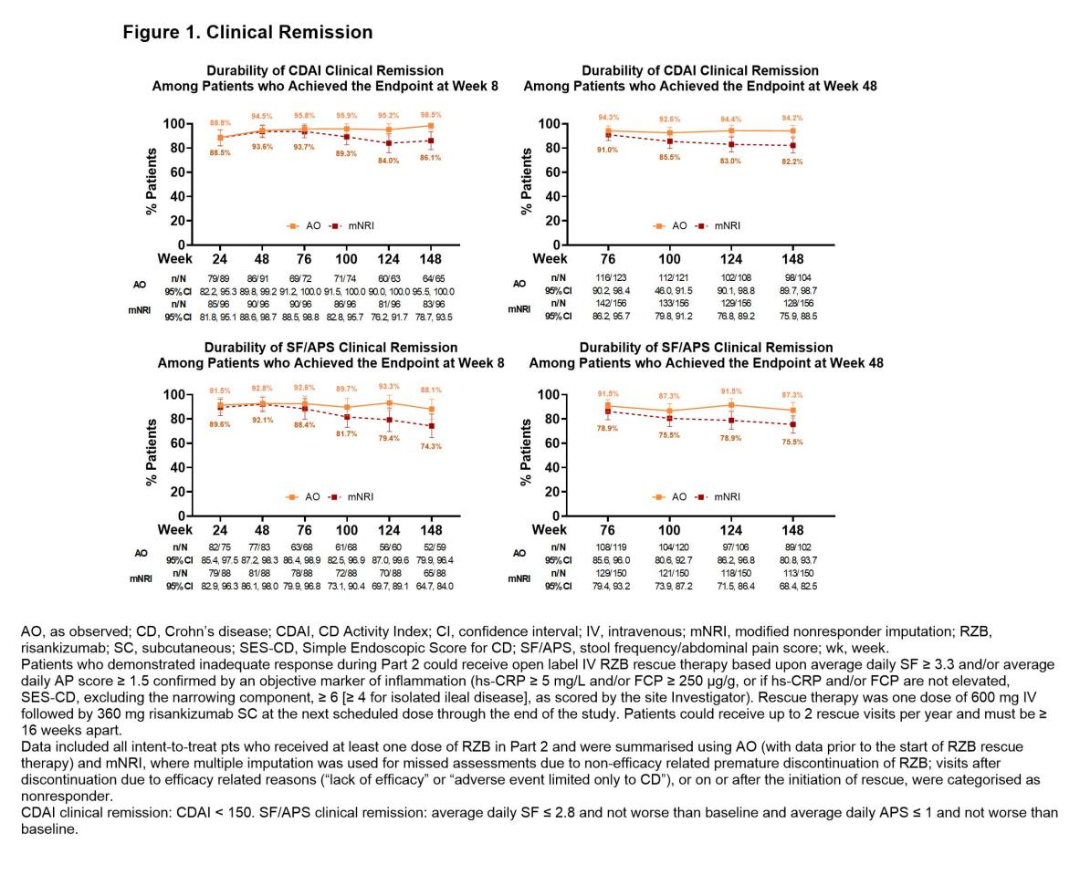
在第24周达到内镜应答、内镜缓解或黏膜愈合的患者中,分别有84.7%、78.2%和67.3%在第148周保持了相应的终点;第48周达到上述内镜终点的患者,在第148周也观察到相似的结果(图2)。使用mNRI分析的数据显示出了与AO数据相似的结果。
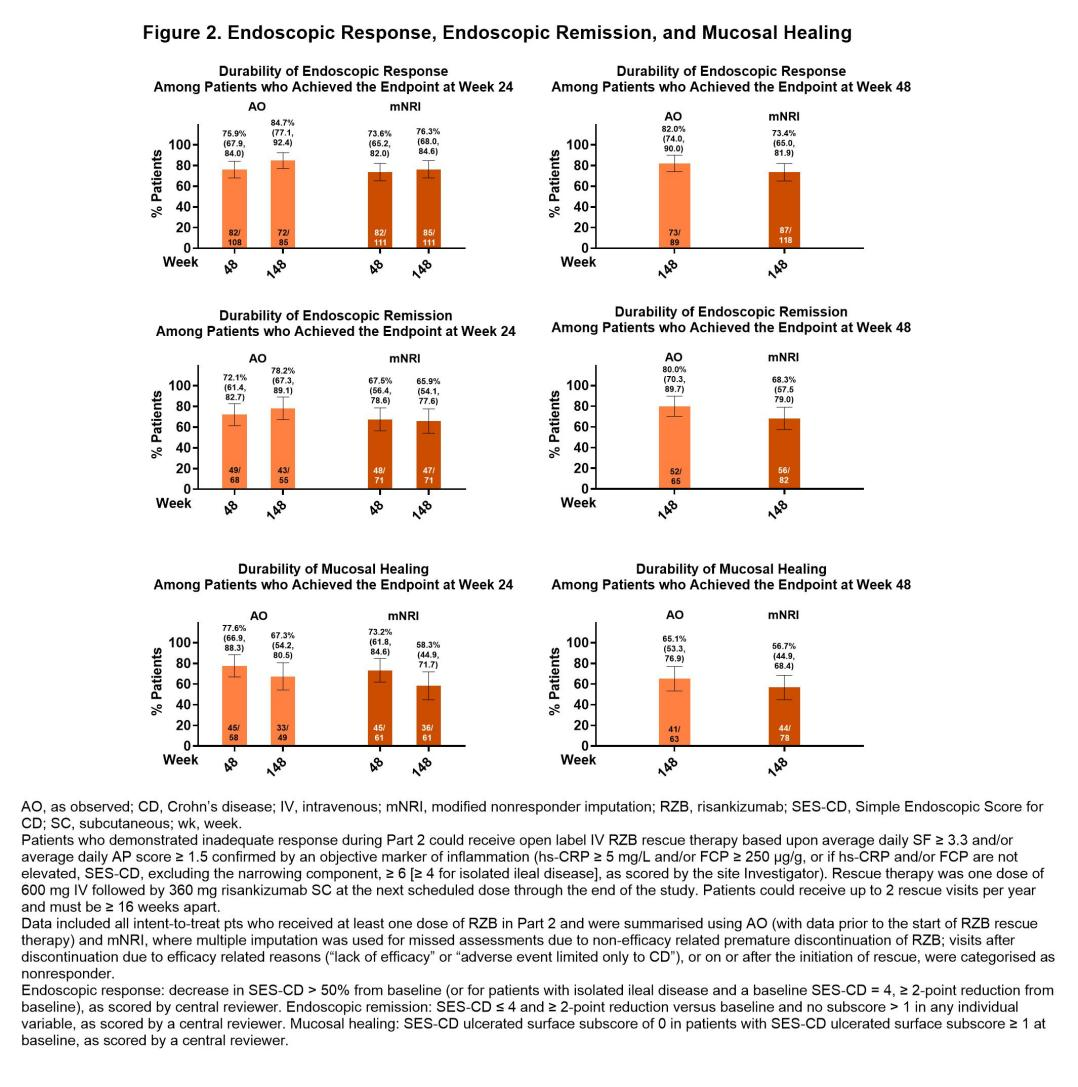
在SEQUENCE研究中,既往抗TNF治疗失败的中重度CD患者(通常被认为更难治),经过148周的利生奇珠单抗治疗,表现出持久的临床缓解、内镜应答、内镜缓解和黏膜愈合。
利生奇珠单抗治疗中重度克罗恩病的长期安全性和有效性分析:SEQUENCE研究的3年结果
摘要编号:DOP031
正在进行的SEQUENCE研究第2部分考察了IL-23 p19抑制剂利生奇珠单抗在中重度CD患者中的长期疗效和安全性。本次研究者报告了SEQUENCE研究的3年结果(第2部分的2年结果)。
在SEQUENCE研究的第2部分中,被随机分配至利生奇珠单抗组并完成第1部分第48周随访的患者,继续接受开放标签的利生奇珠单抗治疗,360mg皮下注射Q8w。评估至第148周时的临床缓解(基于CDAI和SF/APS)、无类固醇临床缓解、内镜反应、内镜缓解、无类固醇内镜缓解、深度缓解、黏膜愈合、炎症性肠病问卷(IBDQ)缓解,以及
对所有意向性治疗患者,分别采用观察值(AO)和改良无应答者填补法(mNRI)进行分析,其中mNRI对缺失评估值采用多重填补。接受挽救治疗之前数据呈现见图注。对第2部分中首次给予利生奇珠单抗剂量当日及之后报告的治疗期不良事件(TEAEs)进行分析(截止日期:2025年7月2日)。
总计有224例意向性治疗患者进入第2部分研究。与第52周相比,AO数据显示第148周的临床缓解率相似或更高(CDAI:76.4% vs 86.3%;SF/APS:72.1% vs 75.9%)、无类固醇临床缓解(CDAI:75.9% vs 83.5%;SF/APS:72.1% vs 73.0%)、IBDQ缓解(62.1% vs 69.0%)、内镜反应(55.8% vs 65.1%)、内镜缓解(39.2% vs 48.8%)、无类固醇内镜缓解(38.7% vs 48.3%)、黏膜愈合(37.3% vs 43.6%)和深度缓解(31.5% vs 36.8%)(图)。
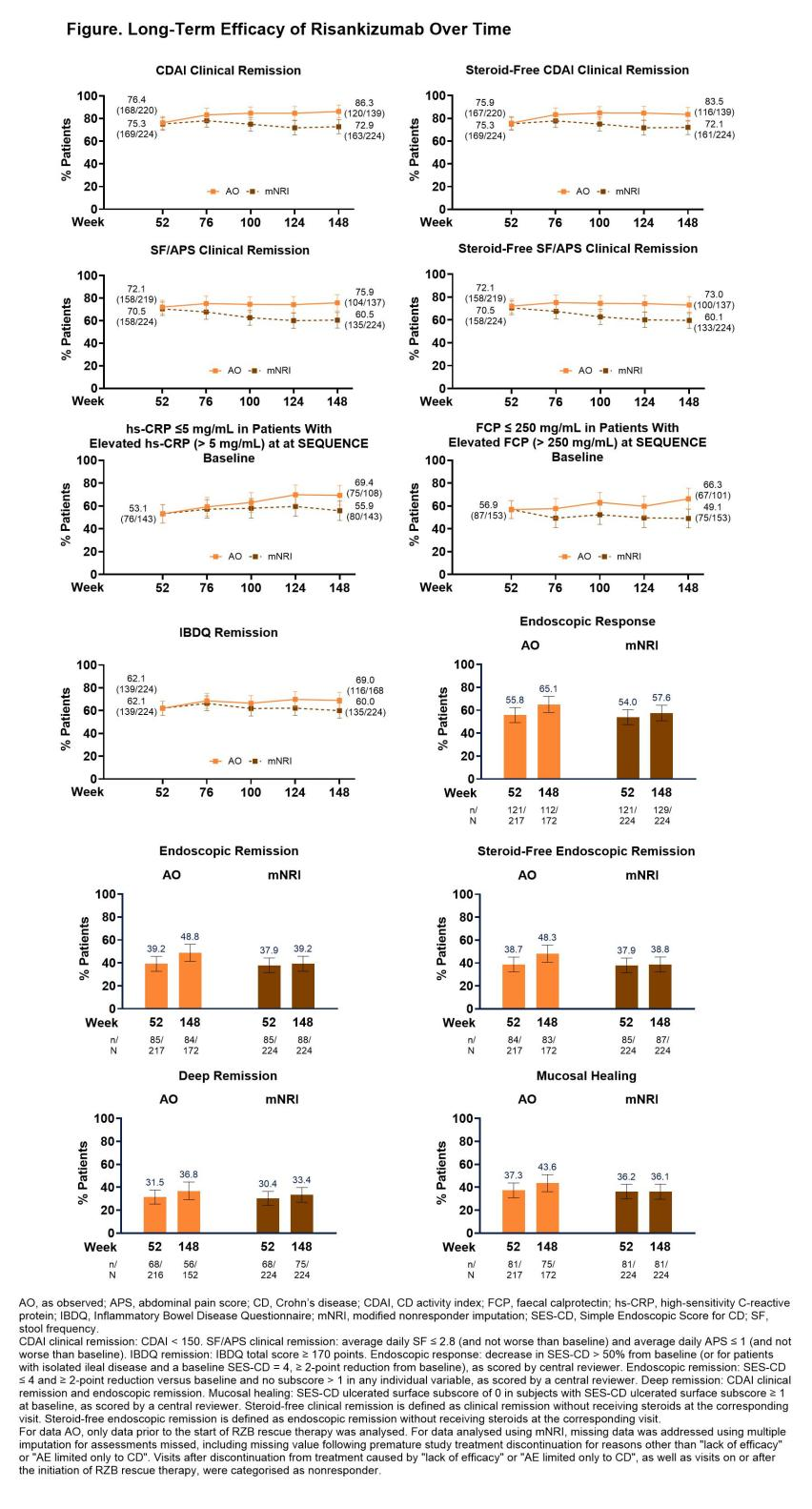
此外,与第52周相比,基线生物标志物水平升高的患者在第148周达到正常水平的比例更高(hs-CRP:53.1% vs 69.4%;FCP:56.9% vs 66.3%)。采用mNRI分析,有效率数值较低,但疗效也持续至第148周。治疗期不良事件及特别关注的治疗期不良事件特征与利生奇珠单抗已知的安全性特征一致(表)。第2部分研究期间未报告死亡病例。
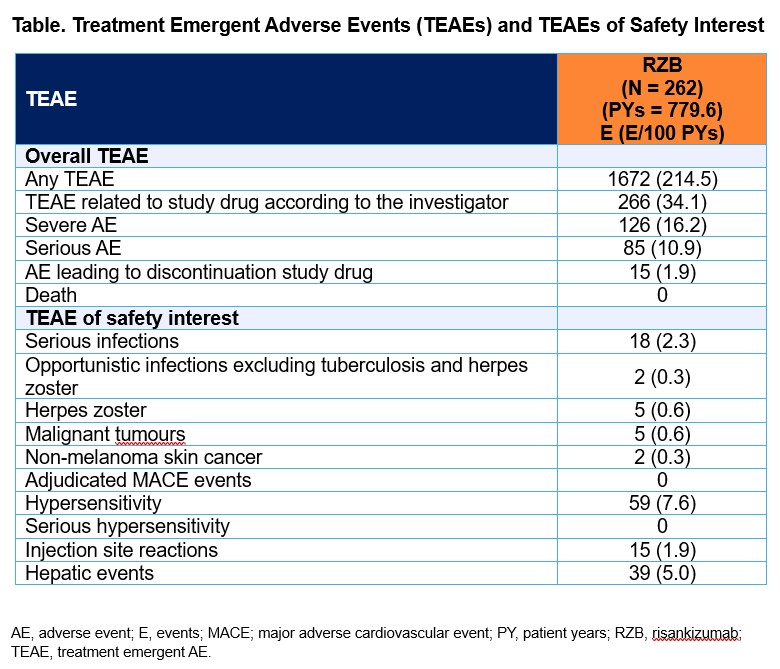
在SEQUENCE研究中,持续3年的利生奇珠单抗治疗带来了持久的长期临床、内镜和生活质量获益。安全性特征与利生奇珠单抗已知的安全性特征一致,支持其长期治疗。
利生奇珠单抗剂量优化的基线预测因素和临床结局:一项真实世界多中心回顾性研究
摘要编号:DOP085
部分接受利生奇珠单抗治疗的患者对标准剂量反应不佳或出现继发性失应答。研究者在一个由成人CD患者组成的多中心联盟中,探讨了与未来利生奇珠单抗剂量优化相关的因素,以及剂量优化的结局。
研究者在一个多中心队列中收集了开始利生奇珠单抗治疗时的基线特征以及随后的临床、内镜和生化结局。利生奇珠单抗剂量优化后的结局包括:临床应答和临床缓解(基于HBI评分,无HBI时使用PGA)、内镜缓解(基于SEMA-CD,无SEMA-CD时基于无溃疡判断),以及生化反应。使用卡方检验和双样本t检验比较标准剂量组和剂量优化组之间的特征。通过调整了年龄和性别的附加模型来评估剂量优化的预测因素。
研究者确定了309例接受标准剂量治疗的患者和58例建议进行剂量优化的患者。在这58例患者中,29例随访缺失(n=19)或保险拒绝剂量优化(n=10)被排除在结局分析之外。人口统计学信息见表1。
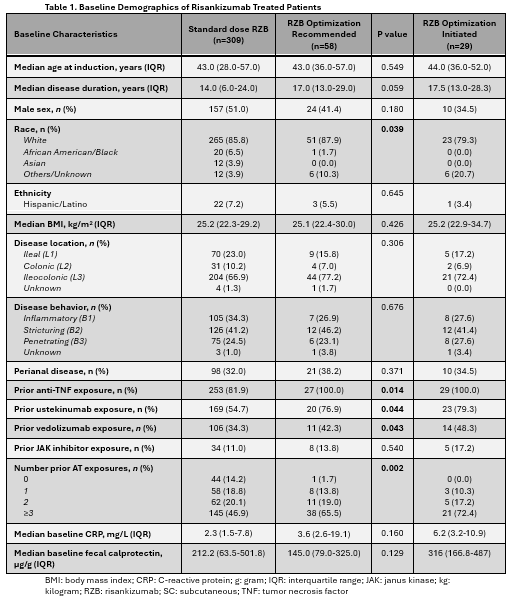
与未来剂量优化相关的基线特征包括:既往接受先进疗法的次数(OR 1.29,p<0.001)、既往抗TNF治疗(OR 4.06;p=0.022)和既往使用乌司奴单抗(OR 1.82;p=0.053)(表2)。
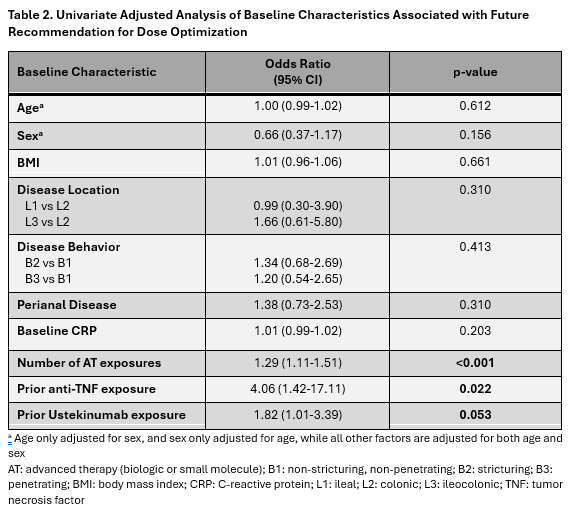
纳入结局分析的29例患者因原发性无应答(n=2)、部分应答(n=23)或继发性失应答(n=4)接受利生奇珠单抗剂量优化治疗,利生奇珠单抗起始后321天(中位数;IQR 234-440天)开始剂量优化。剂量优化后的中位随访时间为217天(IQR 147-331天)。所有患者均曾使用过先进疗法(表1)。27例患者(93.1%)在基线时有临床症状,中位HBI评分为6.5(IQR 6.0-8.0)。
12例基线时接受
在这项多中心回顾性队列中,既往使用过先进疗法(尤其是抗TNF)与需要对利生奇珠单抗进行剂量优化相关。对于利生奇珠单抗治疗后出现部分应答或失应答的患者,剂量优化可使相当大比例的患者成功重获临床应答。
中重度活动性溃疡性结肠炎患者使用利生奇珠单抗维持治疗长达3年的疗效与安全性:III期COMMAND开放标签扩展研究的中期结果
摘要编号:DOP055
利生奇珠单抗是一种靶向IL-23 p19的高亲和力人源化IgG1单克隆抗体,已证明对溃疡性结肠炎(UC)患者具有持续疗效和一致的安全性,支持其长期使用。本中期分析报告了COMMAND开放标签扩展(OLE)研究中,截至OLE第96周(总计维持治疗3年)的疗效和安全性数据。
本开放标签扩展研究纳入了利生奇珠单抗治疗、完成52周维持子研究和/或对12/24周诱导治疗有应答的患者。所有患者从OLE第0周开始接受利生奇珠单抗180mg皮下注射(RZB180),但既往接受过OLE利生奇珠单抗挽救治疗(利生奇珠单抗1200mg静脉注射1次,随后360mg每8周一次 [RZB360])并继续接受利生奇珠单抗360mg治疗96周的患者除外。
在OLE第0周和第96周评估疗效终点(包括基于AMS的临床缓解、基于PAMS的临床缓解、基于PAMS的无皮质类固醇临床缓解、基于AMS的临床应答、基于PAMS的临床应答、内镜改善和内镜缓解);安全性分析包括至少接受过1剂OLE利生奇珠单抗的患者,数据以事件/100患者年呈现。
在OLE第0周,约90%的患者(N=1003)完成了研究访视;观察到RZB180和RZB360治疗患者的临床特征存在一些差异,包括平均AMS(2.0 vs 3.4);RZB360组患者的AT-IR比例更高(63.1% vs 76.8%),且内镜评分≥3的比例更高(12.1% vs 31.1%)。
在OLE第0周,RZB360组患者达到临床缓解(基于AMS)的比例较低(54.8% vs 25.2%),RZB360组接受OLE挽救治疗患者的比例更高(RZB180:22.1%;RZB360:34.5%)。在OLE第0周和第96周,基于AMS的临床缓解率保持稳定;在AT-IR和非AT-IR各亚组观察到相似结果(表1)。在第96周,AT-IR患者与非AT-IR患者相比,有效率在数值上较低;OLE第96周,所有终点的疗效均得以维持(表1,AO及NRI结果)。
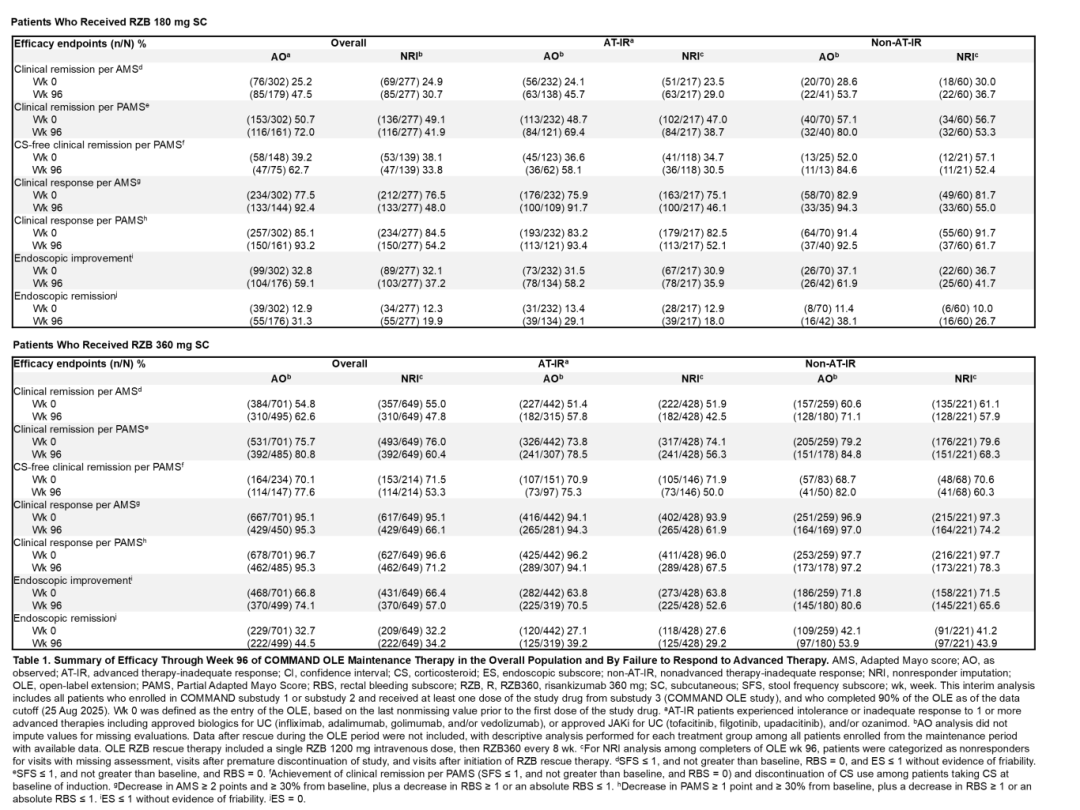
RZB180和RZB360治疗患者任意不良事件、重度不良事件和严重不良事件的发生率相似。两个治疗组中均未发现新的安全风险(表2)。
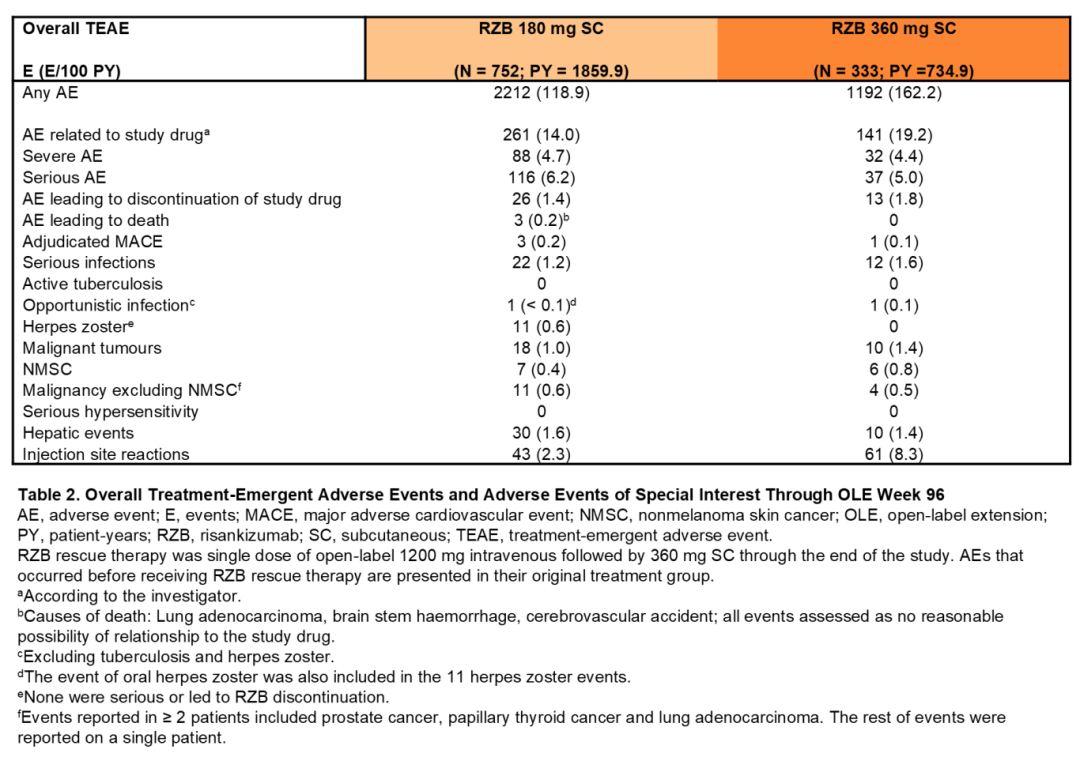
在正在进行的COMMAND开放标签扩展研究中,观察到接受长达3年长期利生奇珠单抗维持治疗的患者获得了持续的临床和内镜获益,AT-IR患者与非AT-IR患者相比,疗效率在数值上较低。RZB的长期安全性与其已知的有利获益-风险特征保持一致。