
本期配图来自2025年11月23日发表在Journal of Colloid and Interface Science( IF 9.7 )上的文章《A biodegradable nanomedicine for potentiated cancer therapy via Ca2+-overload and photothermal dual-amplifying cuproptosis》[1]
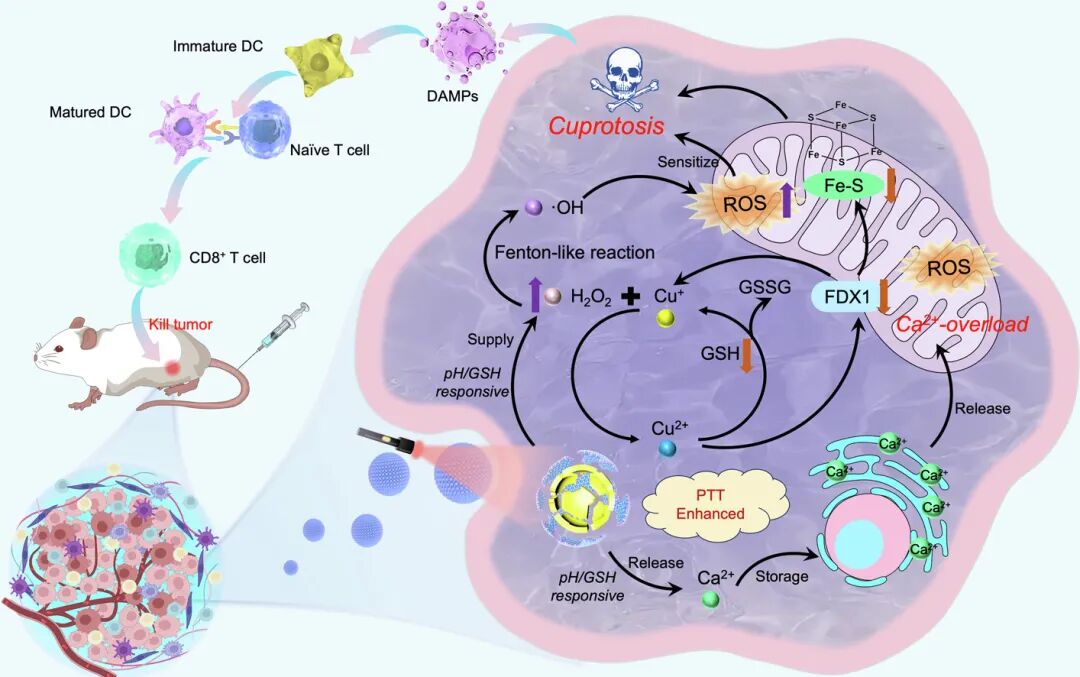
图1. CaO2@CuPDA通过Ca2+过载和光热双重增强铜死亡治疗
本图呈现了一种可生物降解的纳米药物,通过pH/
纳米药物被肿瘤细胞摄取后,响应肿瘤微环境的pH/GSH responsive(pH/谷胱甘肽)信号,释放负载的Cu2+与Ca2+;同时,外部光源激活纳米药物的PTT(光热治疗)功能,实现PTT Enhanced(光热增强)。
释放的Cu2+被细胞内的GSH还原为Cu+,GSH被氧化成GSSG,GSH水平降低;Cu+与细胞内的H2O2发生Fenton-like reaction(类芬顿反应),生成・OH等ROS(活性氧)。
同时,过量的Cu2+被FDX1(铁氧还蛋白1)还原成Cu+,抑制Fe-S(铁硫簇)蛋白合成,从而触发铜死亡。生成的ROS可Sensitize(致敏)肿瘤细胞,进一步放大铜死亡的杀伤效应。
纳米药物释放的Ca2+ 在细胞内积累(storage),引发Ca2+-overload(钙超载),加剧铜死亡过程,导致大量损伤相关分子模式(DAMPs)的释放。
这些DAMPs促进Immature DC(未成熟树突状细胞)分化为Matured DC(成熟树突状细胞);成熟DC将肿瘤抗原呈递给Naïve T cell(初始T细胞),使其分化为CD8+T细胞;最终,CD8+T细胞发挥Kill tumor(杀伤肿瘤)的作用,激活系统性抗肿瘤免疫,进一步增强治疗效果。
背景补充
近年来,离子干扰疗法作为一种创新的抗癌策略受到关注,该策略利用生物活性纳米材料破坏细胞内离子稳态,改变理化与代谢过程以诱导细胞死亡。本研究提出了一种设计策略:利用铜-聚
参考文献:
Wang L, Deng Y, Zhou X, Song K, Jiang C, Zhao F, Li X. A biodegradable nanomedicine for potentiated cancer therapy via Ca²⁺-overload and photothermal dual-amplifying cuproptosis. Journal of Colloid and Interface Science. 2026;705:139548. DOI: 10.1016/j.jcis.2025.139548

往期推荐
图解乳“献” | 第125期:小RNA片段5′tRF-GlyGCC通过乳酸脱氢酶A介导的糖酵解与巨噬细胞极化促进乳腺癌进展
编辑:Sophia
审校:Luna
排版:Sophia
执行:Ocean
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)