AE 多表现为边缘性脑炎,但可累及全脑各区域。传统上,AE 仅被视为 “亚急性起病、伴
过去十年,研究重点集中于 AE 的早期症状识别与诊断标准化,2016 年发布的诊断指南是该领域的重要进展。多种诊断预测工具(如副肿瘤性神经系统综合征(PNS)护理评分的应用、实验室检测技术的优化与解读水平提升,均为 AE 的早期精准诊断提供了支持。近期,《Nat Rev Dis Primers》发表的一篇综述,系统阐述了AE 的诊疗全貌,涵盖流行病学、病理生理机制、当前诊断流程、治疗、预后及生活质量,重点关注成年患者。

流行病学
AE 是一个涵盖多种疾病的总称,包括 “有明确生物标志物定义且病例标准已发表的亚型”(如抗 NMDAR 脑炎)和 “排除性诊断亚型”(可能血清阴性 AE)。其患者群体包括自身免疫病因者与副肿瘤病因者(图 1)。
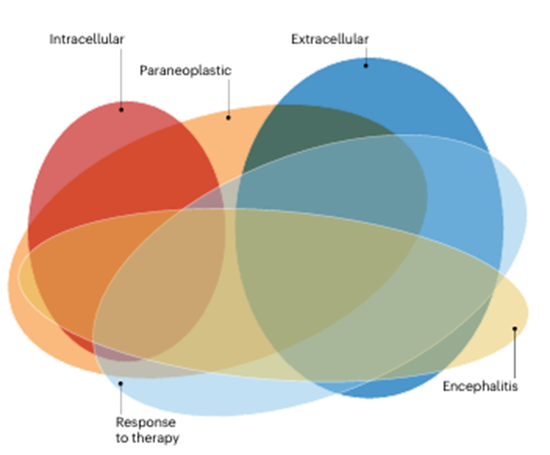
图 1 | 引发或关联自身免疫性脑炎(AE)的抗体类型重叠情况
AE 为罕见疾病:成人年累积发病率约为 0.5-1/10 万,儿童为 1.0-1.3/10 万。肿瘤治疗中免疫检查点抑制剂的应用,导致 1%-3% 的治疗患者出现多种免疫相关不良事件,其中近 50% 表现为 AE(可检出或未检出自身抗体)。随着这类药物获批用于更多肿瘤类型,免疫相关不良事件(包括 AE)的发病率可能进一步上升,或将占 AE 总病例数的较大比例。
不同 AE 亚型的患者性别与年龄分布差异显著(图 2):成人起病的畸胎瘤相关抗 NMDAR 脑炎女性占比显著较高;抗接触蛋白相关蛋白 2(CASPR2)脑炎和抗 LGI1 脑炎男性占比更高(约 60%);其他亚型的性别分布相对均衡(图 2)。
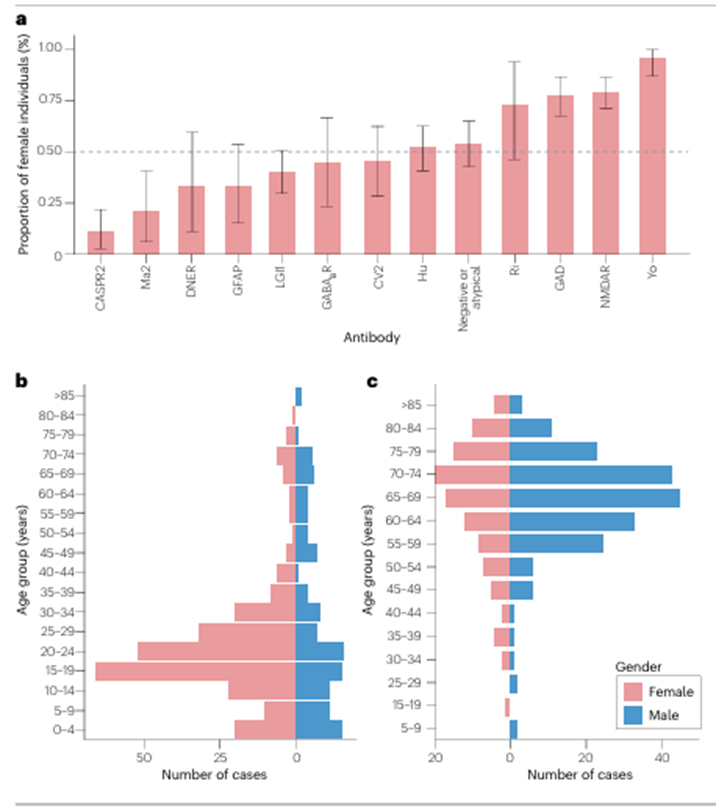 图 2 | 自身免疫性脑炎亚型的人群特征
图 2 | 自身免疫性脑炎亚型的人群特征
特定 AE 亚型的主要危险因素包括:
副肿瘤性因素:潜在的神经外胚层来源、神经内分泌来源肿瘤或
遗传因素:携带特定杂合或纯合人类白细胞抗原(HLA)单倍型;
药物因素:既往使用免疫检查点抑制剂;
感染因素:近期
遗传危险因素
部分 AE 亚型存在明显遗传易感性:85%-90% 的抗 LGI1 脑炎患者携带 HLA-DRB1*07:01 等位基因,纯合子携带可使发病风险翻倍。
机制/病理生理学
总体而言,自身免疫性脑炎(AE)由靶向中枢神经系统(CNS)的 “异常适应性抗原特异性免疫反应” 引发。这一核心机制可拆解为四个逐步递进、部分重叠且相互作用的病理过程(图 3):首先,一种或多种共存的触发因素导致免疫耐受被打破;其次,针对自身抗原的特异性免疫反应启动,抗原特异性淋巴细胞被募集至靶组织;随后,中枢神经系统内发生靶向特定自身抗原的免疫反应,影响突触功能并导致神经网络紊乱;最后,靶抗原的类型及其功能、解剖和亚细胞定位,决定了疾病的具体表现。
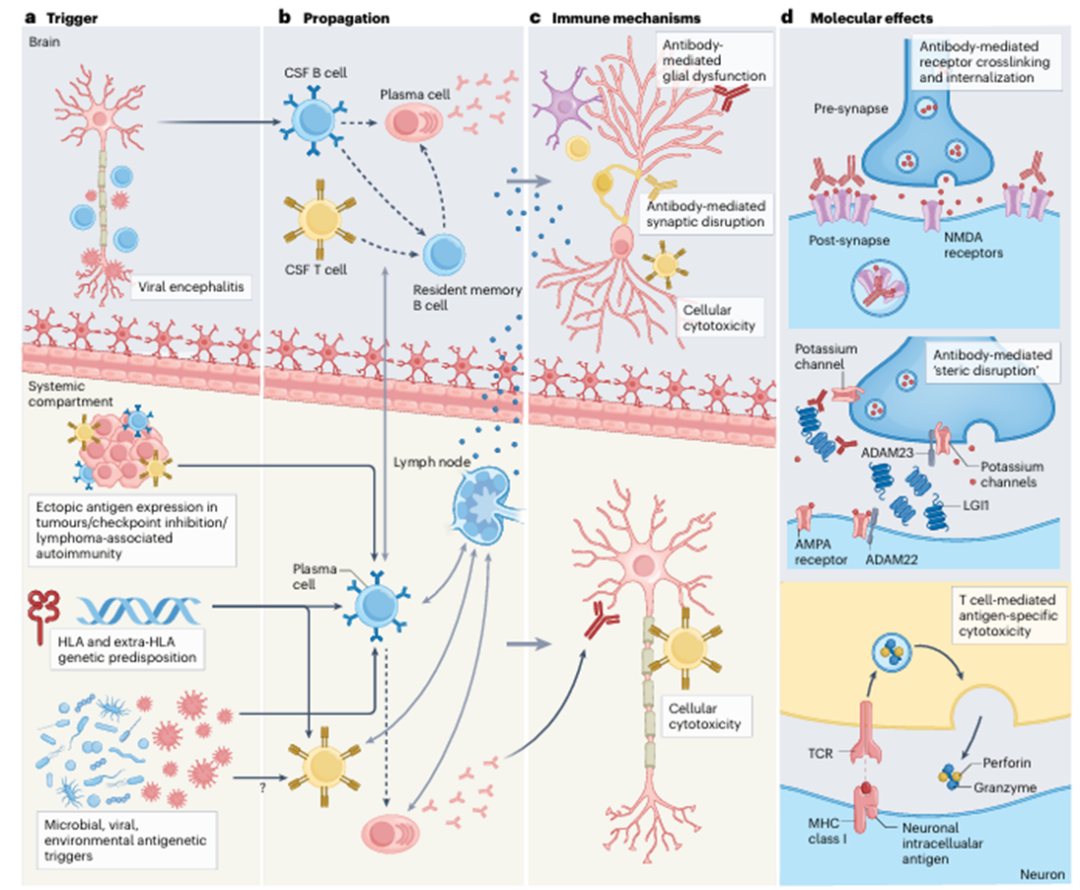 图 3 | 自身免疫性脑炎(AE)的发病机制
图 3 | 自身免疫性脑炎(AE)的发病机制
自身抗原的种类及其组织与亚细胞定位,是决定 AE 致病机制的核心因素。它们直接或间接影响临床表型、疾病进程、免疫触发因素、慢性化倾向、可逆性、预后、复发风险及对免疫治疗的差异化反应。这些发现强烈支持按 “靶抗原类型” 对 AE 进行亚型分类(如抗 NMDAR 脑炎)。深入理解每种 AE 亚型的致病机制,不仅是解析病理生理过程的关键,也为开发 “过程特异性标志物” 与 “靶向病理过程的疗法” 奠定基础。
诊断、筛查与预防
AE 的临床诊断以核心症状识别为基础,包括记忆障碍、精神病性症状(如妄想)、紧张症、行为异常、癫痫发作、意识模糊及意识水平改变。这些症状可急性、亚急性或慢性起病,持续时间因关联的自身抗体类型而异。
AE 的鉴别诊断范围广泛,需结合临床症状与辅助检查结果综合判断。早期鉴别 AE 与感染性脑炎存在挑战 —— 二者临床表现与脑脊液改变可能相似,但脑 MRI 可提供关键线索。所有患者均需完善血液与脑脊液病原学检查,排除潜在感染病因;部分病例还需与快速进展性神经退行性疾病、代谢性疾病及遗传性模拟疾病鉴别。
需注意两类特殊情况:
慢性起病亚型:部分AE 综合征(如抗 IgLON5、抗 CASPR2 相关疾病、抗 GAD 相关综合征)并非亚急性起病,病程可达数月至数年,不符合上述诊断流程标准。
非脑病表现亚型:抗LGI1 脑炎患者可能以突出癫痫发作为主要表现,无暴发性脑炎特征,因此需单独制定 “可能抗 LGI1 脑炎” 标准;此外,诊断流程不适用于无脑病表现(如无工作记忆障碍、意识状态改变或精神病性症状)的患者,例如仅表现为小脑症状、脑干脑炎或脊髓病的病例。
神经影像学(脑 MRI)
脑 MRI 可显示边缘性脑炎的特异性表现
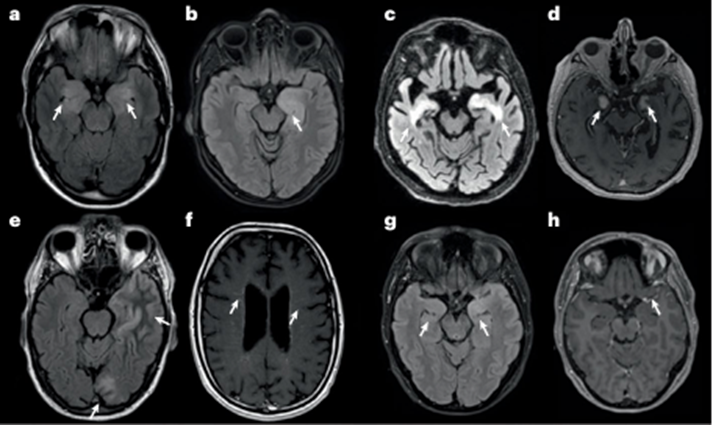 图 4 自身免疫性脑炎患者的典型 MRI 表现
图 4 自身免疫性脑炎患者的典型 MRI 表现
a 最典型的 MRI 模式为双侧内侧颞叶在 T2 / FLAIR序列上呈高信号(箭头),即边缘性脑炎。
b 较少见的表现为单侧内侧颞叶在 T2/FLAIR 序列上呈高信号(箭头)。
c 该 T2/FLAIR 图像初看可见典型高信号(箭头),但病变范围略超出内侧颞叶区域。
d 该 T1 序列上的强化表现(箭头)为 “警示信号”;该患者最终确诊为Whipple。
e 抗 GABAA 受体脑炎中,FLAIR 序列可见多灶性、边界不清的大片白质病变(箭头)。
f 抗 GFAP 星形细胞病的典型 MRI 特征为增强上呈线性 / 放射状血管周围强化(箭头)。
g 最后一例患者的 T2/FLAIR 图像符合自身免疫性脑炎典型表现,显示双侧高信号(左侧较右侧明显;箭头)。
h 钆强化表现(箭头)不典型(警示信号);该患者最终确诊为多形性胶质母细胞瘤。
纵向 MRI 随访具有重要临床价值:可确认治疗反应、观察既往 T2/FLAIR 病变的消退情况、监测提示不良临床结局的脑萎缩进展,以及发现复发或新发脑病变。
脑脊液分析
脑脊液常表现为细胞增多或总蛋白升高;鞘内抗体合成(以脑脊液 IgG 指数升高或寡克隆带为特征)常提示中枢神经系统内存在活动性免疫病理过程。不同自身抗体相关 AE 的脑脊液异常发生率存在差异:抗 NMDAR 脑炎中常见,而抗 LGI1、抗 CASPR2 或抗IgLON5 脑炎中罕见。需注意:部分 AE 患者的常规脑脊液检查可完全正常。
脑电图
常表现为背景活动减慢或癫痫样放电。“极度 δ 刷” 是抗 NMDAR 脑炎的特征性脑电图模式,但仅见于少数重症患者。
FDG-PET
并非多数疑似 AE 患者的常规检查项目:虽敏感性较高,但鉴别 AE 与其他神经系统疾病的特异性有限。在快速进展性痴呆患者中,FDG-PET 可用于区分自身免疫性与神经退行性病因;抗 NMDAR 脑炎中,FDG-PET 可表现为额叶高代谢与相对枕叶低代谢。
抗体检测
自身抗体检测是确诊 AE 的关键,有时甚至是提示神经炎症的唯一旁证(尤其抗 LGI1、抗 CASPR2、抗IgLON5 抗体阳性患者)。同时检测血清与脑脊液对提高诊断准确性至关重要。
基因检测
目前 HLA 分析并非 AE 的常规诊断项目,但研究显示部分 AE 亚型与特定 HLA 亚型相关,未来可能纳入诊疗流程。例如:
约 90% 抗 LGI1 脑炎患者携带 HLA-DRB1*07:01;
48%-94% 抗 CASPR2 脑炎患者携带 HLA-DRB1*11:01;
约 85% 抗 IgLON5 脑炎患者携带 HLA-DQB1*05:01;
60%-70% 抗 Kelch 样蛋白 11(KLHL11)脑炎患者携带 HLA-DQB102:01/HLA-DRB103:01。
肿瘤筛查
对于疑似副肿瘤性 AE 的患者,常规肿瘤筛查包括:胸部 CT、腹盆腔增强 CT;女性需加做乳腺X 线/超声 / MRI,男性需加做睾丸超声。若初步筛查阴性,通常需进一步行 PET-CT;但需注意:FDG-PET 检测成熟畸胎瘤的敏感性较低。
对于 PNS 护理评分高(提示高癌症风险)但初始未确诊癌症的患者,建议在至少 2-5 年内,每 3-6 个月重复一次肿瘤筛查。该评分综合了患者表型、抗体类型及肿瘤存在情况(表 4)。
表 4 副肿瘤性神经系统综合征(PNS)护理评分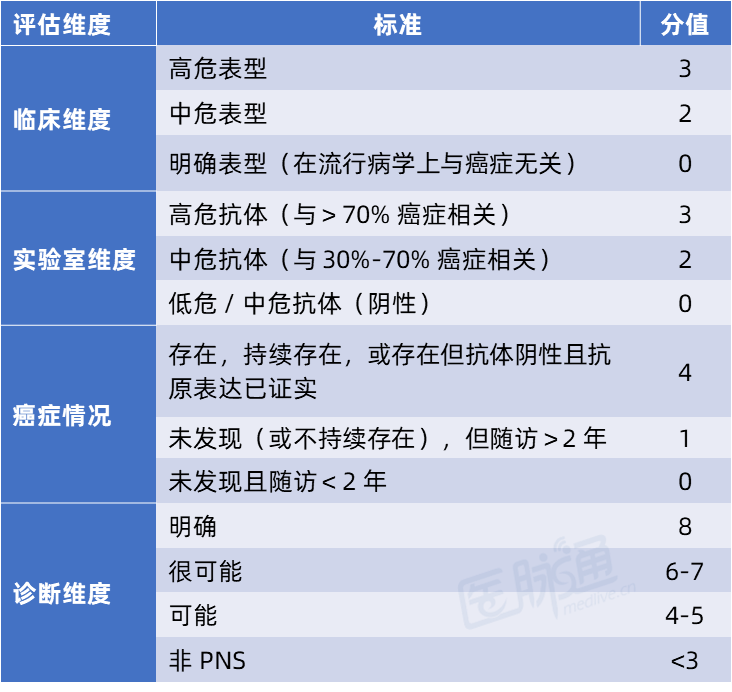
治疗管理
自身免疫性脑炎(AE)的综合管理需兼顾 “合理使用现有药物疗法” 与 “多学科团队协作的全程整体护理”,尤其需覆盖该病常有的长期病程。多学科协作是优化 AE 患者康复效果的关键 —— 除神经科诊疗外,精神科、重症医学科、儿科、肿瘤科及康复科等多个专科均在 AE 的诊断与治疗中发挥核心作用。
首先,确诊 AE 的患者需尽快启动经验性免疫治疗。只要临床高度怀疑 AE,即使尚未获得抗体检测结果,也应尽早开始治疗 —— 这一点在两种最常见 AE 亚型(抗 LGI1 脑炎、抗NMDAR 脑炎)中已得到证实,早期免疫治疗可显著改善神经功能结局。当然,启动治疗需平衡 “误诊或过度诊断的明确风险”,这些风险包括延误感染、淋巴瘤或全身性炎症疾病的诊断。
在免疫治疗的同时,若患者合并肿瘤,需及时有效处理肿瘤 —— 该干预措施可帮助部分患者改善或稳定病情。此外,还需针对性使用对症治疗药物,包括抗癫痫药(控制癫痫发作)、镇静药物(缓解行为症状)及运动障碍治疗药物。但需注意:对症治疗的效果远逊于免疫治疗,且常需大剂量使用才能显现临床效果;部分抗癫痫药还可能引发严重过敏反应或行为相关不良反应。因此,综合疗效与安全性下,对症治疗在 AE 管理中的优先级较低。
AE 病程早期的免疫治疗可分为一线与二线两类方案:
一线免疫治疗
1. 糖皮质激素
一旦高度怀疑 AE,通常首先启动糖皮质激素治疗。
2. 血浆置换
血浆置换的作用机制被认为是清除循环中的自身抗体、免疫复合物及细胞因子,疗效可在数天内显现,但难以单独归因于该疗法(常与其他免疫治疗联用)。
3. 静脉注射免疫球蛋白(IVIG)
IVIG 的免疫调节作用机制包括:中和自身抗体及细胞因子、饱和新生儿 Fc 受体(减少抗体循环利用)、抑制补体级联反应。
二线与三线免疫治疗
一线治疗后,需根据患者的临床改善程度决定后续方案(目前尚无生物标志物辅助该评估过程)。具体决策需结合 “改善幅度”“疾病已知病程特点” 及 “复发预防需求”,判断是否启动二线治疗。二线治疗主要用于一线治疗无效(难治性)或改善不佳的患者,以抗 NMDAR 脑炎最为常见。
1. 常用二线药物
利妥昔单抗:CD20靶向药物,通过耗竭 B 细胞发挥作用。
环磷酰胺:细胞毒性药物,广谱抑制淋巴细胞活性。
其他可选药物(使用频率较低):托珠单抗、硼替佐米、吗替麦考酚酯、硫唑嘌呤、维持性 IVIG。
临床实践中,绝大多数患者仅需使用利妥昔单抗或环磷酰胺。此外,多种新型药物正处于小样本研究阶段,包括补体抑制剂、抗 CD38 单克隆抗体、BAFF/APRIL 抑制剂、钙调神经磷酸酶抑制剂、整合素抑制剂及 JAK 抑制剂(图 5)。
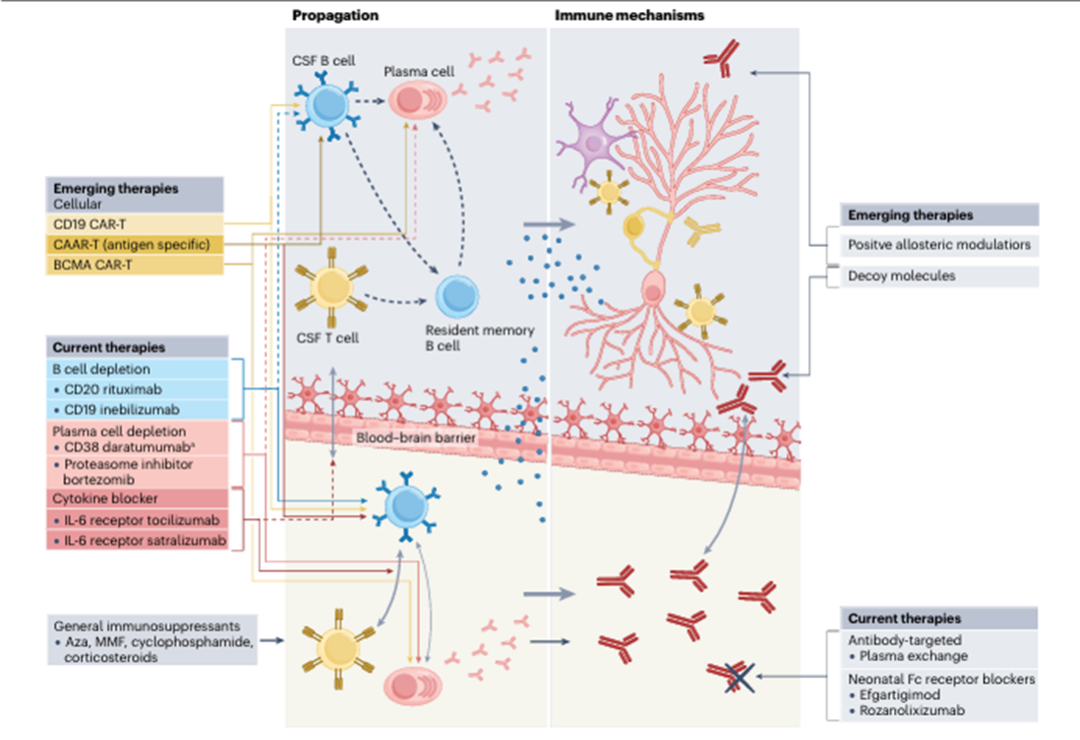
图 5 自身免疫性脑炎的二线免疫治疗
图中展示了自身免疫性脑炎相关的病理生理靶点及通路。
2. B 细胞靶向治疗
B 细胞可分化为抗体分泌细胞、呈递抗原以激活 T 细胞,并分泌多种信号分子。通过靶向 B 细胞特异性表面标志物(如 CD20、CD19)的单克隆抗体耗竭B 细胞,可同时干预上述多种功能,适用于多种疾病。此外,细胞性 B 细胞耗竭疗法(如嵌合抗原受体 T 细胞疗法)是新兴领域,目前在 AE 及相关神经系统疾病中的数据有限。
3. DNA 合成抑制剂
通过非选择性抑制 DNA 合成,可诱导快速分裂细胞死亡,多数经典化疗药物属于此类。大剂量使用时毒性较高,但低剂量时不良反应可控。
4. 细胞因子拮抗剂
AE 中最相关的靶向细胞因子是 IL-6——IL-6 是一种多效性促炎细胞因子,可促进 B 细胞存活、刺激抗体产生、支持辅助性 T 细胞增殖,并减轻血脑屏障功能障碍。
5. 新生儿 Fc 受体(FcRn)抑制剂
FcRn 广泛表达于内皮细胞等多种细胞表面,通过内吞抗体并阻止其在循环中降解,延长免疫球蛋白半衰期。阻断 FcRn 可使循环 IgG 水平显著降低至基线的 30%,与 CD20/CD19 靶向药物不同,此类药物可直接降低 IgG 水平,但对致病性自身抗体无选择性。
6. 蛋白酶体抑制剂
通过抑制蛋白酶体亚基功能,阻止蛋白质降解,导致毒性蛋白蓄积并诱导细胞死亡。浆细胞因高表达分泌性蛋白(抗体),对这类药物敏感性较高。
AE 患者的预后存在显著异质性,与自身抗体类型及病理生理机制密切相关:
复发与死亡风险:12%-35%的患者会出现临床复发;死亡率因病因与病情严重程度而异,介于 5%-40%。
长期残疾:常用mRS 评分评估残疾程度,其影响因素包括自身抗体类型、免疫抑制治疗效果、病情严重程度(如是否需重症监护)及随访时长。
亚型差异:合并高危副肿瘤抗体的 AE 患者,其残疾程度与死亡率通常高于靶向细胞外表位抗体的 AE 患者。
展望
AE 是一类已明确且可治疗的神经炎症性疾病。随着症状识别能力提升与实验室检测技术优化,AE 发病率(诊断率)持续升高;罕见病领域至关重要的国际协作,也为这些进步提供了支撑。
本文摘译自文献Autoimmune encephalitis. Nat Rev Dis Primers. 2025 Sep 11;11(1):66. PMID: 40935815.不足之处,请批评指证。
