2026年2月18日至21日,第21届欧洲
会议期间,IBD领域多项生物制剂相关研究进展相继揭晓、亮点纷呈。本文特汇总整理其中关于
要点一览

静脉注射维得利珠单抗在中重度溃疡性结肠炎儿童患者中的疗效和安全性:KEPLER 3期试验结果
摘要编号:DOP037
儿童及青少年溃疡性结肠炎(UC)的获批治疗方案有限。KEPLER 3期试验旨在评估抗α4β7整合素生物制剂维得利珠单抗静脉输注诱导及维持治疗中重度活动性UC儿童及青少年患者的疗效、免疫原性、药代动力学及安全性。
该研究为3期单臂临床试验,纳入2~17岁、体重≥10kg、既往常规治疗(如类固醇、免疫调节剂和/或肿瘤坏死因子[TNF]拮抗剂)失败的中重度UC患者(改良Mayo评分5-9分且内镜评分≥2分)。
在为期14周的开放标签诱导期内给予维得利珠单抗静脉注射,随后进入为期40周的随机、双盲维持期,根据患者体重以1:1的比例随机分为低剂量组和高剂量组(10-15kg [100 vs 150mg];>15-<30kg [100 vs 200mg];≥30kg [150 vs 300mg]),每8周给药一次。
研究主要终点为意向性治疗维持人群在第54周时经改良Mayo评分评估达到临床缓解。次要终点包括第14周临床缓解、持续临床缓解(第14周和第54周)、第54周无激素临床缓解、免疫原性、药代动力学和安全性指标。
研究共纳入121例患者(10-15kg,n=3;>15-<30kg,n=27;≥30kg,n=91),120例患者接受了给药,93例患者后续被随机分入低剂量组(47例)和高剂量组(46例)接受维持治疗(表1)。
表1 基线特征
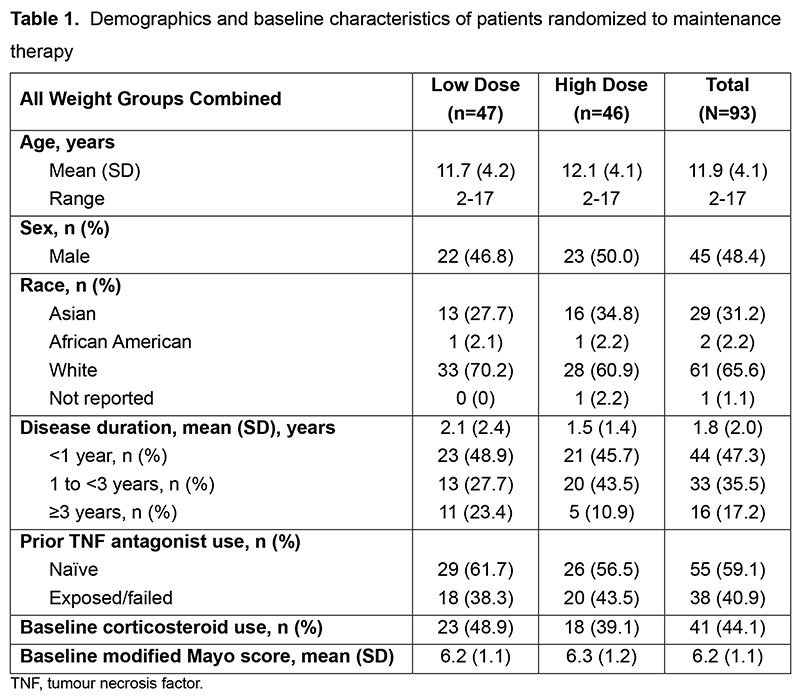
93例维持治疗患者中,44例(47.3%)在第54周达到主要终点(临床缓解),低剂量组与高剂量组缓解率相近(图1A)。按体重、年龄、TNF拮抗剂暴露史和基线激素使用情况分层的患者在第54周临床缓解率见图1B~E。121例患者中,42例(34.7%)在第14周达到临床缓解;93例维持治疗患者中,27例(29.0%)在第54周达到持续临床缓解。
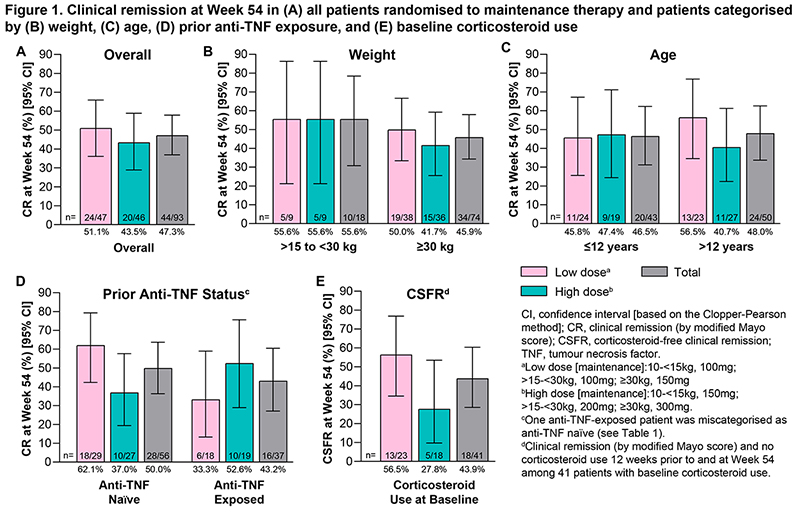
图1 第54周临床缓解情况
120例接受维得利珠单抗治疗的患者中,7例(5.8%)产生抗维得利珠单抗抗体,其中4例(3.3%)为中和抗体;不同体重组患者的维得利珠单抗血清谷浓度相近。安全性人群中,120例患者中有103例(85.8%)发生治疗期间不良事件(TEAE),其中15例(12.5%)与维得利珠单抗相关;468例TEAE中,25例(5.3%)为严重TEAE,5例(4.2%)患者发生与维得利珠单抗相关的严重TEAE;7例(5.8%)患者因TEAE停用维得利珠单抗,其中最常见原因为溃疡性结肠炎加重(3例)和感染(3例)。
低剂量和高剂量维得利珠单抗静脉输注方案治疗UC儿童和青少年有效,包括既往TNF拮抗剂或激素治疗失败的患者。在成人UC患者中也观察到了类似的疗效。维得利珠单抗耐受性良好,未发现新的安全性信号。
乌司奴单抗治疗肛周瘘管型克罗恩病:USTAP随机安慰剂对照试验第48周结果
摘要编号:DOP007
肛周瘘管型克罗恩病(CD)仍然是一个重大挑战,相关随机对照试验较少。USTAP试验旨在通过多中心随机对照设计评估乌司奴单抗在活动性引流性肛周瘘管CD患者中的疗效和安全性。
这项双盲、安慰剂对照、多中心试验纳入了活动性引流性肛周瘘管CD成人患者。符合条件的患者在必要时进行挂线引流术后,以1:1的比例随机分配接受乌司奴单抗(基线时静脉注射6mg/kg,第8周皮下注射90mg,后续每8周给药一次)或安慰剂治疗。
研究主要终点为患者在第12周时达到联合缓解,即临床缓解和影像学缓解。在第12周,安慰剂组无应答者可转为乌司奴单抗治疗,乌司奴单抗组无应答者在开放标签期可接受强化治疗。次要终点包括临床缓解、影像学缓解和安全性。第12周的终点指标由盲态裁决委员会独立审查。研究按患者既往TNF拮抗剂暴露史和研究中心进行分层。计划样本量为每组73例患者,由于入组缓慢,该研究于2024年6月终止,未揭盲研究数据。
研究在法国10个研究中心共入组32例患者,其中乌司奴单抗组16例、安慰剂组16例,70%的患者既往有TNF拮抗剂暴露史。基线时,84%的患者有1个引流性瘘管,16%有2个,25%有脓肿。
第12周时,乌司奴单抗组62%的患者达到联合缓解,安慰剂组为25%(表1);乌司奴单抗和安慰剂组临床缓解率分别为69% vs 31%,影像学缓解率分别为87.5% vs 75%。
表1 第12周疗效指标
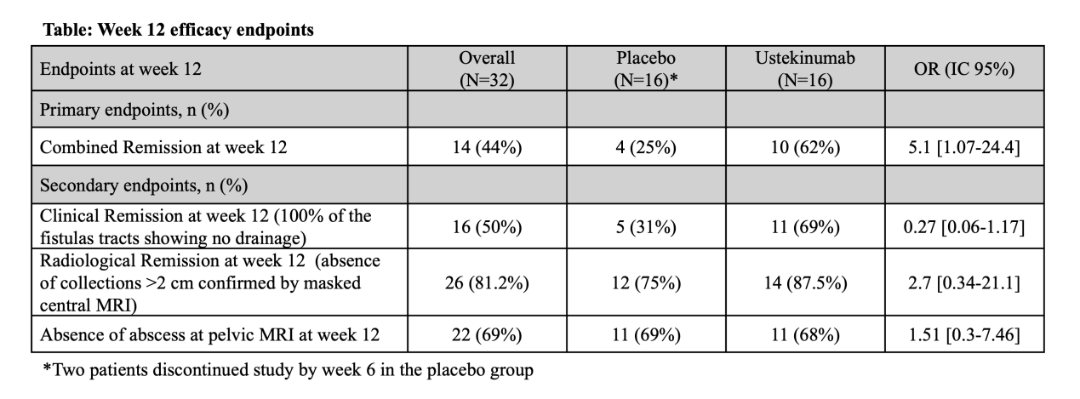
第48周时,乌司奴单抗组患者自随机入组后的治疗持续率为56%(9/16),安慰剂组为12.5%(2/16)。9例安慰剂组患者在开放标签阶段换用乌司奴单抗治疗。第48周时,安慰剂换用乌司奴单抗组的联合缓解率为7/16(50%),乌司奴单抗组为5/16(31%)。
两组间不良事件和严重不良事件发生率相近,共报告14例严重不良事件(安慰剂组11例、乌司奴单抗组3例),2例安慰剂组患者因肛周脓肿和回肠周围脓肿在第6周前终止研究。
该研究中多数患者既往有TNF拮抗剂暴露史,所观察到的乌司奴单抗短期临床获益支持其用于肛周瘘管型CD,约半数乌司奴单抗治疗患者能持续治疗。
UNITI Jr研究:乌司奴单抗在克罗恩病儿童患者中的安全性和有效性结果
摘要编号:DOP007
在IM-UNITI研究中,乌司奴单抗诱导及维持治疗在中重度CD成人患者中展现出良好的应答率和缓解率。UNITI Jr研究旨在评估乌司奴单抗治疗中重度活动性CD儿童患者的疗效与安全性。
101例患者(≥2岁-<18岁;pcdai评分>30;对常规/生物制剂治疗应答不佳/不耐受或皮质类固醇依赖)接受了1剂开放标签乌司奴单抗静脉注射诱导治疗。第8周时,97例患者根据基线体重(<40kg/≥40kg)和应答状态(应答:PCDAI评分下降≥12.5分且总分≤30分;无应答:PCDAI评分下降<12.5分)进行分层,以1:1的比例随机分为两组,分别接受盲法乌司奴单抗皮下注射维持治疗,每8周或每12周给药一次,维持治疗周期44周。乌司奴单抗剂量基于体表面积(<40kg)或体重分层(≥40kg)。
研究主要终点为第8周时的临床缓解(PCDAI评分≤10分),以及诱导治疗应答的随机化患者在第52周时达到临床缓解。
UNITI Jr研究共纳入101例患者,其中男性59.4%,中位年龄14.0岁(12.0~15.0岁),42.6%未接受过生物制剂治疗,中位PCDAI评分为40.0分(35.0~45.0分)。第8周时,47例患者(46.5%)达到临床缓解。在第8周达到临床缓解的患者中,32例(68.1%)在第52周维持临床缓解。
第8周时,85例患者(84.2%)达到临床应答,其中46例(54.1%,95% CI:43.6%~64.3%)在第52周达到临床缓解,45例(52.9%,95% CI:42.4%~63.2%)在第52周达到无激素临床缓解。既往无生物制剂治疗失败史与第52周缓解率更高相关(图1A)。所有体重亚组患者从第8周到第52周的缓解率均相近(图1B)。
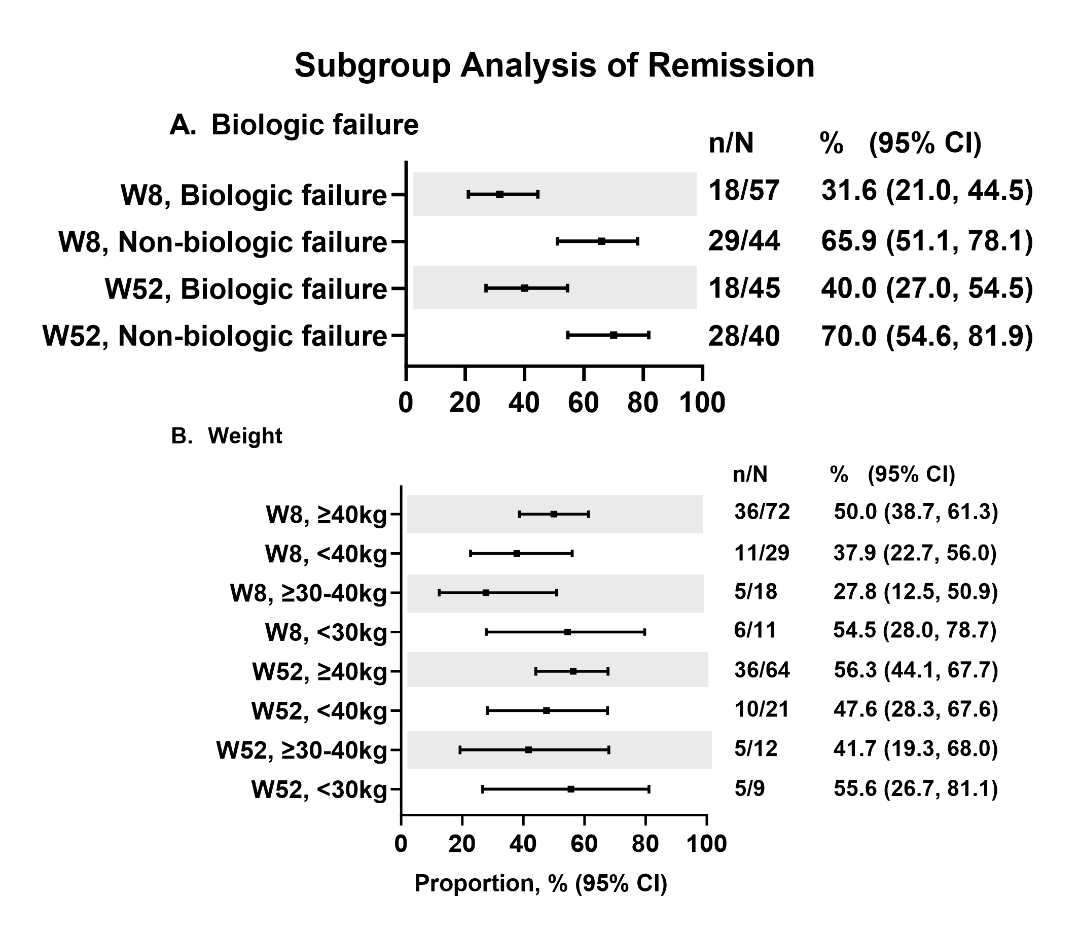
图1 缓解情况亚组分析
维持治疗阶段,8周给药组和12周给药组的疗效相当,不良事件和严重不良事件发生率也相似。16.8%(17/101)的患者发生严重不良事件,其中CD恶化最常见(5/17);严重感染发生率为5.9%。
乌司奴单抗在儿童CD患者中耐受性良好,未发现新的安全性信号。乌司奴单抗诱导和维持治疗方案在中重度儿童CD患者治疗中有效。