前言
研究背景
脑转移是晚期实体瘤患者发病和死亡的重要原因。约10%–25%的转移性癌症患者会发生脑转移,乳腺癌是继
传统上,脑转移患者的标准治疗依赖于手术、放疗及全身治疗的联合。近年来,一些小分子靶向药物已在脑转移中显示出一定疗效。与此同时,ADC作为新兴治疗策略,其复杂活性可作用于具有异质性靶点表达的肿瘤。研究表明,即使ADC分子体积相对较大,仍能递送足量细胞毒性药物至脑转移灶。
ADC治疗乳腺癌脑转移:临床前证据
多项临床前研究支持ADC对乳腺癌脑转移的活性。例如,在脑转移雌性裸鼠模型中,
ADC对乳腺癌脑转移的临床疗效
高达50%的HER2过表达(HER2+)转移性乳腺癌患者会发生脑转移。表1概述了涉及使用ADC治疗的HER2阳性/HER2低表达转移性乳腺癌患者的临床试验。
表1 ADC在HER2阳性/HER2低表达转移性乳腺癌伴脑转移患者中的疗效[1]
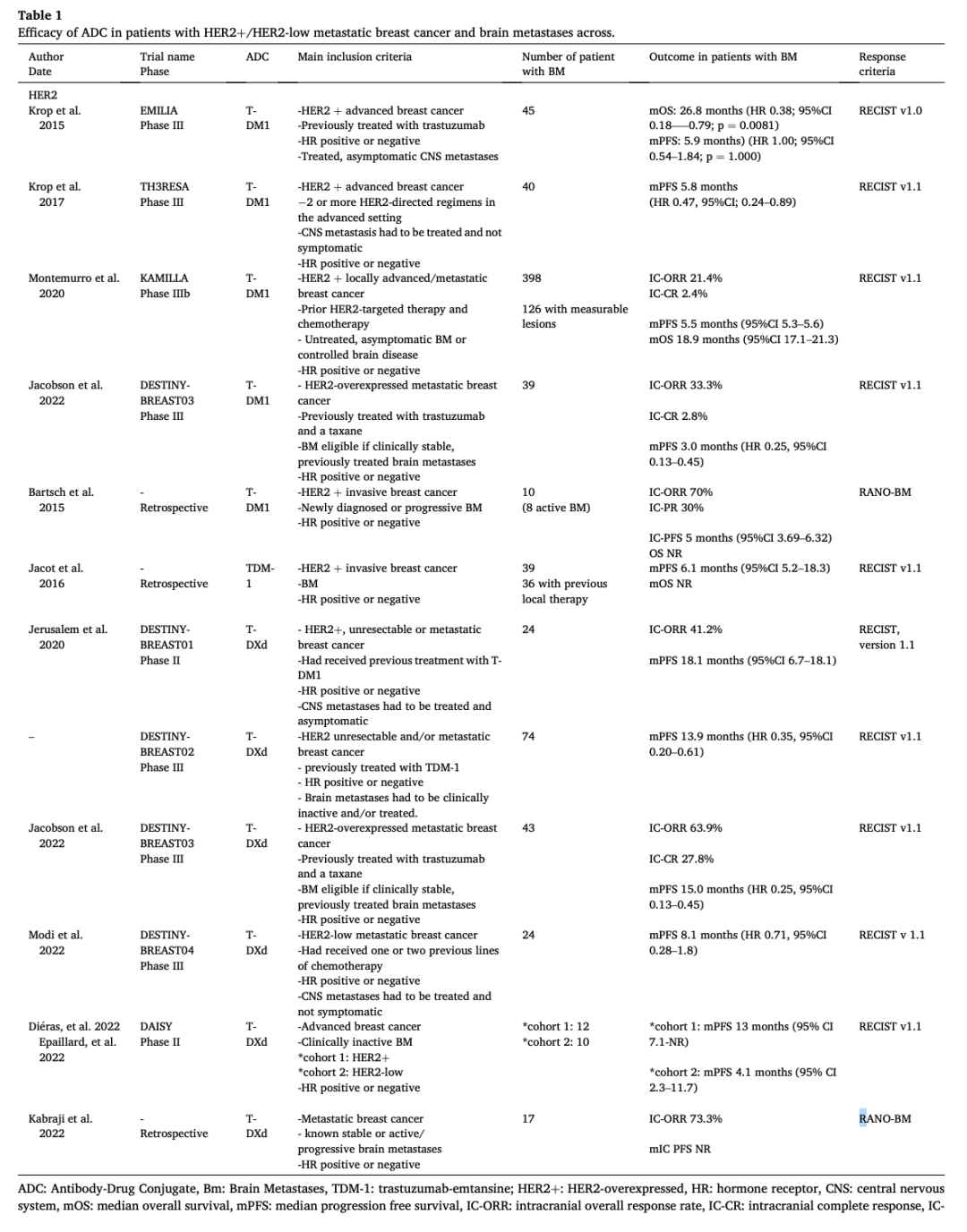
T-DM1
T-DM1由曲妥珠单抗与细胞毒性抗微管药物DM1通过不可切割的硫醚连接子偶联而成。多项临床试验评估了T-DM1在HER2阳性乳腺癌脑转移患者中的疗效。在EMILIA试验的先前接受过治疗且无症状的中枢神经系统(CNS)转移亚组中,T-DM1组中位总生存期较对照组显著延长(26.8个月 vs 12.9个月)。TH3RESA试验中,T-DM1在CNS转移患者中亦显示出PFS获益。KAMILLA研究显示,在可测量脑转移灶患者中,T-DM1的颅内客观缓解率(ORR)为21.4%,中位无进展生存期(mPFS)为5.5个月。
T-DXd
T-DXd通过一个基于四肽的可切割连接子,将靶向HER-2的人源化单克隆抗体与拓扑异构酶I抑制剂偶联。DESTINY-Breast01研究中,基线有脑转移的患者mPFS达18.1个月,可测量脑转移患者的颅内客观缓解率(IC-ORR)为41.2%。在DESTINY-Breast03研究中,T-DXd组脑转移患者的IC-ORR达63.8%,mPFS为15.0个月,均优于T-DM1组。DESTINY-Breast04研究在HER2低表达脑转移患者中也观察到T-DXd的颅内活性趋势。
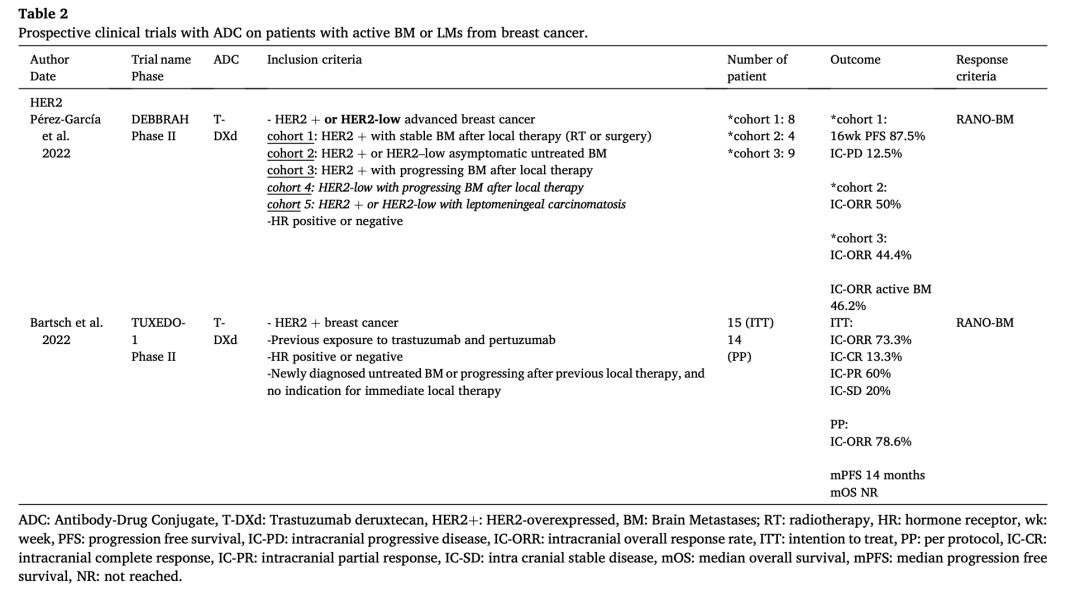
值得注意的是,两项前瞻性临床试验(DEBBRAH试验和TUXEDO-1试验)特别探索了T-DXd对乳腺癌脑转移和/或软脑膜转移的疗效(表2)。DEBBRAH是一项正在进行的II期试验;TUXEDO-1研究的事后分析显示,T-DXd在未接受局部治疗的新发脑转移患者中IC-ORR达100%。
表2 ADC在乳腺癌活动性脑转移或软脑膜转移患者中的前瞻性临床试验[1]
滋养层细胞表面抗原2(Trop-2)是一种传递细胞内钙信号的跨膜糖蛋白,在包括80%乳腺癌在内的多种上皮性肿瘤中过表达,回顾性研究表明,Trop-2过表达与更差的预后相关。
SG
SG由抗Trop-2抗体与拓扑异构酶I抑制剂SN-38(
新型ADC结构及联合治疗探索
MM-302(靶向HER2的
表3 针对乳腺癌脑转移的新型ADC药物临床试验[1]

目前研究正在探索ADC与靶向治疗、免疫检查点抑制剂或化疗的联合。例如,T-DM1联合
结论与展望
近年来,新型ADC显著改善了转移性乳腺癌的治疗结局。然而,脑转移仍是重大挑战,相关研究多排除或未详细报告CNS受累患者数据。此外,探索第三代ADC在活动性脑转移或软脑膜疾病患者中疗效的研究极为有限。现有初步数据显示,ADC对活动性脑转移患者展现出抗肿瘤活性。鉴于CNS转移预后不佳,亟需在这一人群中开展对ADC等新型治疗方案的研究。同时,新一代ADC的设计需充分考虑血脑屏障穿透能力、药物抗体比等特点。目前多项评估新型ADC及联合方案的临床试验正在进行中,其结果有望进一步推动临床对脑转移的理解和治疗选择。
参考文献:
[1] Epaillard N, Bassil J, Pistilli B. Current indications and future perspectives for antibody-drug conjugates in brain metastases of breast cancer. Cancer Treat Rev. 2023 Sep;119:102597.
编辑:Dana
审校:Uni
排版:Ben
执行:Ocean
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)