
在心内科的临床实践中,抗
理解抗心律失常药物的核心机制与致心律失常风险,绝非纸上谈兵,而是精准治疗的关键。例如,为何Ic类药物在房颤合并心衰患者中慎用?为何纯粹的IKr阻滞剂(如
严干新教授团队的这篇最新综述,正是为我们系统梳理了这一关键知识图谱。文章深入浅出地阐释了:
1.作用基石:从动作电位各期离子流出发,阐明了决定有效不应期(ERP)的细胞学基础。
2.核心机制:聚焦折返这一主要心律失常机制,清晰解读了钠通道阻滞剂与钾通道阻滞剂延长ERP、发挥抗心律失常作用的不同路径。
3.风险之源:深刻剖析了“使用依赖性”如何导致传导减慢与引发
4.治疗新策:重点探讨了以Ito通道为靶点、抑制“2相折返”在J波综合征治疗中的独特价值与策略。
掌握这些离子与细胞学原理,将使我们不再机械地记忆药物分类与禁忌,而是能从电生理本质理解药物行为,从而更自信、更安全地驾驭抗心律失常药物,为患者制定个体化治疗方案。
现在,让我们跟随这篇权威综述,一同深入抗心律失常药物作用的核心,揭开其疗效与风险并存的奥秘。
来源:心言豆语

心脏作为电同步细胞团运作,其协调的电激活与传导可确保同步收缩,从而实现高效泵血功能。每个心肌细胞因其细胞膜上存在多种离子通道而具有电兴奋性,这些离子通道调控细胞内外的离子运动。心肌细胞的电特性因细胞类型而异,主要由其离子通道的组成与及其相应功能决定。离子通道的正常活性对维持正常电传导和心律至关重要。在病理状态下,协调的电激活与传导可能被破坏或改变,导致异常心律(即心律失常),可分为异常缓慢(心动过缓)或异常快速(心动过速)两类。本文重点探讨心动过速,通常分为两大类:(1)异常激活,包括自律性增强与触发活动;(2)异常电传导,导致折返运动。
自20世纪10年代以来,当从金鸡纳树皮中提取的生物碱奎尼丁被确认为治疗
本综述探讨了参与心肌细胞电活动的关键离子通道,以及动作电位(AP)产生、异质性和传导机制。此外,重点阐述了心律失常发生的主要机制,特别关注作为临床心律失常主要病因的折返性心律失常,以及抗心律失常药物的作用及其相关的促心律失常风险。本综述主要聚焦于心室(肌)和心房(肌)快反应动作电位,这些是I类和III类抗心律失常药物的主要作用靶点。而由钙电流而非钠电流主导、具有独特电生理特性的起搏细胞(慢反应)动作电位,则不在此文讨论范围。


心脏的协调电激活及扩布依赖于心肌动作电位(AP)的产生与传导,后者定义为单个心肌细胞膜电位的瞬时快速变化。这些电信号使心房与心室实现同步收缩,从而确保心泵功能的有效运作。深入理解动作电位(产生)的离子电流与细胞(学)基础(包括除极、复极及不应期)对于阐明心律失常的发生机制至关重要。此类知识不仅为抗心律失常药物的临床应用奠定基础,亦有助于识别其潜在的促心律失常风险。非起搏细胞(如浦肯野纤维、大多数的房室旁路细胞、心房肌及心室肌细胞)动作电位分为5期,每期均涉及特定离子运动,产生跨膜内向或外向电流(如图1所示)。
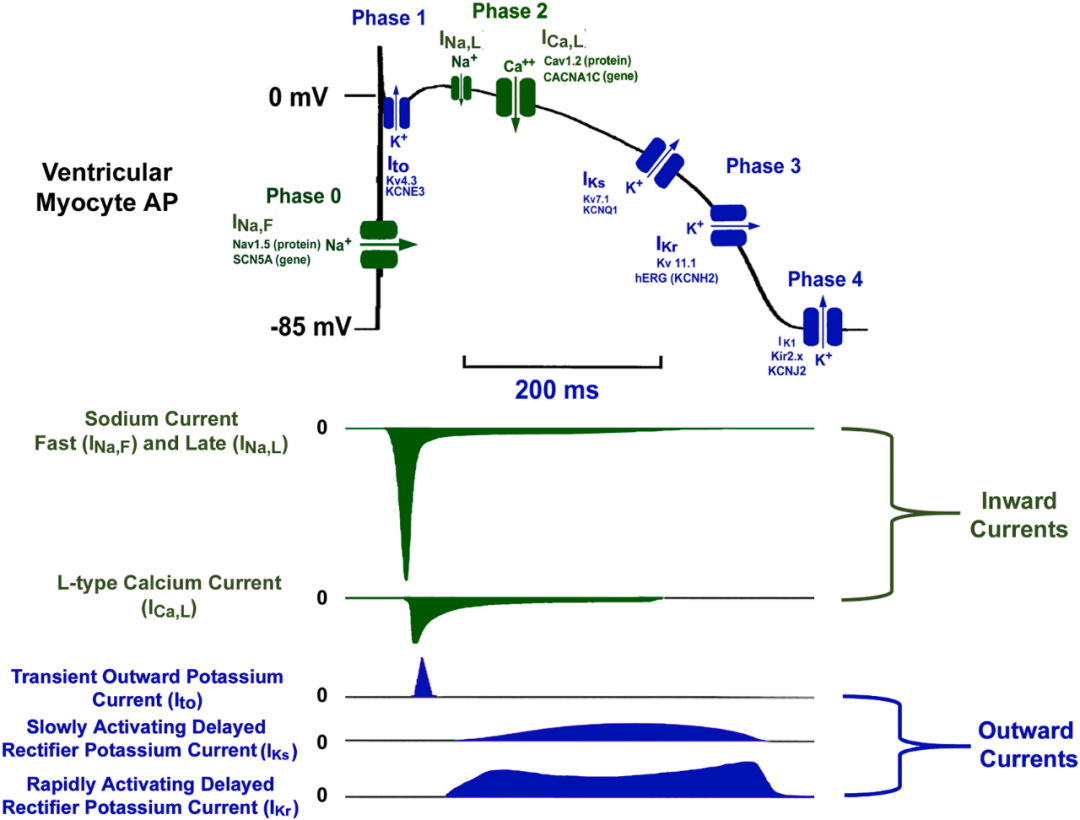 图1:心室肌细胞的主要离子流:蓝色代表外向电流,绿色代表内向电流。各离子通道均标注三类名称,依次为:电流名称、蛋白质名称与基因名称。
图1:心室肌细胞的主要离子流:蓝色代表外向电流,绿色代表内向电流。各离子通道均标注三类名称,依次为:电流名称、蛋白质名称与基因名称。
0期——快速除极
当受到刺激时,心肌细胞动作电位的0期开始,标志着心肌细胞的兴奋。在此阶段,电压门控钠通道(NaV1.5)迅速开放,允许钠离子(Na+)快速内流。该内流导致膜电位从约-85mV急剧上升至+35 mV。引发此快速除极的钠电流被称为快钠电流(INa,F)。这些钠通道在数毫秒内失活,0期结束。0期去极化上升速率和幅度是心肌传导速度的关键决定因素。
1期—复极初期
此时大多数电压门控钠(Na+)通道失活,瞬时外向钾(K+)通道(Ito)短暂开放,导致轻微复极。Ito电流的显著增大与J波综合征相关,后者与心脏性
2期—平台期
L型钙通道开放,允许Ca2+离子进入细胞,产生内向钙电流(ICa,L)。此外,一小部分钠通道缓慢失活,保持开放,形成晚钠电流(INa,L)。这两种内向电流与外向K+电流相互平衡,从而形成动作电位中特征性的平台期。平台期对于确定有效不应期(ERP)至关重要。INa,L不仅影响动作电位时程(APD),而且还在APD /QT间期的频率适应性以及抗心律失常药物的反向使用依赖性中起重要作用。
3期—快速复极
此时,钙通道和晚钠通道失活,而延迟整流钾通道(IKr和IKs)保持开放,导致K+离子外流,膜电位恢复至复静息水平。在未使用抗心律失常药物的生理条件下,ERP及其后续相对不应期(RRP)在此阶段结束。
4期—静息电位
细胞维持稳定的静息电位,主要归功于内向整流钾通道(IK1)的活性,其将膜电位维持在接近钾平衡电位的水平。在此阶段,钠(Na+)通道虽处于关闭状态,但已从失活状态完全恢复,可对下一个去极化刺激做出响应而开放。起搏细胞动作电位(AP)的离子机制超出了本综述的讨论范围。
兴奋后,心脏立即进入不应期,在此期间对进一步的刺激无反应。此期与动作电位形态及时程密切相关,对于确保心脏节律和协调泵血功能至关重要。不应期通过防止心肌细胞过早再兴奋,有助于避免不规则心律。动作电位时程定义为从0期去极化开始到3期复极化结束的时间间期。它是不应期的关键决定因素,对有效不应期(ERP)和相对不应期(RRP)均有影响。心肌细胞的不应期可分为两部分。
有效不应期(ERP)
指心肌细胞兴奋后,即使给予足够强度的刺激也无法引发新的可扩布动作电位的时期。临床上,ERP通常通过程序化刺激评估,即以固定周长施加一刺激序列(S1),随后以固定强度(等于舒张阈值的两倍)、不同间隔给予额外刺激(S2)。ERP被定义为S2未能引发可扩布动作电位的最长S1-S2间期。
相对不应期(RRP)
紧随ERP之后是RRP,即刺激能够引发新的动作电位的时期。然而在此期间,动作电位0期去极化速度及其传导速度均较正常时慢。
心脏中存在两种类型的动作电位,其静息膜电位不同,负责细胞兴奋的内向离子电流也存在差异:(1)依赖钠通道兴奋和0期去极化的动作电位;(2)依赖钙通道兴奋和0期去极化的动作电位(如图2A、B所示)。这些根本性差异导致ERP、RRP的特征各异以及相应的传导模式与速度的变化(表1)。在INa,F依赖性AP中,0相快速除极、高AP振幅及短暂RRP使得其在生理条件下以“全或无”方式实现快速传导。即这些AP要么以全速传导,要么完全无法传导。相比之下,ICa,L依赖性AP表现出0相上升速度较慢、振幅较低及RRP延长,导致传导速度减慢且呈递减性。
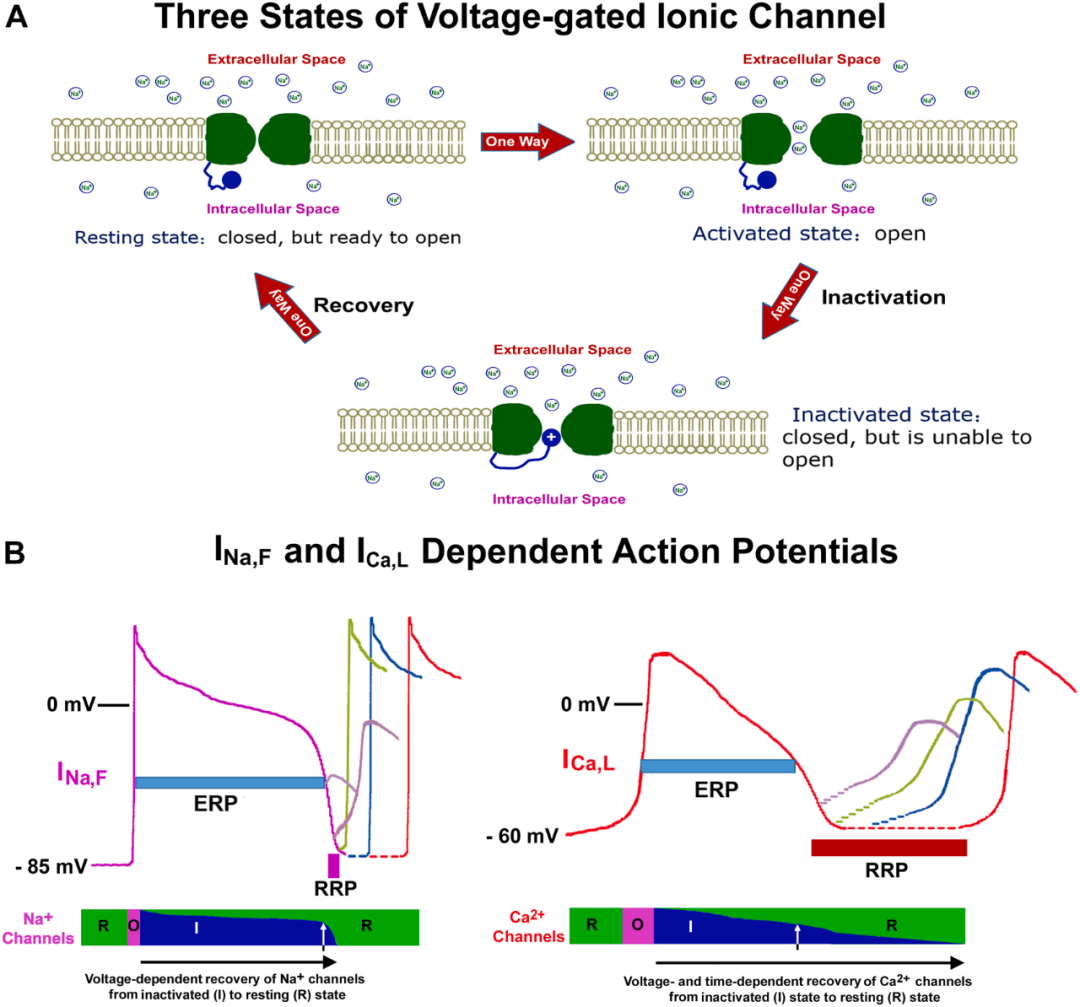 图2:电压门控离子通道的三种状态与两种动作电位类型。(A) 钠通道三种功能状态的示意图:静息态、激活态(开放)和失活态。(B) 比较由钠电流介导兴奋与L型钙电流介导兴奋的细胞动作电位差异。需注意在钙控细胞,钙通道从失活态恢复至静息态的过程于ERP后变得非常缓慢,导致相对不应期(RRP)明显延长。蓝色表示失活态通道百分比,绿色表示静息态通道百分比。ERP:有效不应期;RRP:相对不应期。
图2:电压门控离子通道的三种状态与两种动作电位类型。(A) 钠通道三种功能状态的示意图:静息态、激活态(开放)和失活态。(B) 比较由钠电流介导兴奋与L型钙电流介导兴奋的细胞动作电位差异。需注意在钙控细胞,钙通道从失活态恢复至静息态的过程于ERP后变得非常缓慢,导致相对不应期(RRP)明显延长。蓝色表示失活态通道百分比,绿色表示静息态通道百分比。ERP:有效不应期;RRP:相对不应期。
在心肌细胞中,大多数离子通道的通透性,即其开放与关闭过程,呈电压依赖性。这些电压门控离子通道会经历三种主要状态(见图2A):静息态、激活态和失活态。在静息态时,通道处于关闭状态,但能够响应刺激而开放——例如静息膜电位下的钠通道。激活态时,通道处于开放状态,允许离子流动。失活态时,通道从激活态关闭,暂时对进一步刺激无反应。在重新开放前,通道必须从失活态恢复到静息态。从心肌细胞的角度来看,ERP(有效不应期)的长短由复极过程中恢复至静息态的离子通道比例是否达到特定的阈值来决定。例如,在钠通道介导动作电位0相去极化的细胞中,只要从失活态恢复至静息态的钠通道数量低于临界阈值,细胞就保持不可兴奋状态。当足够多的钠通道恢复至静息态而超过该阈值时,ERP结束,细胞可产生新的动作电位。
这一恢复过程既具有电压依赖性又具有时间依赖性。更负的膜电位会加速钠通道和钙通道从失活态恢复至静息态的过程。这解释了为何INa,F依赖性动作电位具有较短的相对不应期(RRP):快速复极至更负电位可促进电压依赖性通道活性快速恢复。相比之下,ICa,L依赖性动作电位由于在更正膜电位下通道(活性)恢复较慢,此恢复过程更依赖时间而非电压,故其RRP更长。INa,F与ICa,L依赖性动作电位在RRP上的显著差异决定了它们不同的传导模式,如表1所示。关于特殊传导方式的讨论不在本综述范围。
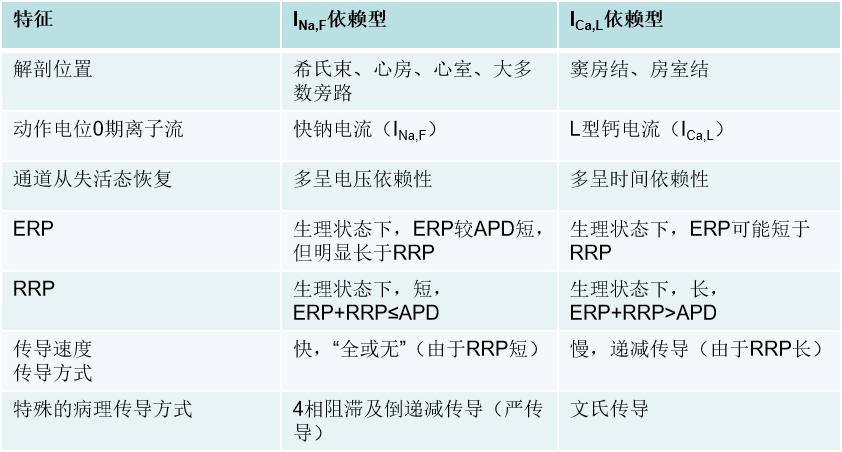


折返是多种心律失常(如瘢痕介导的室性心动过速、心房扑动和心房颤动)维持的最常见机制。这里的“折返”是指激动波围绕障碍物连续传播,使其重新回到“原点”。在此过程中,心肌细胞依次从兴奋中恢复,以备后续波峰到达时再次激活。这些障碍物可为解剖性障碍(如瘢痕组织、正常结构如二尖瓣和三尖瓣环等),或功能性障碍(因兴奋后不应期导致的心肌“电失活”区域)。
目前普遍认为:电冲动围绕障碍物进行连续、循环运动的条件(如图3A所示)是该激动的波长必须短于折返环长。该条件可确保激动的波峰不会遇到处于ERP的心肌组织。激动的波长(λ)由传导速度(CV)和组织的ERP的乘积决定:λ= CV ×ERP。
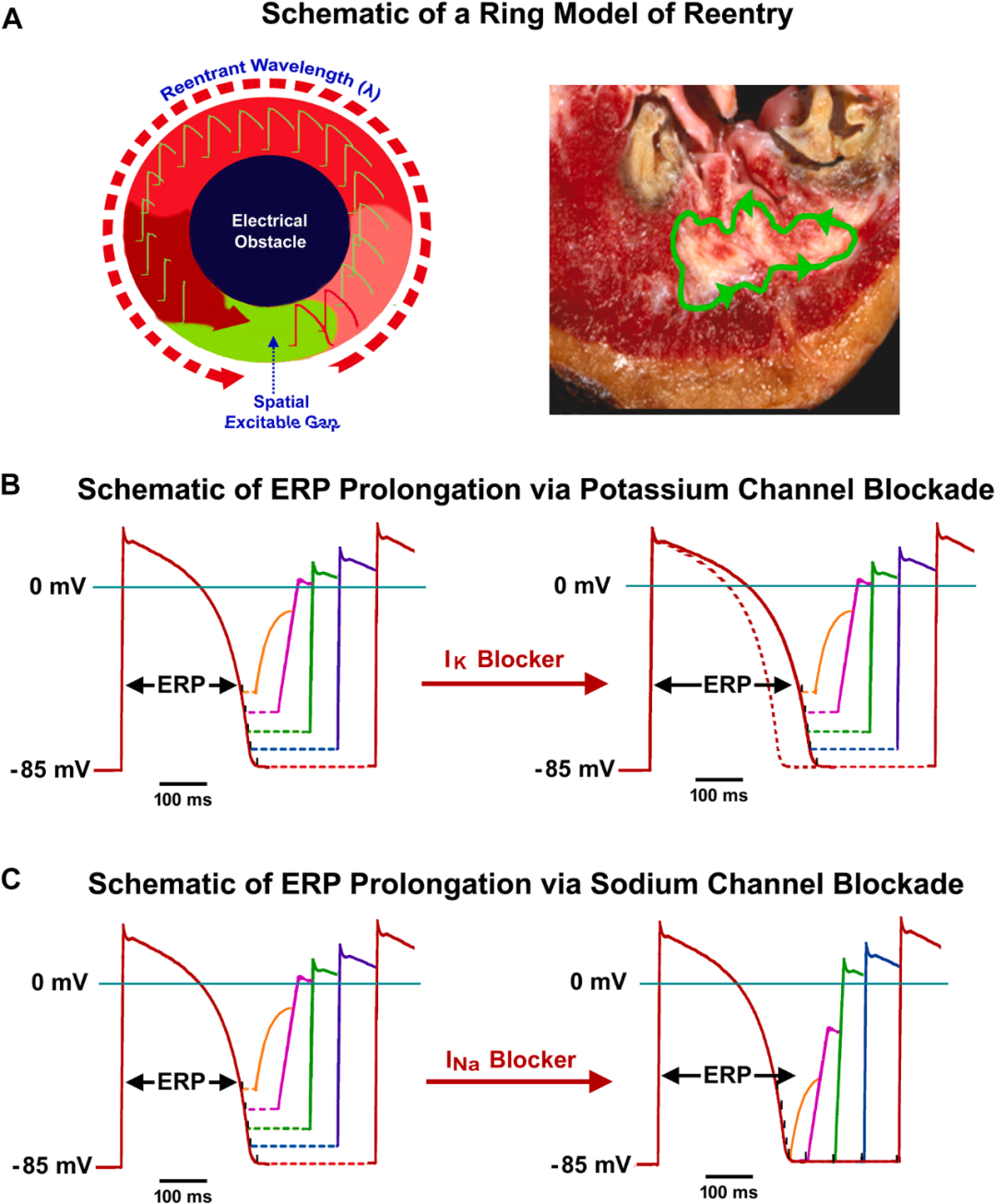
图
3. 折返、有效不应期(ERP)与抗心律失常作用。(A) 环状模型示意图,阐释折返机制。该机制是绕过固定解剖结构或电学障碍(如瘢痕组织)引发折返性心动过速的基础。(B) 钾通道阻滞剂延长APD致ERP延长。(C) 钠通道阻滞剂作用于钠控细胞致ERP延长。纯钠通道阻滞可略微缩短APD,从而产生复极后不应期。APD:动作电位时程;ERP:有效不应期。心脏内存在天然解剖学障碍,如三尖瓣环和二尖瓣环,理论上可作为折返性电活动的传导通路。然而在健康心脏中,由于激动波长长于折返环长,折返性心律失常不会发生。减慢传导速度或缩短ERP可缩短激动的波长,在激动的波峰与波尾之间形成可激动间隙,从而有利于折返性心律失常的发生。
理论上,有两种策略可以增加激动波长以终止折返:提高传导速度和延长ERP。然而,目前临床上尚无药物能有效增快传导速度。因此,现有抗心律失常药物主要通过延长ERP来治疗折返性心律失常。这可以通过阻断外向钾电流(主要是IKr,图3B)延长APD,或者抑制钠电流(INa,图3C)(对心房和心室肌的兴奋至关重要)等来实现。在临床实践中,许多抗心律失常药物——如Ia类药物和胺碘酮可同时作用于外向钾电流和钠电流。
纯IKr阻滞剂延长有效不应期
几乎所有延长 APD 的药物均主要通过抑制IKr起作用。在III类抗心律失常药中,多非利特和索他洛尔被认为是纯粹的IKr阻断剂。如图3B所示,APD延长,特别是在平台期,与ERP延长之间的关联是直观的,因为钠通道从失活状态恢复很大程度上依赖于电压。
INa阻滞剂延长有效不应期
INa阻滞剂延长ERP的机制并不简单。与IKr阻滞剂不同,INa阻滞剂延长ERP的机制是通过减少可用于(细胞)再兴奋的可用钠通道(数量)而非延长APD。事实上,纯钠通道阻滞实际上可能缩短APD(注释:直接抑制晚钠电流)。
INa抑制与两种电生理学结果相关:(1)动作电位0期最大上升速度减慢,传导减慢;(2)复极化晚期可重新开放的钠通道数量减少,即钠通道从失活状态恢复的时间延长,这是由于该过程具有电压依赖性和时间依赖性;这反过来延长了ERP。因此,INa阻滞剂可以使ERP延长至APD之后,这种现象称为复极后不应期。
普遍的误解是,减慢折返环路内的传导可以阻止折返冲动的传播。实际上,减慢传导可通过为折返环路提供更多(可激动)时间来促进折返。


抗心律失常和致心律失常效应是同一枚硬币的两面。深刻理解抗心律失常药物的致心律失常机制对于使其疗效最大化至关重要。
抗心律失常药物的使用依赖性
所有内向电流阻滞剂(包括钠通道阻滞剂和钙通道阻滞剂)均表现出使用依赖性或频率依赖性——即激活频率越高,通道阻滞程度越显著。
I类抗心律失常药物主要根据其对钠通道的使用依赖程度分为三种。
Ic类药物(如氟卡尼和普罗帕酮)表现出强使用依赖性,其次是Ia类药物(如奎尼丁和普鲁卡因胺)。相比之下,Ib类药物(如美西律)则显示弱使用依赖性。
众所周知,Ic类抗心律失常药物通过钠通道阻滞的强使用依赖性,可导致冠心病高危患者或心室收缩功能减退患者死亡率增高。由于中效至强效的使用依赖性,Ia类和Ic类抗心律失常药物应避免用于收缩性心力衰竭患者。另一方面,具有弱使用依赖性的INa阻滞剂(如Ib类药物美西律)被认为可安全用于结构性心脏病患者。钠通道阻滞剂的强效使用依赖性可导致促心律失常效应。图4A展示了一个由Ic类药物氟卡尼诱发的宽QRS心动过速病例。患者为28岁女性,有先天性房间隔缺损外科修补术及阵发性房颤病史。患者每日两次、每次服用100mg氟卡尼,并联用美托洛尔;因主诉头晕胸闷就诊于急诊科。初次心电图显示房扑伴1:1房室传导,心率216次/分钟,同时伴有类似室性心动过速的宽QRS波群。
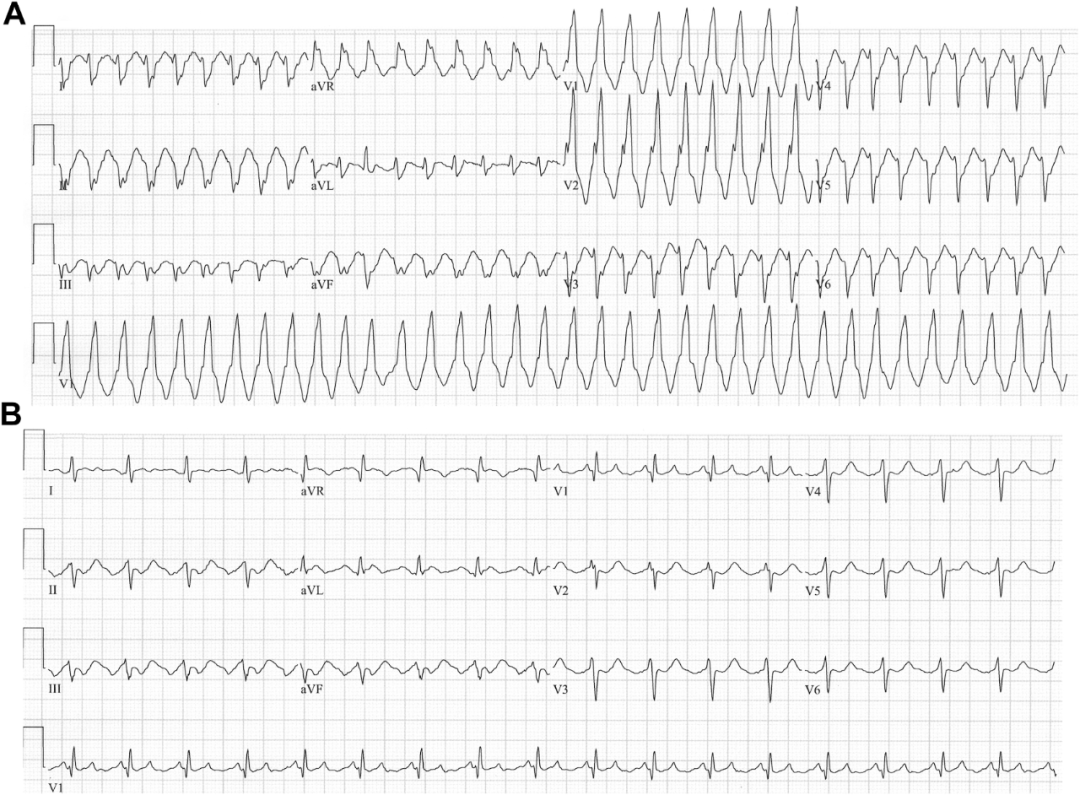 图4. Ic类钠通道阻滞剂的强使用依赖性。(A) 一名28岁女性因阵发性房颤每日两次、每次服用100 mg氟卡尼治疗时,出现宽QRS波群心动过速。(B) 静脉注射胺碘酮后,心电图显示缓慢房扑伴2:1房室传导及QRS波群变窄。该房扑频率与图A所示宽QRS心动过速的心室率完全一致。这表明图A中的宽QRS心动过速为房扑伴1:1房室传导,其QRS波增宽归因于氟卡尼对INa,F的强使用依赖性抑制。
图4. Ic类钠通道阻滞剂的强使用依赖性。(A) 一名28岁女性因阵发性房颤每日两次、每次服用100 mg氟卡尼治疗时,出现宽QRS波群心动过速。(B) 静脉注射胺碘酮后,心电图显示缓慢房扑伴2:1房室传导及QRS波群变窄。该房扑频率与图A所示宽QRS心动过速的心室率完全一致。这表明图A中的宽QRS心动过速为房扑伴1:1房室传导,其QRS波增宽归因于氟卡尼对INa,F的强使用依赖性抑制。
本例中氟卡尼表现出显著的使用依赖性,导致:(1) 大折返性环路(如三尖瓣环周围)内传导显著减慢,致房扑频率相对缓慢且呈现1:1房室传导;(2) 高心室率时QRS波显著增宽。静注胺碘酮后,心电图(图4B)显示典型房扑波形,伴2:1房室传导及窄QRS波群。
抗心律失常药物的反向使用依赖性
目前已充分证实,心室复极(通过APD和QT间期反映)能够适应心率变化,即在较快心率时缩短,在较慢心率时延长。IKr阻滞会延长APD和QT间期,并放大这种与心率相关的复极化适应性。这种现象称为反向使用依赖性,即IKr阻滞剂在较慢心率下比较快心率下产生更显著的 APD /QT间期延长的倾向。
然而,重要的是要强调,反向使用依赖性并非IKr阻滞剂所特有,而是与APD延长本身相关的内在特性。在未同时抑制晚钠电流(INa,L)的情况下(晚钠电流是参与复极频率适应性及反向使用依赖性的关键电流),较长的动作电位时程(APD)在较慢心率下表现出更显著的心率依赖性延长。如图5A所示,即使在没有IKr阻滞的基线条件下,在长间歇后,QT间期延长同时伴随有Tp-e间期(心室复极离散度的指标)不成比例的更大增加。这一观察结果表明,较长的动作电位时程在长间歇后或更慢心率时会更显著的延长,从而导致Tp-e/QT比值(Tp-e指T波顶峰至T波终末的间期)增加。
这一现象在先天性长QT综合征中更为明显,表现为复极化在较慢心率下不成比例地进一步延长。Tp-e/QT比值作为多形性室性心动过速(包括尖端扭转型室性心动过速)易感性的指标最早由Yan及其同事于2006年提出。
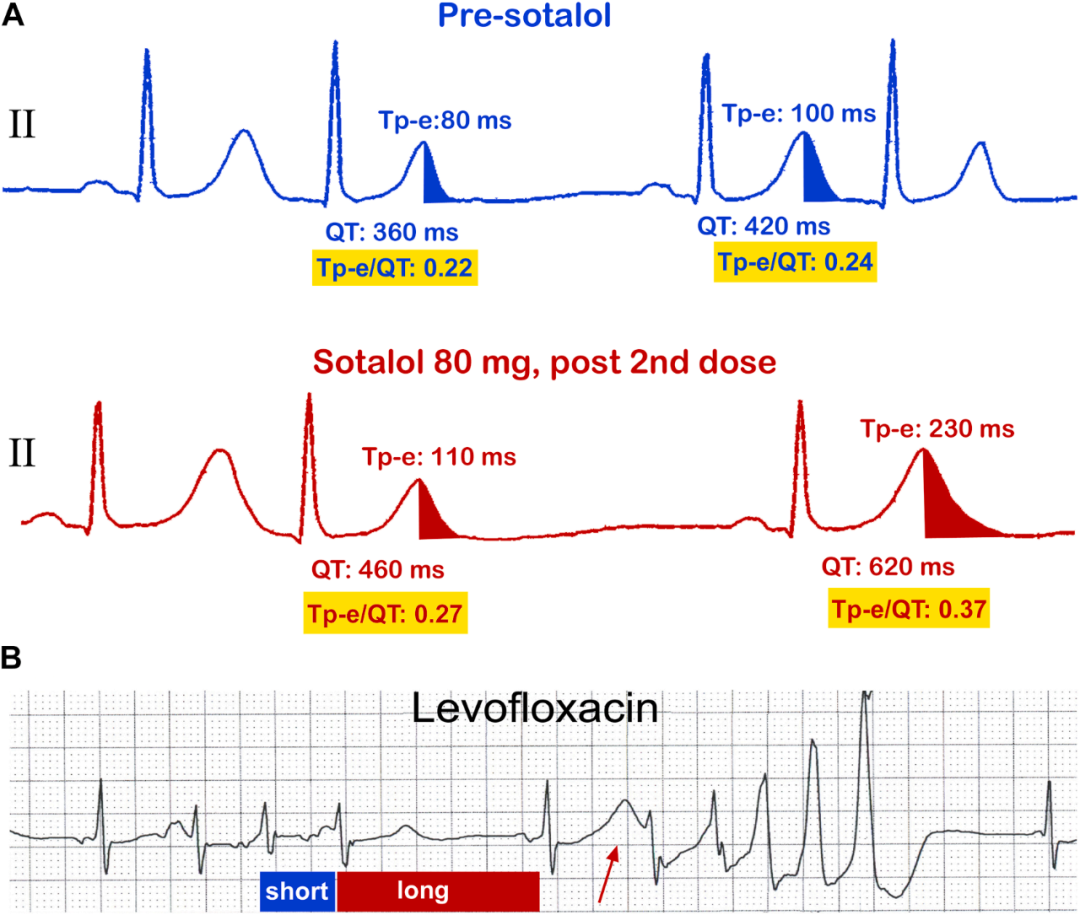 图5. 纯IKr阻滞剂的反向使用依赖性。(A) IKr阻滞剂索他洛尔显著增强了长间歇依赖的QT间期及Tp-e的延长,表现为显著的T波—这是反向使用依赖性的典型特征。反向使用依赖性的显著特征在于Tp-e增幅超过QT间期增幅,导致Tp-e/QT比值显著升高。 (B) IKr阻滞剂左氧氟沙星在短-长周期序列后诱发显著QT间期延长及显著T波。随后长偶联间期R-on-T室早触发了TdP。图中红色箭头标示了伴随显著T波的明显QT间期延长。
图5. 纯IKr阻滞剂的反向使用依赖性。(A) IKr阻滞剂索他洛尔显著增强了长间歇依赖的QT间期及Tp-e的延长,表现为显著的T波—这是反向使用依赖性的典型特征。反向使用依赖性的显著特征在于Tp-e增幅超过QT间期增幅,导致Tp-e/QT比值显著升高。 (B) IKr阻滞剂左氧氟沙星在短-长周期序列后诱发显著QT间期延长及显著T波。随后长偶联间期R-on-T室早触发了TdP。图中红色箭头标示了伴随显著T波的明显QT间期延长。
IKr阻滞剂的反向使用依赖性,特别是在短-长周期序列时,会显著增加Tp-e/QT比值,并促进TdP(一种与QT间期显著延长相关的多形性室速)的发生。这一现象如图5A、B所示。这也解释了为什么TdP总是始于显著或宽大的T波,其反映了复极离散度的增加和早后除极的发生。
有人可能会争辩说,胺碘酮也可显著延长QT间期,但为什么其TdP发生率很低。这实因胺碘酮不仅阻断IKr,还抑制INa,L。此外,INa,L的抑制减弱了由IKr阻滞引起的复极化不成比例延长,如用胺碘酮时所见,尤其是在APD本身就更长的细胞类型中,如心内膜下细胞。
该作用降低了心室复极离散度(表现为Tp-e/QT比值的降低),从而降低了TdP的易感性,尽管QT间期绝对值明显延长。由于INa,L在各种形式的QT间期延长中均相对增加,其抑制在所有长QT综合征中或多或少是有益的,无论其根本原因如何。
例如,美西律(mexiletine)作为一种选择性晚钠电流(INa,L)抑制剂,已被证实可缩短QT间期,在多种长QT间期综合征中降低Tdp的发生率,包括先天性LQT2、LQT3和LQT8、以及应激性心肌病和多非利特诱导的长QT间期时。这些研究结果表明,美西律可作为广谱抗心律失常药物用于多种病因的长QT综合征。若欲进一步深入了解相关内容,可参阅Olleik及其同事近期发表的综述。此外,在接受节律控制治疗的房颤患者中,多非利特与美西律的联合用药不仅可减轻QT间期延长,还能明显延长维持窦律的时间。


2相折返是J波综合征短偶联间期室早触发多形性室性心动过速的唯一机制。然而,有关J波综合征的心电图识别及其致心律失常机制仍存在若干误解。清晰理解其潜在的离子和细胞学基础,对于准确诊断及有效治疗至关重要。
J波及J波综合征
直到1996年J波的离子和细胞学基础方被阐明。当时Yan和Antzelevitch开发了一种新的实验模型—动脉灌注的犬心室楔形标本—在此模型中,可以通过跨壁ECG同时记录心外膜和心内膜的跨膜动作电位。如图6A所示,J波(箭头指示)对应于心室心外膜动作电位的1相和2相之间的切迹,这一过程由瞬时外向钾电流(Ito)介导。这一关于J波离子和细胞学基础的发现,促使Yan和Antzelevitch于1996年1月首次命名Brugada综合征,其特征为V1至V3导联出现J波。
认识到Brugada综合征、传统早期复极综合征以及其他与J波相关的多形性室速或室颤之间的机制联系,最终导致Yan及其同事在2004年引入了更广泛的术语“J波综合征”。然而,对J波综合征的历史认识和理解过程,仍存在一些误解。
Brugada波实为出现在心电图V1-V3导联上的J波
如图6B所示,Brugada I型和II型波在V1至V3以外的导联中可出现对应的“等同”表现(J波 I型和II型)。Brugada I型波对应于非右前胸导联中显著的J波伴倒置T波(J波 I型),而Brugada II型模式可镜像为传统的早期复极模式—以J点抬高或J波为特征,随后出现ST段凹面向下抬高及显著T波(J波II型)。Brugada I型与II型波及其对应J波的主要区别在于QRS电轴的方向。如图6C所示,将Brugada I型和II型波时的QRS轴翻转180度可产生I型和II型J波模式,以及相应的ST段和T波形态。
J波是一种复极波成分,而非除极波成分
由于J波发生于QRS波群与ST段的交界处,可能被误认为室内传导延迟。需要强调的是,J波是一种复极现象,由心室心外膜动作电位1期增大的Ito电流(瞬时外向钾电流)所介导。SCN5A基因突变患者可能同时存在传导异常;然而,这些异常并非J波综合征多形性室性心动过速的主要原因。J波振幅随心率减慢而增高,随心率加快而降低,与图6A所示心外膜动作电位切迹的变化一致。相比之下,室内传导延迟则表现相反,通常在心率增快时变得更加明显,这是由于依赖于心率的传导减慢或阻滞所致。
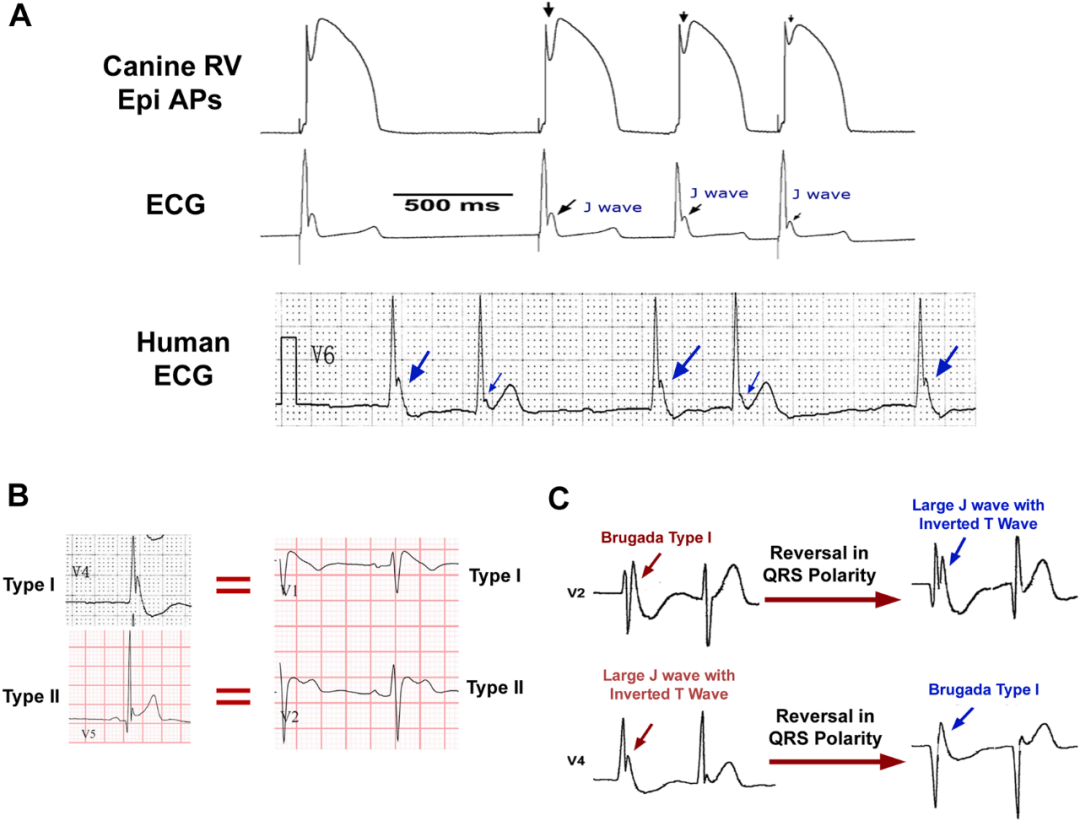 图6. J波与Brugada波。(A) J波是由伊藤介导的心外膜动作电位(Epi AP)缺口决定的复极化成分。其振幅与心率相关,随心外膜动作电位缺口幅度的变化而平行变化。(B) 根据除V1至V3导联外的ECG导联中J波和ST段的特征,J波模式可分为I型和II型,分别对应Brugada I型和II型模式。(C) J波与Brugada波的唯一区别在于QRS轴的取向。人为反转QRS轴可将I型和II型J波模式转化为Brugada I型和II型模式,反之亦然。
图6. J波与Brugada波。(A) J波是由伊藤介导的心外膜动作电位(Epi AP)缺口决定的复极化成分。其振幅与心率相关,随心外膜动作电位缺口幅度的变化而平行变化。(B) 根据除V1至V3导联外的ECG导联中J波和ST段的特征,J波模式可分为I型和II型,分别对应Brugada I型和II型模式。(C) J波与Brugada波的唯一区别在于QRS轴的取向。人为反转QRS轴可将I型和II型J波模式转化为Brugada I型和II型模式,反之亦然。
2相折返和多形性室性心动过速
2相折返发生在各种原因导致的心外膜细胞动作电位穹隆不均一丢失,导致动作电位2期局部再兴奋。这种再兴奋可触发早搏,引发多形性室速或室颤。2相折返的形成需具备两个关键前提条件。
存在延迟的2相上升支(动作电位穹隆延迟)
(延迟的)心外膜动作电位穹隆为再兴奋提供了必要的去极化电流。为了形成(延迟的)动作电位穹隆,Ito必须大到足够产生一个深的心外膜切迹,该切迹的最低电位可接近激活L型钙电流(ICa,L)的阈电位。这可以在动作电位穹隆完全消失之前产生一个延迟的动作电位穹隆—通常在心率较慢时。

显著的复极离散
心室心外膜(心肌)动作电位穹隆丢失常具有空间异质性。在此期间(动作电位2期),一些心外膜细胞表现为“穹隆延迟”,APD矛盾性的延长,而另一些细胞则表现为动作电位穹隆完全消失,APD显著缩短。这种复极的时间和空间差异形成了一个陡峭的梯度,成为2相折返的基质。
一旦满足以上两个条件,2相折返即可发生,产生短偶联间期室早,可引发多形性室速或室颤 ,如图7A、B所示。
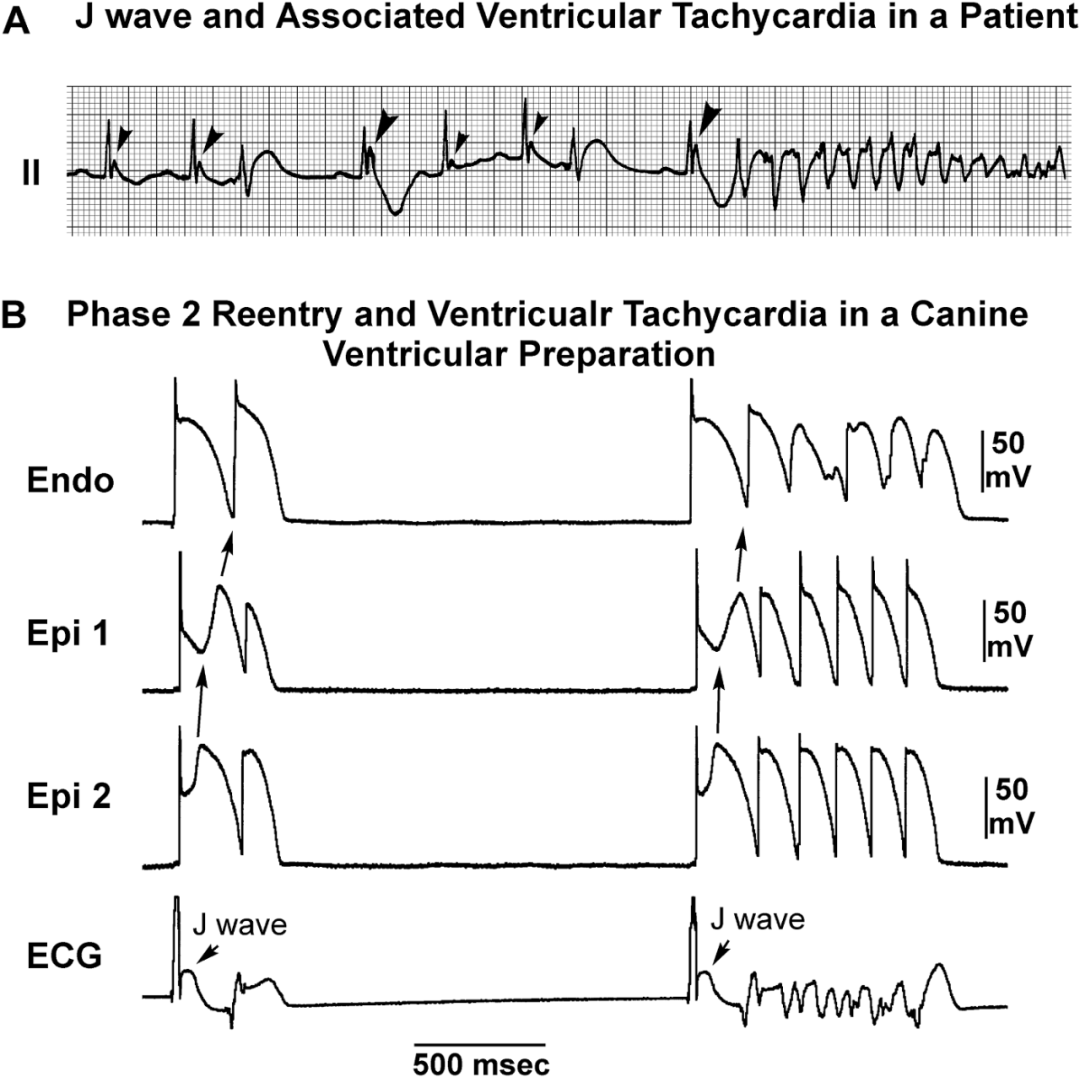 图7. J波相关心律失常发生机制。(A) 一名具有显著J波的患者出现多形性室性心动过速。注意长间歇依赖的J波增大及更明显的负向T波(箭头所示),随后出现短偶联间期早搏,引发多形性室性心动过速。(B) 在暴露于2.5 μmol/L吡那地尔(钾通道开放剂)的犬右心室楔形标本中,由2相折返引发的多形性室性心动过速。动作电位(AP)同时从两个心外膜位点(Epi1和Epi2)和一个心内膜位点(Endo)记录。Epi1中AP穹窿的缺失(而非Epi2)为2相折返创造了基质,触发多形性室性心动过速。AP,动作电位;VT,室性心动过速 (Gan-Xin Yan et al., Ventricular repolarization components on the electrocardiogram: Cellular basis and clinical significance, Journal of the American College of Cardiology, 42 (3), 2003, 401-409, https://doi.org/10.1016/S0735-1097(03)00713-7.)
图7. J波相关心律失常发生机制。(A) 一名具有显著J波的患者出现多形性室性心动过速。注意长间歇依赖的J波增大及更明显的负向T波(箭头所示),随后出现短偶联间期早搏,引发多形性室性心动过速。(B) 在暴露于2.5 μmol/L吡那地尔(钾通道开放剂)的犬右心室楔形标本中,由2相折返引发的多形性室性心动过速。动作电位(AP)同时从两个心外膜位点(Epi1和Epi2)和一个心内膜位点(Endo)记录。Epi1中AP穹窿的缺失(而非Epi2)为2相折返创造了基质,触发多形性室性心动过速。AP,动作电位;VT,室性心动过速 (Gan-Xin Yan et al., Ventricular repolarization components on the electrocardiogram: Cellular basis and clinical significance, Journal of the American College of Cardiology, 42 (3), 2003, 401-409, https://doi.org/10.1016/S0735-1097(03)00713-7.)
阻断Ito是J波综合征的独特治疗靶点
尽管多种离子通道基因突变与J波综合征有关,但心室心外膜细胞中显著Ito介导的动作电位切迹是所有类型J波综合征的先决条件,无论涉及的具体离子通道如何。这是因为显著Ito介导的AP切迹创造了一种条件,使得心外膜AP穹隆对复极电流平衡的改变变得高度敏感——无论是由于内向钠或钙电流减少,还是外向钾电流增加。以上机制解释了为什么奎尼丁,这种同时阻断Ito和INa的药物,成为抑制和预防J波综合征患者多形性室速的核心疗法。
一个典型的例子是一名45岁男性Brugada综合征患者,他经历了反复发作的室颤(VF)和ICD电击,应用奎尼丁成功抑制以上发作多年,但西洛他唑无效。由于有几天未拿到奎尼丁导致药物中断引发VF风暴。这呈现了奎尼丁治疗中典型的“开-关”现象(注:用则抑制,停则发作)。关于J波综合征中奎尼丁的临床剂量,Shinohara及其同事最近的一项临床研究表明,低剂量奎尼丁在有症状的Brugada综合征患者中是有效且安全的,与传统的高剂量方案相比,显著减少了心律失常事件,同时减少了不良反应。


抗心律失常药物通过选择性靶向(作用于)离子通道、改变动作电位动力学并延长不应期而发挥作用。虽然这类药物能有效抑制心律失常,但其使用依赖性和反向使用依赖性等机制也可能带来致心律失常风险。针对J波综合征等的最新研究揭示了靶向治疗的重要性。深入理解药物作用机制对于指导临床治疗、实现更安全、更个性化的心律失常管理至关重要。
1.折返机制是大多数心律失常的基础病理机制,其发生与传导速度减慢或ERP缩短有关。
2.治疗折返性心律失常的主要机制是延长ERP。IKr阻滞剂通过延长APD实现这一效果,而I类钠通道阻滞剂则通过减少可再兴奋钠通道数量来延长ERP。
3.纯IKr阻滞与反向使用依赖性相关,这会增加尖端扭转型室速的风险。Ic类钠通道阻滞剂表现出强烈的使用依赖性,可导致传导显著减慢,增加心律失常风险及心源性死亡率。
4.抑制晚钠电流可减轻QT间期延长和反向使用依赖性,无论病因如何,这对长QT综合征具有治疗价值。
5.同样地,阻断瞬时外向钾电流(Ito)(如奎尼丁)是J波综合征的关键治疗策略,无论是否存在潜在的离子通道突变。
审校:GXM
排版:GXM
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
