
来源:IBD Daily
克罗恩病 (Crohn’s disease, CD) 是一种累及全消化道、以全层炎症和反复缓解-复发为特征的慢性免疫介导性疾病。生物制剂 (尤其是英夫利西单抗,IFX) 显著改善了CD患者的症状控制与预后,但临床上仍有约10%–30%的患者在诱导期即出现原发无应答 (primary non-response, PNR),导致疾病控制延迟、用药调整增多,甚至增加不可逆肠损伤风险。因此,在治疗早期甚至治疗前识别高风险PNR人群,对实现 “精准用药” 和 “treat-to-target” 策略尤为关键。既往PNR预测多依赖单一生物标志物或单模态数据,且外部验证不足,泛化能力受限;影像组学与病理特征虽各有潜力,但单一维度难以完整刻画CD从微观黏膜炎症到宏观结构改变的复杂性。本研究因此提出将内镜活检病理学特征、CTE影像特征与临床指标进行多模态融合,构建深度学习预测模型,以提升IFX-PNR的可预测性与临床可转化性。
研究为双中心回顾性队列:中山大学附属第一医院 (2016年10月–2021年10月) 作为内部训练/验证队列,陆军军医大学陆军特色医学中心提供独立外部测试队列。纳入标准包括:成人CD患者接受IFX诱导治疗;起始治疗前1个月内完成结肠镜及CTE;并于治疗后第14周进行疗效评估等;排除合并肿瘤/感染性
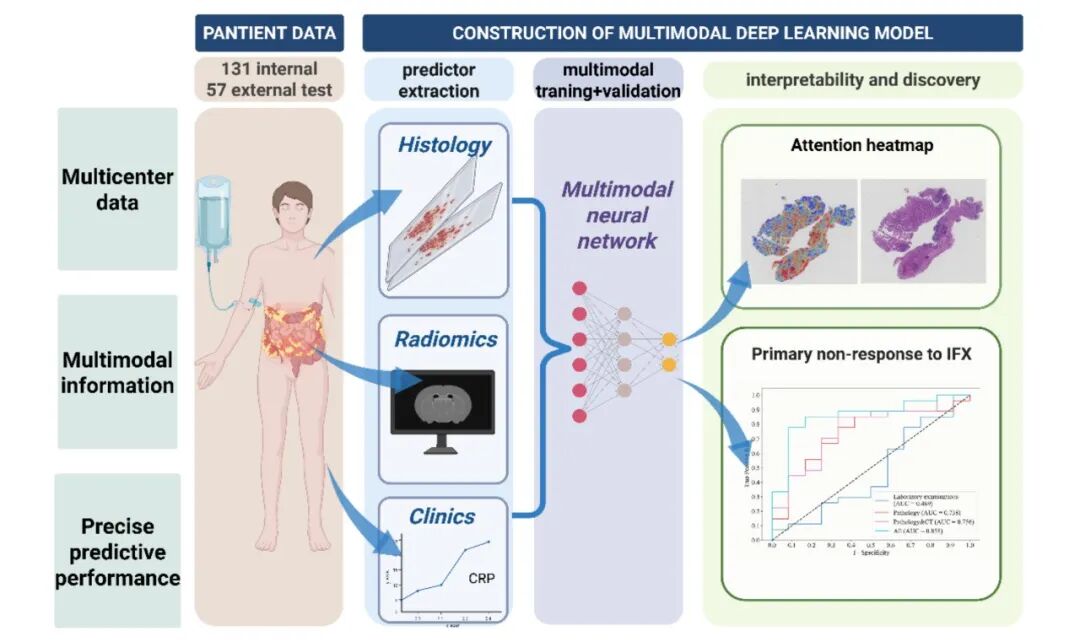
图1. 研究流程
多模态数据包括:(1) 临床与实验室:记录基线人口学、Montreal分型、CDAI、SES-CD、
模型采用 “三阶段融合” 框架:先对 WSI 的patch级嵌入进行聚类与基于聚类的多实例学习 (MIL) 池化得到患者级病理向量;CTE侧对病灶VOI提取患者级CT向量;随后通过跨模态序贯注意力进行病理—影像双模态融合,并将融合后的视觉表征与临床特征拼接,最终使用TabNet对关键共享特征进行选择并输出PNR预测。内部数据按7:3划分训练/验证,最终模型在外部独立队列进行验证,以AUC等指标评估性能。
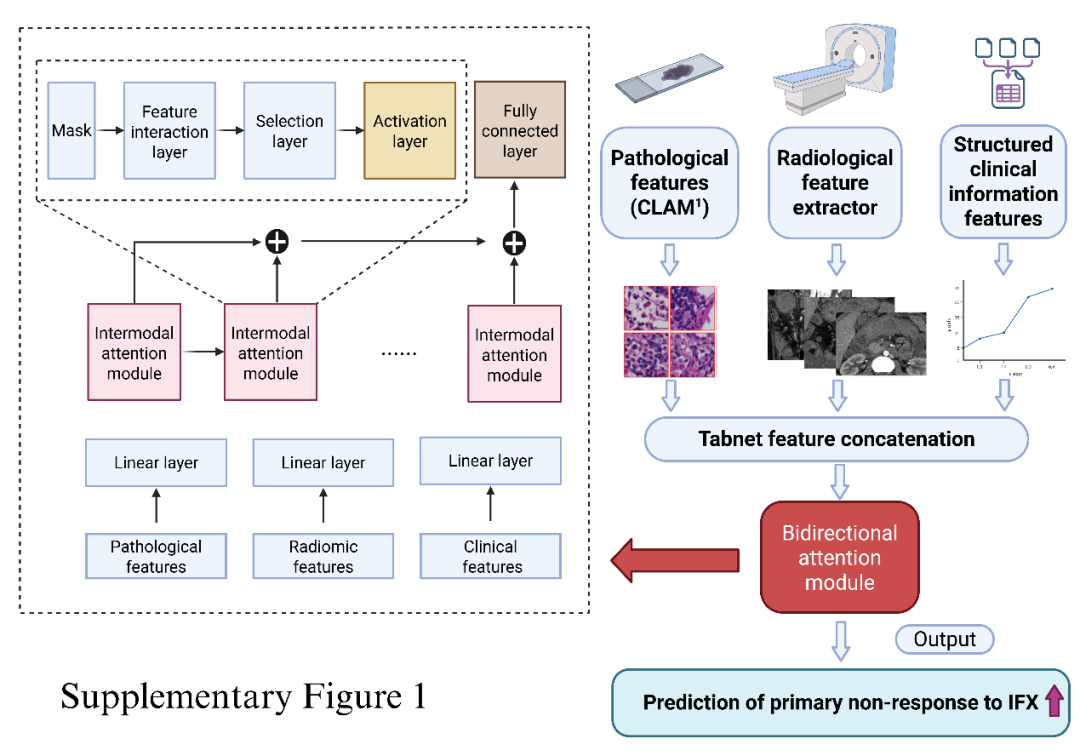
图2. 三阶段多模态特征融合框架
注:临床模型基于TabNet框架,而病理和CT影像的特征则通过带残差学习的卷积模块提取。基于聚类的多实例学习方法探索病理图像块之间的关系。在特征融合阶段,跨模态注意力模块对两种模态的共享特征进行对齐,随后通过交互融合过滤并整合相关特征,最终实现克罗恩病患者的疗效预测。CLAM (聚类约束注意力多实例学习):用于全切片图像分析的弱监督深度学习框架。
共纳入188例CD患者:内部训练集93例、内部验证集38例、外部测试集57例。多模态对比显示:仅用临床特征的TabNet模型预测能力有限,内部验证AUC为0.539、外部测试AUC为0.469;病理学特征的模型,内部验证AUC达0.789、外部测试AUC为0.738;病理+CTE双模态模型内部验证AUC为0.844、外部测试AUC为0.756;整合临床+病理+影像的最优多模态模型表现最佳,内部验证AUC为0.852,外部测试AUC为0.858,且在两队列中敏感度、特异度与准确度均达到可接受水平 (内部≥0.65,外部≥0.60),提示融合策略优于任何单模态模型并具有更好的泛化能力。
在可解释性方面,WSI热图提示模型主要关注重度炎症区域:以中性粒细胞浸润为主的活动性炎症、淋巴细胞聚集灶,以及隐窝结构异常等,这些区域可能反映持续的组织学活动度,与IFX诱导期疗效不佳存在关联线索。
本研究构建并外部验证了一个融合内镜活检病理全切片、CTE影像深度特征与临床指标的多模态深度学习模型,可较准确地预测CD患者IFX诱导期原发无应答风险。与仅依赖临床指标的模型相比,病理AI贡献了关键增益,而多模态融合进一步带来更稳健、可推广的预测表现。该工具有望在临床实践中用于治疗前/早期风险分层,辅助个体化选择与及时优化方案,从而提升疗效并改善长期结局。
致谢
中一毛仁教授&深圳大学黄炳升教授&陆军军医大学魏艳玲教授
团队供稿