
第67届美国血液学会(ASH)年会已于2025年12月6日至9日在佛罗里达州奥兰多市举办,本次会议汇聚全球血液学领域的顶尖专家与学者,共同探讨包括Castleman病在内的多种血液疾病的诊疗进展与未来方向。
Castleman病是一种罕见的血液系统疾病,曾经对患者的生存和生活带来了巨大挑战。近年来,Castleman病诊疗取得了里程碑式的进展,本次ASH年会中,来自中国等国家和地区的研究者报告了该领域多项最新进展,医脉通特别整理相关内容,并特邀北京协和医院李剑教授、张路教授进行解读,以飨读者。
迈向精准分层:中国研究探索iMCD精准治疗策略
特发性多中心型Castleman病(iMCD)具有高度异质性,主要分为iMCD-非特指型(iMCD-NOS)、iMCD-特发性浆细胞性淋巴结病(iMCD-IPL)和iMCD-TAFRO亚型1。如何根据iMCD不同的临床亚型进行更精细的风险分层和治疗策略调整,成为本次ASH年会上中国学者关注的焦点。一项来自北京协和医院和浙江大学第一附属医院合作的研究,挑战了“iMCD需无限期治疗”的传统观念,纳入了27例在停止治疗后仍维持缓解的iMCD-TAFRO患者。停药后中位随访31个月,结果显示高达85.2%(23例)的患者维持缓解且为生化完全缓解,其中20例为完全缓解(CR)(图1)。中位无进展生存期(PFS)未达到,估计6个月、1年及3年PFS率分别为96.3%、85.2%和85.2%。仅4例患者发生疾病进展,且疾病进展均发生在停药后1年内。截至末次随访日期,所有27例患者均存活。这一发现提示,一部分iMCD-TAFRO患者或可实现治愈而不需要“无限期”治疗,对于达到生化完全缓解的的iMCD-TAFRO患者,尝试停药是一个值得考虑的临床选项2。
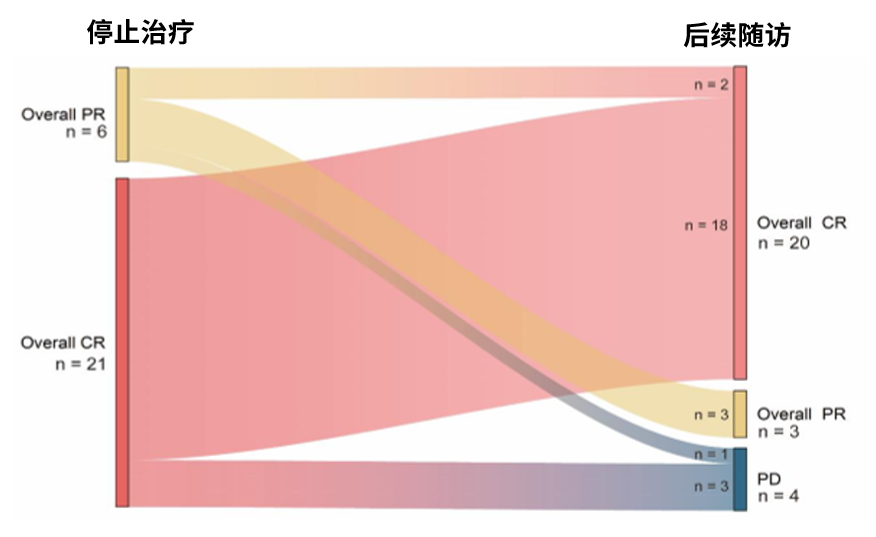
图1 停止治疗后iMCD-TAFRO患者疗效情况
另一项来自北京协和医院的回顾性研究纳入了2000年1月至2025年3月期间被诊断为iMCD-IPL和iMCD-NOS的患者。根据CDCN定义的严重程度标准,患者被分为四组:重型iMCD-IPL、非重型iMCD-IPL、重型iMCD-NOS和非重型iMCD-NOS。研究共纳入152例iMCD-IPL患者(重型37例,非重型115例)和186例iMCD-NOS患者(重型52例,非重型134例)。中位随访时间45.1个月,四组患者均未达到中位总生存期(OS)。进一步比较发现,重型iMCD-IPL与非重型iMCD-NOS患者的OS无显著差异(P=0.402)。然而,重型iMCD-NOS患者的预后相对较差,其OS显著低于重型iMCD-IPL(P=0.008)、非重型iMCD-IPL(P=0.001)以及非重型iMCD-NOS患者(P=0.002)(图2)1。
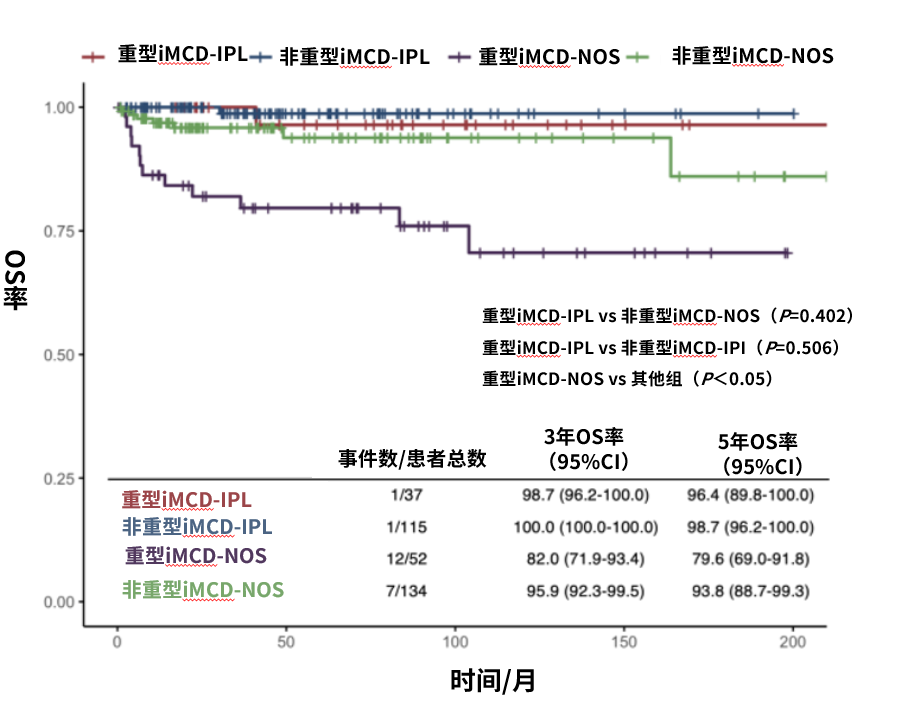
图2 重型iMCD-IPL、非重型iMCD-IPL、重型iMCD-NOS和非重型iMCD-NOS患者OS
在37例重型iMCD-IPL患者中,接受“针对重型的治疗方案”和“针对非重型治疗方案”两个治疗组之间的中位至下次治疗时间(TTNT)无显著差异(P=0.52)。该研究结果表明,当前CDCN基于严重程度的分层标准可能不足以准确反映iMCD-IPL亚型的预后特征。部分“重型”iMCD-IPL患者可能并非真正高危,且有可能从“非重型治疗方案”中获益1。
从有效治疗到全程管理:CRP动态监测为实现精准诊疗提供“导航”
为系统评估CRP在司妥昔单抗治疗过程中的动态演变及其与疗效的关系,一项研究纳入了69例接受司妥昔单抗治疗且具备基线与治疗后CRP数据的患者3。通过对CRP水平随时间变化的定性分析,观察到所有患者从基线到第1周期治疗后均出现了由司妥昔单抗介导的CRP水平降低。而在2周期后,仅CR患者的CRP完全且持续降低(图3)。研究结果提示:尽管早期CRP下降普遍存在,但其变化幅度并不能预测最终疗效;而持续维持低水平CRP,则与持续CR密切相关,提示CRP反弹或下降不充分可能意味着治疗失败风险升高3。
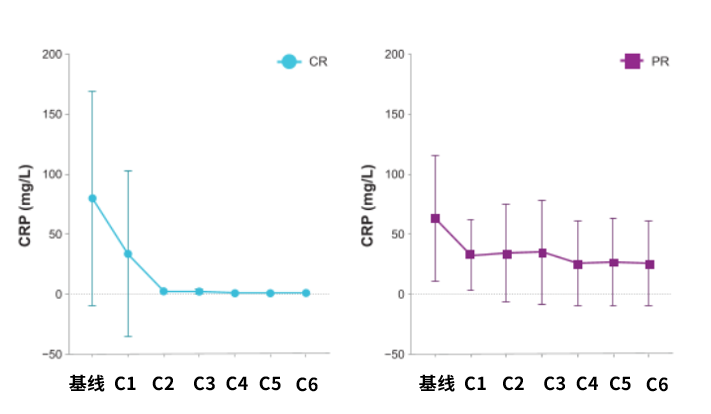
图3 从基线到C6不同疗效的CRP水平变化情况(左:CR,右:PR)
综上所述,该研究强调了对iMCD患者进行CRP动态监测在全程管理中的重要价值,凸显了CRP、时间与临床反应之间的动态关系,提示持续抑制IL‑6通路并维持低CRP水平是iMCD疾病有效控制的关键标志。
直面iMCD疾病挑战,司妥昔单抗在儿童中展现良好疗效与安全性
尽管iMCD治疗在成人中已有一定研究基础,但由于儿童发病率极低,其临床表现、病理机制及治疗策略仍认知有限。今年ASH年会中公布的一项基于ACCELERATE注册登记研究的首次大规模系统性分析对比了儿童(发病年龄<19岁,n=30)与成人(n=96)iMCD患者的临床特征与治疗结局4。治疗方面,最常使用的方案是司妥昔单抗±激素,分别有14例儿童和55例成人iMCD患者接受该类方案。在可评估疗效的儿童患者中,司妥昔单抗治疗组的临床应答率达86%,与成人患者的73%相当(P=0.48)。更值得注意的是,在儿童中观察到64%的患者实现了持久缓解,优于成人组的49%(P=0.50),显示出司妥昔单抗在儿童iMCD患者中具有良好且持久的疗效。在其它治疗方案中,儿童和成人iMCD患者的临床应答率相似,无显著差异(图4)。在安全性方面,司妥昔单抗在儿童iMCD患者中的安全性良好,与成人患者相当。
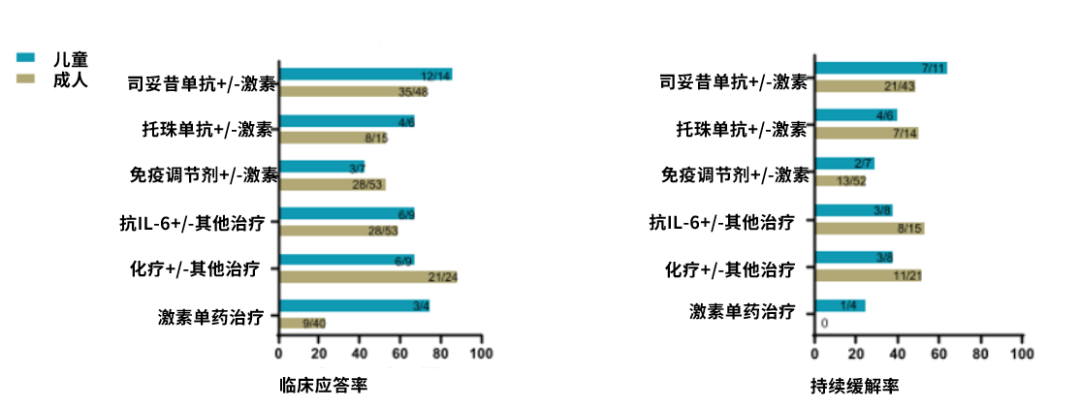
图4 儿童与成人iMCD患者临床应答与持续缓解率相当
作为迄今规模最大的儿童iMCD队列分析,本研究中观察到司妥昔单抗在儿童iMCD中的高应答率与持久缓解,为其在儿童iMCD的应用提供了有力的循证支持。研究结果进一步巩固了司妥昔单抗作为iMCD一线治疗的核心地位,并为儿童患者的临床管理提供了参考。

张路教授
iMCD作为一种罕见的血液系统疾病,其诊断与治疗始终存在挑战。随着司妥昔单抗在国内的可及性提高,尤其是进入医保后,更多患者得以接受这一治疗,生存预后与生活质量获得了切实改善。虽然司妥昔单抗说明书中提示“尚未确立在17岁或以下儿童中的安全性和有效性”,但本次ASH大会上,美国宾大研究团队基于ACCELERATE注册登记研究的数据,也体现了司妥昔单抗在儿童患者中的应用前景。除了前述宾大研究团队的工作外,我中心公布的两项研究为不同临床类型iMCD的临床实践提供了新的思路。首先,关于iMCD-TAFRO停药可能性的研究,我们秉持着以患者为中心的治疗理念,对“需要无限期治疗”的传统观念提出了挑战。我们的研究表明,对于达到生化完全缓解的患者,尝试停药是一个值得考虑的临床选项,这不仅为治疗策略提供了更灵活的选择,也有望减轻患者的长期治疗负担,从而进一步提升其生活质量。不过临床中的确仍有部分iMCD-TAFRO患者停药后会面临疾病复发。前述策略还有待进一步验证。其次,关于iMCD-IPL亚型的研究提示,基于疾病亚型的精准分层,可能比单纯的“重型/非重型”分类更能准确反映患者预后与治疗需求。这有助于避免部分患者的过度治疗,推动诊疗策略向更精准的方向发展。这两项研究反映了中国学者在Castleman病精准治疗领域的持续探索,该成果对于未来制定个体化的治疗与管理方案具有积极的参考价值。

李剑教授
iMCD作为一种具有特征性病理改变和高度临床异质性的血液系统罕见疾病,临床特征包括全身多发淋巴结肿大、全身炎症症状、多克隆淋巴增生和多器官功能障碍,IL-6在其发病中发挥关键作用,此类患者病情重,预后差5-6。作为iMCD标准一线治疗方案,司妥昔单抗通过靶向中和IL-6而使iMCD获得缓解。目前,多项高质量循证医学证据已充分验证了司妥昔单抗在iMCD治疗中的疗效与安全性,确立了其作为一线首选治疗方案的重要地位5。当前,iMCD的诊疗模式正逐步从寻求有效治疗阶段,迈入以精准监测为导向的全程化管理。本届ASH年会上中国研究者的最新研究进一步深化了这一理念:通过揭示iMCD-TAFRO患者停药可能性,以及对iMCD-IPL亚型所需治疗强度的重新定义,有力推动了iMCD治疗从“统一框架”向精准分层策略演进。在此过程中,结合CRP动态监测的诊疗策略,为推动iMCD的个体化、全程化精准管理提供了可靠路径。此外,司妥昔单抗在儿童这一高危iMCD人群中也展现出持久缓解潜力,展现了其更广泛的、全年龄段应用潜力。未来,随着更多真实世界数据与生物学标志物研究的积累,iMCD患者的长期生存与生活质量有望实现进一步改善。

张路 教授
北京协和医院 血液科 副主任
主任医师,硕士生导师
北京协和医院首届“杰出青年”
中华医学会血液学分会罕见病学组委员
以第一或通讯作者身份在Blood,Chest,Blood Adv,AJH,Lancet Reg Health West Pac,BJHaem等杂志发表论文
主持包括国自然在内的多项科研基金

李剑 教授
北京协和医院血液内科主任, 主任医师, 博士生导师
中华医学会血液学分会常委
北京医学会血液学分会副主任委员
北京医师协会血液科医师分会副会长
中华医学会血液学分会罕见病学组组长
中华血液学杂志编委
参考文献:
1.Siyuan Li, et al. Is ‘severe’ imcd-IPL really sever e? 2025 ASH. abs25-7949.
2.Lu Zhang, et al. Idiopathic multicentric castleman disease - tafro: A potentially curable disease? 2025 ASH. abs25-12454.
3.Jean-Francois Rossi, et al. Siltuximab-mediated suppression of CRP is associated with clinical response in idiopathic multicentric castleman disease. 2025 ASH. abs25-13203.
4.Bridget Austin,et al. Pediatric idiopathic multicentric castleman disease is often severe and responds to siltuximab. 2025 ASH. abs25-11167.
5.中国临床肿瘤学会(CSCO)淋巴瘤专家委员会. 司妥昔单抗中国专家推荐临床应用指导原则(2024年版) [J] . 白血病·淋巴瘤, 2024, 33(8) : 449-455.
6.Zhang L, Dong YJ, Peng HL, et al. A national, multicenter, retrospective study of Castleman disease in China implementing CDCN criteria[J]. Lancet Reg Health West Pac, 2023, 34:100720.

戳“阅读原文”,查看更多内容
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)