来源:IBD Daily
肠道纤维化是克罗恩病(CD)导致手术的重要原因之一,表现为肠壁肌层增厚、胶原沉积及狭窄形成,且在抗炎治疗后仍可持续进展。由于缺乏可逆转或延缓纤维化的特异性药物,明确驱动纤维化启动与放大的关键分子及可干预的靶点,对降低狭窄/手术风险具有重要意义。
随着肠道微生物组学和代谢组学的快速发展,肠道菌群在 CD 发生与进展中的作用日益受到关注。肠道菌群可通过多种生物活性成分,包括脂多糖、短链脂肪酸、次级胆汁酸、细菌蛋白及毒素等,直接或间接影响肠上皮屏障功能并调控宿主免疫反应。近年来的研究提示肠道菌群不仅参与炎症反应,还可能在 CD 相关肠道狭窄和纤维化的形成中发挥重要作用,但其具体分子机制仍有待系统解析。
二肽基肽酶4(DPP4)既可作为膜结合型蛋白参与细胞间信号与细胞外基质调控,也可形成可溶性形式(sDPP4)在组织微环境中发挥酶学及免疫调节作用。既往研究提示DPP4与多个器官纤维化相关,但其在 CD 相关肠道纤维化中的作用,尤其是其不同来源DPP4(宿主与肠道菌群)在病理机制中的作用,仍有待阐明。
该研究围绕“DPP4驱动CD肠道纤维化”的核心科学问题,提出并验证“双来源DPP4(宿主+微生物)协同促进纤维化”的新概念,从临床证据、机制靶点到药物联合干预进行了研究,为CD狭窄的抗纤维化治疗提供潜在的靶点。
该研究整合临床队列、多组学数据及体内外模型,对宿主和微生物来源的DPP4 在克罗恩病肠道纤维化中的作用进行了系统研究。在临床层面,分析狭窄与非狭窄 CD 患者肠组织样本中 DPP4 的细胞定位和表达特征,评估宿主来源DPP4 与疾病表型的关联。在机制层面,基于人源肠道肌成纤维细胞,评估宿主与微生物来源 DPP4 对成纤维细胞活化及胶原沉积的影响,并解析相关信号通路。在微生物层面,结合宏基因组测序与工程菌体内实验,验证菌源 DPP4 在慢性
1.DPP4在狭窄型CD纤维化病灶显著上调
为筛选与 CD 肠道狭窄相关的关键分子,首先对公开 GEO 数据集进行分析,比较狭窄型与非狭窄型 CD 肠组织的转录组特征,结果显示,DPP4 在差异分析与PPI网络分析中被鉴定为与纤维化重塑显著相关的枢纽基因之一(图1A-C)。随后,通过对 CD 患者肠道狭窄组织、非狭窄炎症组织及健康对照组织进行免疫组化染色联合马松染色,结果显示,DPP4 的表达主要集中于纤维化显著的基质区域,并与胶原沉积区域高度重叠(图 1G-H)。这些结果提示 DPP4 可能在 CD 肠道纤维化过程中发挥重要作用。
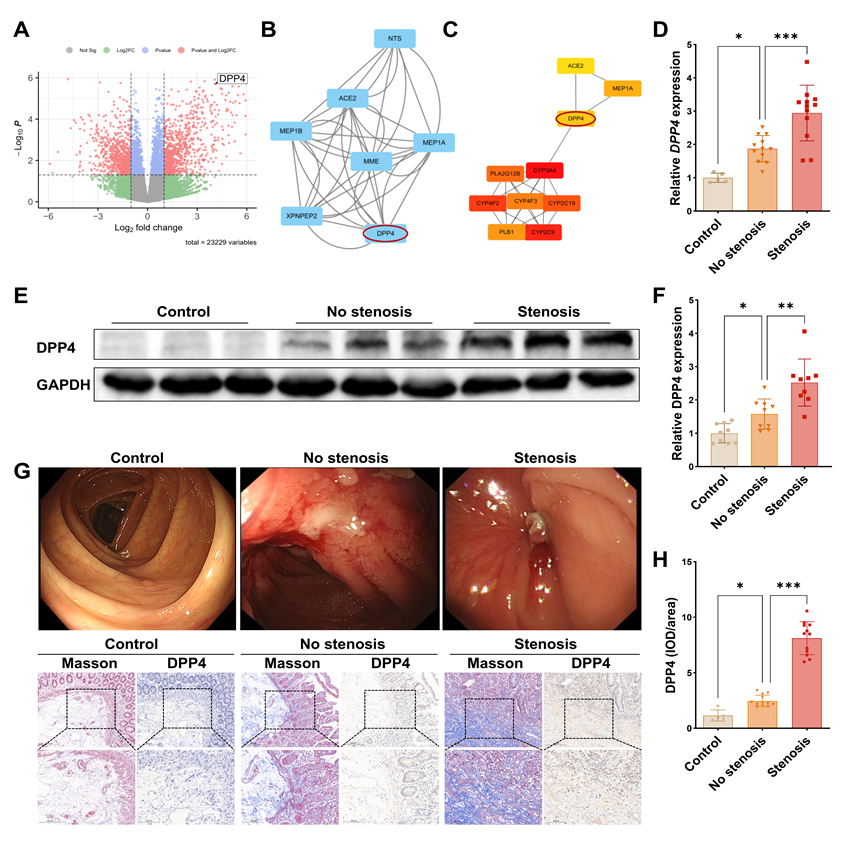
图1:DPP4在狭窄型CD纤维化病灶显著上调
2. DPP4 在慢性结肠炎模型中促进肠道纤维化形成
为进一步验证 DPP4 在肠道纤维化中的功能作用,采用葡聚糖硫酸钠(DSS)诱导的慢性结肠炎模型模拟 CD 相关纤维化过程。该模型通过多轮 DSS 处理与恢复期交替进行,可在炎症基础上形成稳定的肠道纤维化表型。在该模型中,DPP4 的表达水平随纤维化进展而显著升高。无论在免疫组织化学还是蛋白检测中,DPP4 均主要分布于纤维化相关的间质区域,并与胶原沉积区域高度重叠。这一结果提示,DPP4 的上调并非单纯炎症伴随现象,而可能直接参与肠道纤维化的形成过程(图2A-H)。进一步研究者在慢性 DSS 模型后期给予 DPP4 抑制剂
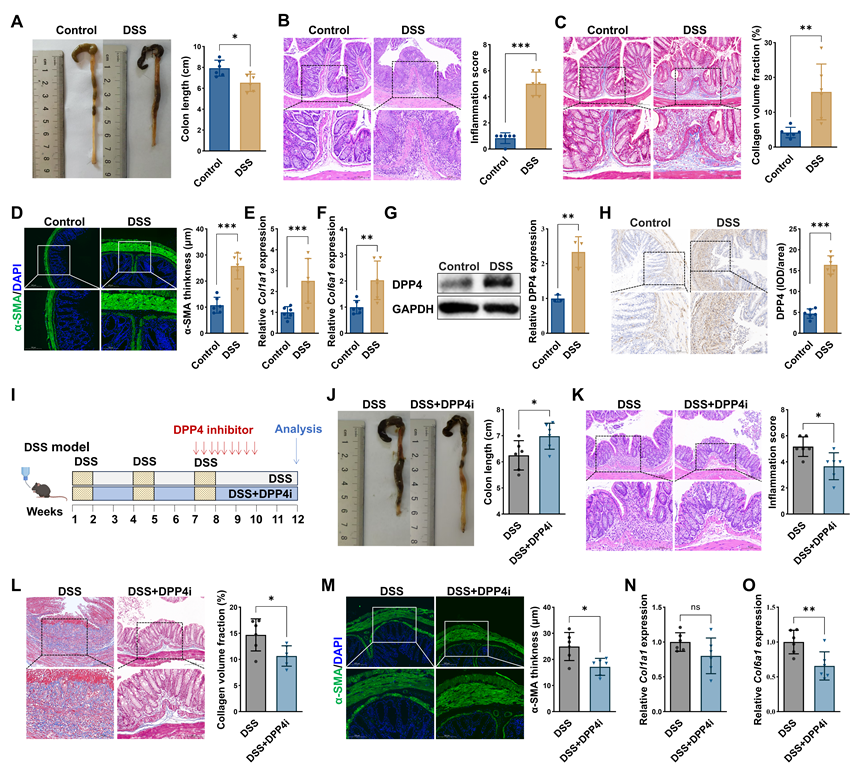
图2:DPP4 在慢性结肠炎模型中促进肠道纤维化形成
3. 成纤维细胞中膜结合型 DPP4 促进肌成纤维细胞活化与迁移
为明确 DPP4 在肠道组织中的主要来源,研究者对 CD 患者肠道组织进行了多重免疫组织化学染色,结果显示,DPP4 信号主要与 CD90⁺ 成纤维细胞共定位,而与 CD3⁺ T 细胞或 EpCAM⁺ 上皮细胞的重叠极少(图3A)。转录组数据分析同样证实,与非狭窄组织相比,来源于狭窄组织的成纤维细胞中 DPP4 mRNA 表达水平显著升高(图3B)。分离培养人源肠道肌成纤维细胞(HIMFs),通过 TGF-β 诱导其活化,在此基础上,药物抑制 DPP4 后HIMFs 的迁移能力明显下降,α-SMA 及胶原相关基因表达受到显著抑制(图3D-H)。这些结果表明,膜结合型 DPP4 在成纤维细胞中具有细胞自主性促纤维化作用,可直接促进成纤维细胞向肌成纤维细胞表型转变,并增强其迁移能力,从而促进肠道纤维化进程。
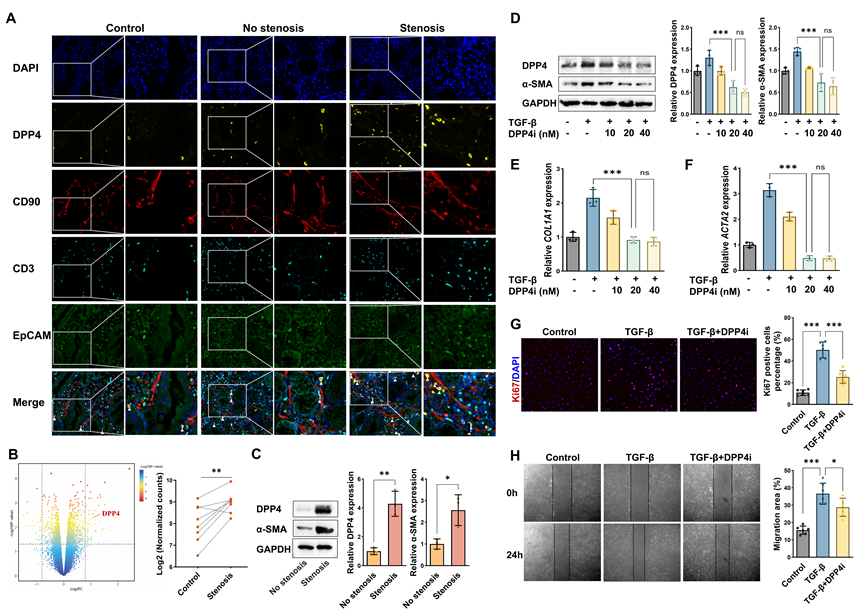
图3:成纤维细胞中膜结合型 DPP4 促进肌成纤维细胞活化与迁移
4. 可溶性 DPP4 促进肠道肌成纤维细胞增殖与迁移
除膜结合型 DPP4 外,该研究进一步关注可溶性 DPP4(sDPP4)在 CD 相关纤维化中的作用。与健康对照相比,CD 患者血浆 sDPP4 水平升高,且在狭窄型 CD 患者中最为显著(图4A)。体外实验中,研究者采用不同浓度的重组 sDPP4 刺激 HIMFs,结果显示,sDPP4 可呈剂量依赖性地上调 COL1A1 和 ACTA2 等纤维化相关基因的表达,并显著提高 α-SMA 蛋白水平。与此同时,sDPP4 明显促进 HIMFs 的增殖和迁移,而 DPP4 抑制剂可有效逆转上述效应(图4B-F)。以上结果提示,可溶性 DPP4 与膜结合型 DPP4 在功能上具有协同作用,二者可能共同放大成纤维细胞的促纤维化反应,从而加速肠道纤维化形成。
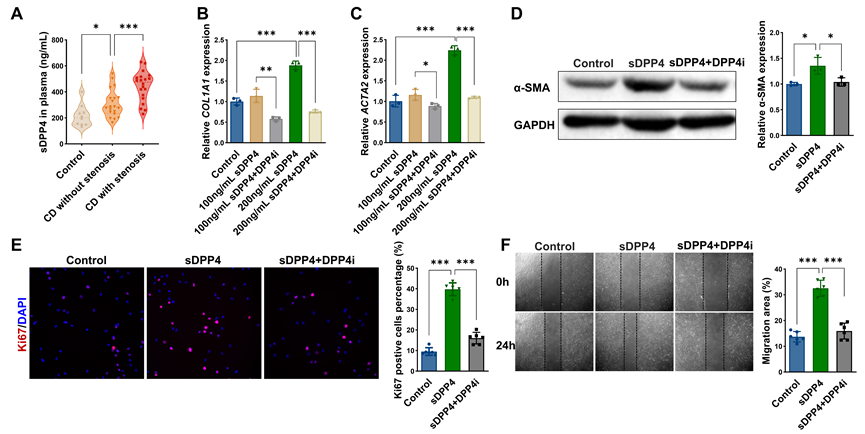
图4:可溶性 DPP4 促进肠道肌成纤维细胞增殖与迁移
5. DPP4 通过 PI3K-AKT 信号通路驱动肠道肌成纤维细胞活化
为阐明 DPP4 介导成纤维细胞活化的分子机制,基于已发表的 CD 合并狭窄肠道组织单细胞 RNA 测序数据进行分析发现,与 DPP4⁻ 成纤维细胞相比,DPP4⁺ 成纤维细胞中与纤维化相关的信号通路显著富集,其中既包括经典的 TGF-β 信号通路,也包括非经典的 PI3K-AKT 信号通路。进一步在体外模型中验证 DPP4 下游信号通路的激活情况,结果表明,DPP4可显著增强 PI3K 和 AKT 的磷酸化水平,并同步上调 α-SMA 蛋白表达(图5)。上述结果表明,PI3K-AKT 信号通路是 DPP4 介导肠道肌成纤维细胞活化的主要下游通路。
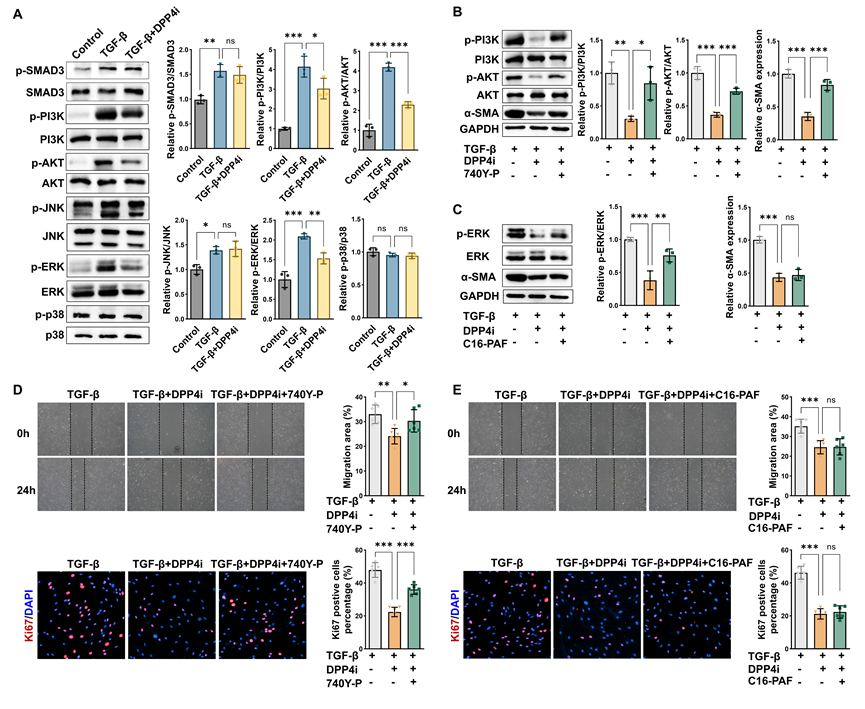
图5:DPP4 通过 PI3K-AKT 信号通路驱动肠道肌成纤维细胞活化
6. 肠道菌群来源 DPP4 在狭窄型克罗恩病患者中显著富集,参与促进肠道纤维化形成
鉴于 DPP4 为分泌型酶,且其活性可受局部炎症和代谢环境调控,该研究进一步探讨肠道菌群是否也是 DPP4 的重要来源。宏基因组测序结果显示,与非狭窄型 CD 患者相比,狭窄型 CD 患者粪便样本中编码 Dpp4 的微生物基因显著富集(图6A-D)。由于Bacteroides 属对Dpp4基因丰度的贡献度较高,研究者合成了Bacteroides来源的DPP4重组蛋白(btDPP4),在体外模型中刺激HIMFs,结果显示,微生物来源 DPP4 可呈剂量依赖性地诱导 α-SMA 表达升高(图6H-L),并显著增强 PI3K 和 AKT 的磷酸化水平。使用选择性菌源 DPP4 抑制剂 Dau-d4 后,上述促纤维化效应明显减弱。
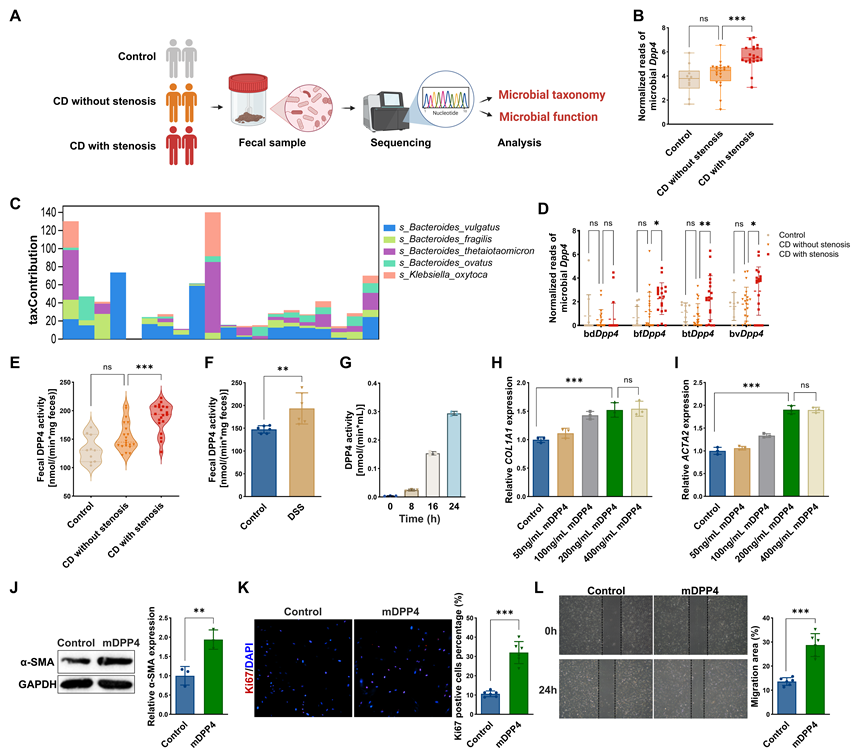
图6:肠道菌群来源 DPP4 在狭窄型克罗恩病患者中显著富集,参与促进肠道纤维化形成
在体内实验中,研究者构建并在小鼠肠道定植过表达菌源DPP4 的工程菌。与对照组相比,定植过表达菌源DPP4工程菌的小鼠在慢性 DSS 诱导模型中表现出更显著的胶原沉积、α-SMA 阳性区域增厚及整体纤维化评分升高(图7)。
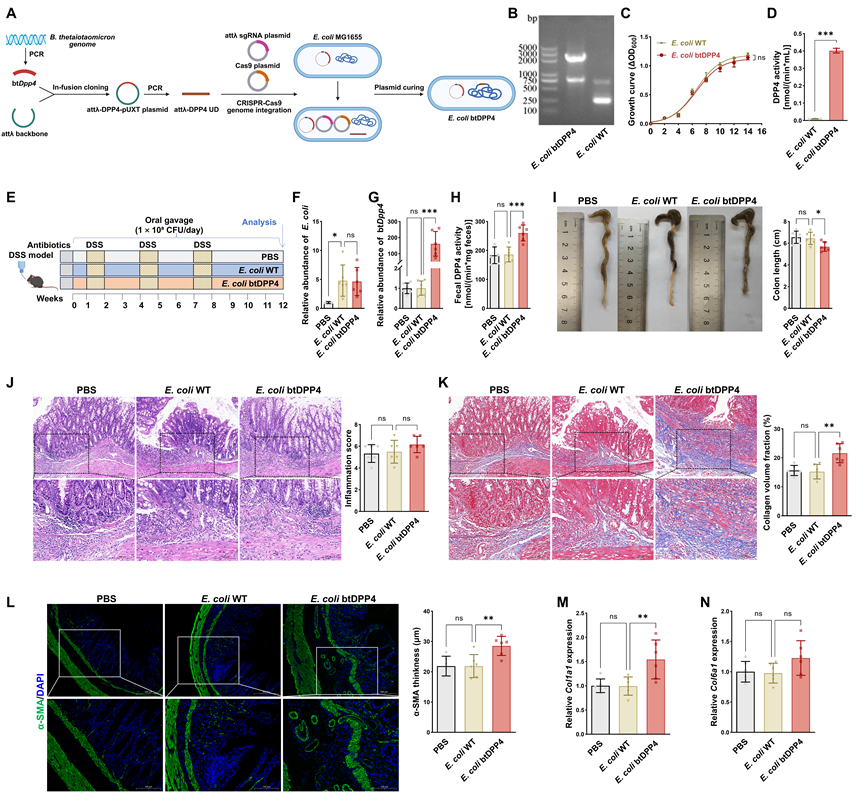
图7:定植过表达菌源DPP4工程菌的小鼠慢性肠炎纤维化程度更高
以上结果从体内外两个层面直接证明,微生物来源 DPP4 本身具有促纤维化致病活性,而非仅作为炎症或菌群失衡的伴随现象存在。
7. 联合抑制宿主与菌源 DPP4 可协同缓解肠道纤维化
在明确宿主与微生物来源 DPP4 均参与肠道纤维化形成后,该研究进一步评估二者联合干预的治疗潜力。在慢性 DSS 模型后期,研究者分别给予宿主 DPP4 抑制剂西格列汀、微生物 DPP4 抑制剂 Dau-d4,或二者联合治疗,结果显示,单独应用任一抑制剂均可在一定程度上减轻肠道纤维化表现,包括结肠长度部分恢复、胶原沉积减少及 α-SMA 表达下降。然而,联合用药组在上述多个指标上均表现出更显著的改善效果,纤维化相关基因(如 Col1a1、Col6a1)的抑制程度亦明显优于单药治疗(图8)。
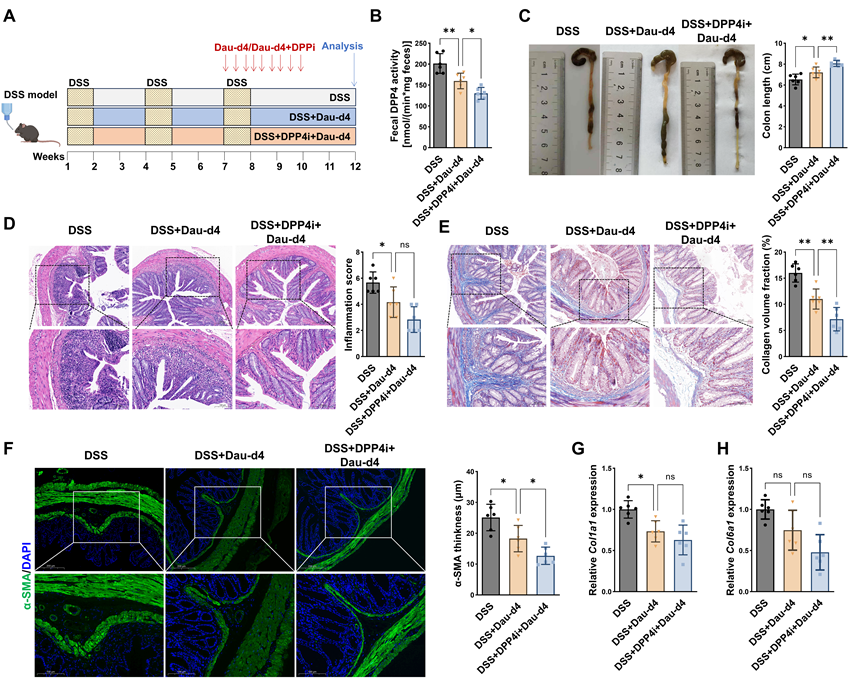
图8:联合抑制宿主与菌源 DPP4 可协同缓解肠道纤维化
该研究首次提出并验证了克罗恩病肠道纤维化的一个多因素调控模型,其中宿主来源(膜结合型与可溶性)及肠道菌群来源的 DPP4 协同驱动成纤维细胞活化、ECM 重塑及肠道狭窄形成。上述发现丰富了 DPP4 在炎症相关组织重塑中的功能认识,并为其作为抗纤维化干预靶点提供了依据。未来有必要在患者来源类器官模型及临床研究中进一步验证 DPP4 靶向干预的转化潜力。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)