肾脏纤维化以细胞外基质(ECM)过度积聚为特征,是各类
近期,南方医科大学南方医院刘友华教授、

核心发现
本研究通过对假手术(Sham)和单侧缺血再灌注损伤10天(UIRI 10D)的小鼠,进行单细胞转录组(scRNA-seq)与空间转录组(ST)联合数据分析,发现了一个富含TNC、兼具促炎与促纤维化特性的特殊微环境,该微环境通过激活巨噬细胞,驱动肾脏炎症与纤维化进程。实验证实,富含TNC的脱细胞肾组织支架及外源性TNC蛋白均可通过Toll样受体4(TLR4)/NF-κB信号通路激活骨髓来源巨噬细胞;而采用TLR4信号通路抑制剂或其基因敲除手段,则可通过抑制巨噬细胞活化有效缓解肾脏炎症与纤维化。移植TLR4缺陷型供体骨髓的嵌合小鼠模型显示出对肾脏炎症与纤维化的显著抵抗能力。本研究揭示:TNC通过激活TLR4/NF-κB信号通路驱动巨噬细胞,进而协同构建促炎-促纤维化微环境,最终加速肾脏纤维化进程。该发现深刻阐释了成纤维细胞、细胞外微环境与巨噬细胞三者间复杂互作推动肾脏纤维化发展的核心机制。
1. 纤维化肾脏空间特征的系统性解析
为在空间维度解析这些细胞群体的分布特征,研究整合运用了10x Genomics Visium空间转录组技术和超高分辨率Visium HD空间转录组测序。比较Sham组与UIRI 10D组小鼠的肾脏细胞组成及分子特征,发现纤维化肾脏中损伤的肾小管上皮细胞、免疫浸润细胞及成纤维细胞显著增加。进一步分析Sham组小鼠与UIRI 10D组小鼠肾脏的皮质-髓质分区结构,发现UIRI 10D肾脏的皮质区呈现显著的损伤相关小管富集,最显著的重塑发生于皮质-髓质交界区。此处原有的正常肾小管结构被活化的成纤维细胞与巨噬细胞浸润所替代,形成了两个界限清晰的纤维化微环境(Niche1和Niche2),其中Niche2表现出特化的成纤维细胞-巨噬细胞/单核细胞空间共定位特征。(图1)。
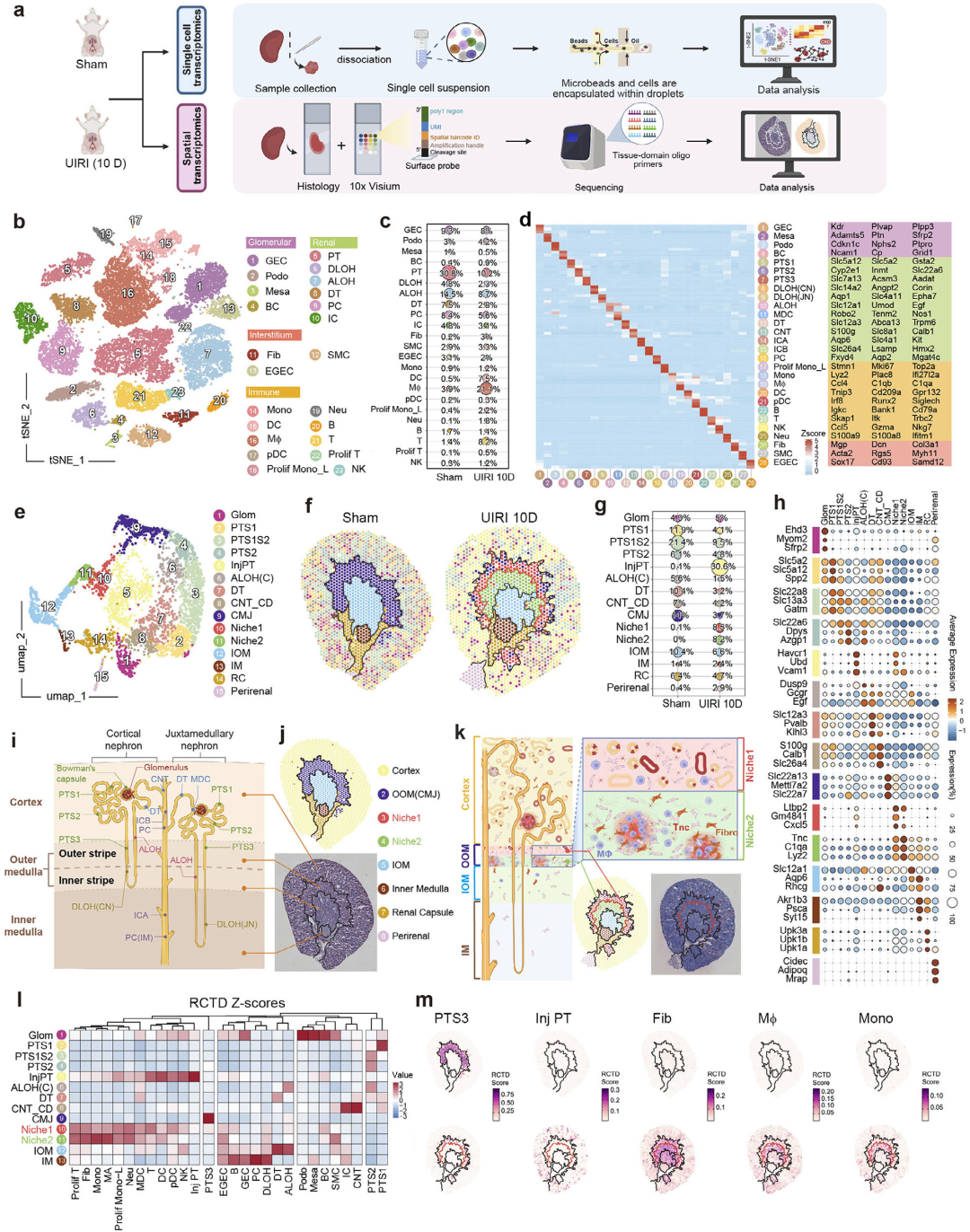
图1. UIRI后健康与纤维化肾脏的单细胞及空间转录组图谱
a)Sham组与UIRI 10天小鼠肾脏scRNA-seq及ST分析示意图。
b)展示纤维化肾脏复杂细胞多样性的t-SNE图,图中明确标注了肾小球内皮细胞(GEC)、足细胞(Podo)、系膜细胞(Mesa)、鲍曼氏囊上皮细胞(BC)、近端小管(PT)、亨利袢降支(DLOH)、亨利袢升支(ALOH)、远端小管(DT)、主细胞(PC)、闰细胞(IC)、成纤维细胞(Fib)、平滑肌细胞(SMC)、肾小球外内皮细胞(EGEC)、单核细胞(Mono)、树突状细胞(DC)、巨噬细胞(Mϕ)、浆样树突状细胞(pDC)、增殖性单核系细胞(Prolif mono_L)、中性粒细胞(Neu)、B细胞(B)、T细胞(T)、增殖性T细胞(prolif T)和自然杀伤细胞(NK)。这些细胞类型按颜色分组进一步归类为四大区室:肾小球区、肾小管区、间质区和免疫细胞区。
c)Sham与UIRI组主要肾脏细胞类型相对比例的气泡图。每个圆点代表特定细胞类型在样本组中的比例,点大小对应其相对占比。
d)主要肾细胞类型特征标志基因表达的综合热图.
e)基于Sham与UIRI 10D小鼠肾脏整合空间转录组数据生成的UMAP图,显示推断的肾细胞区域分布已识别的区域包括肾小球细胞(Glom)、近端小管不同区段(PTS1、PTS1S2、PTS2)、损伤近端小管(InjPT)、皮质区亨利袢升支(ALOH(C))、远端小管(DT)、连接小管与集合管(CNT_CD)、皮质髓质交界区细胞(CMJ)、纤维化微环境区域(Niche1、Niche2)、外髓内带(IOM)、内髓(IM)、肾被膜(RC)及肾周组织(Perirenal)。
f)Sham与UIRI 10D小鼠肾脏中肾细胞区域解剖分布的空间图谱。区域颜色与面板(e)中定义的分类一致。
g)Sham与UIRI 10D小鼠空间转录组数据中主要肾细胞区域相对比例的气泡图。
h)空间转录组数据中各肾细胞区域标志基因表达模式的气泡图。点颜色表示各区域内基因的平均表达水平,点大小代表表达该基因的空间点比例。
i)基于细胞类型的肾单位分段示意图。
j)肾脏解剖区域与空间转录组聚类对比,显示肾脏组织聚类(上图)及相应的Visium H&E染色切片(下图)。
k)UIRI样本中皮质0髓质交界区肾组织结构改变,显示两个不同的纤维化微环境Niche1和Niche2的形成。
l)热图显示通过RCTD方法获得的Visium空间转录组数据中各区域细胞类型组成的反卷积得分。
Sham组(上图)与UIRI组(下图)中基于RCTD的细胞类型得分空间特征图。2. 高分辨率空间转录组学揭示纤维化微环境的分子特征
通过空间转录组数据的非负矩阵分解(NMF),识别出具有空间变异特征的基因模块:因子8(胶原相关基因,广泛分布于成纤维细胞浸润区)与因子10/11(特异性富集于纤维化微环境)。因子11反映巨噬细胞特异性基因,而TNC作为因子10的核心组分,与成纤维细胞-巨噬细胞微呈现显著共定位。单细胞谱系溯源分析证实,TNC主要由活化的成纤维细胞表达和分泌,其空间表达严格局限于皮质-髓质交界处的成纤维细胞-巨噬细胞聚集区。证实成纤维细胞通过定位分泌TNC,为纤维化微环境搭建了分子框架(图2)。
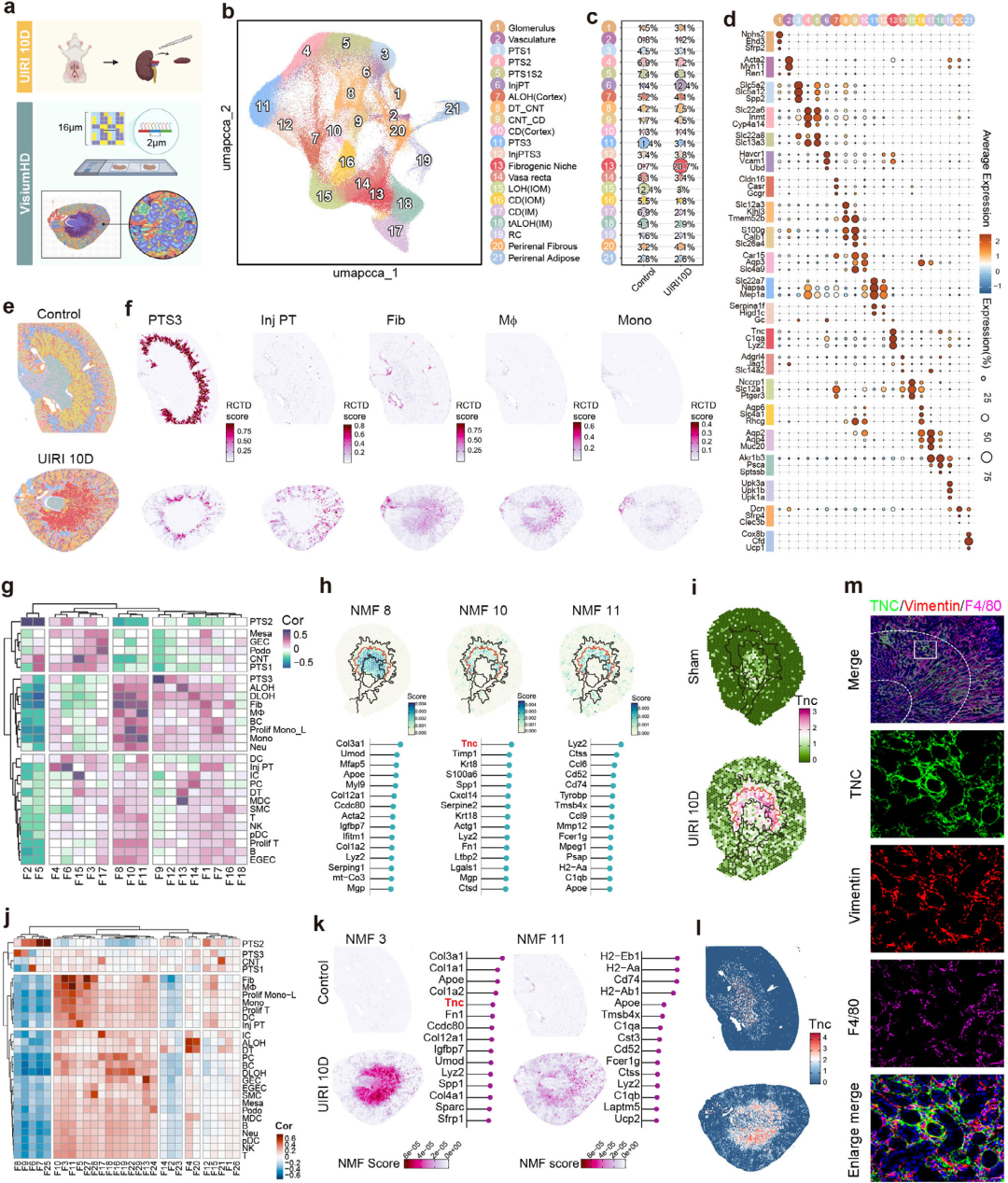
图2. 高分辨率空间转录组学与免疫染色揭示纤维化肾脏中TNC富集的成纤维细胞-巨噬细胞微环境结构
a)Visium HD技术应用于Sham和UIRI模型小鼠肾脏的工作流程示意图。
b)对照组与UIRI组(本研究)Visium HD空间转录组数据的UMAP可视化此降维可视化展示了代表不同肾实质与基质细胞群的特征聚类,包括:肾小球、血管系统、近端小管S1段(PTS1)、S2段(PTS2)、S1/S2过渡段(PTS1S2)、损伤近端小管(InjPT)、皮质亨利袢升支[ALOH(Cortex)]、远端小管与连接小管(DT_CNT)、连接小管与集合管(CNT_CD)、皮质集合管[CD(Cortex)]、近端小管S3段(PTS3)、损伤S3段(InjPTS3)、纤维化微环境、直小血管、外髓内带亨利袢[LOH(IOM)]、外髓集合管[CD(IOM)]、内髓集合管[CD(IM)]、内髓亨利袢薄壁升支[tALOH(IM)]、肾被膜(RC)、肾周纤维组织及肾周脂肪组织。c) 对照组与UIRI 10天组肾脏区域分布对比气泡图(Visium HD数据)。
d) Visium HD数据中不同肾细胞区域标志基因表达模式气泡图。
e) 基于Visium HD生成的对照组与UIRI小鼠肾脏细胞区域解剖分布空间图谱。
f) Visium HD数据空间特征图,显示基于RCTD细胞反卷积分析的主要肾细胞类型在对照组(上图)和UIRI组(下图)中的空间分布。
g) 标准Visium空间转录组数据中NMF因子与细胞类型反卷积得分相关性热图。
h) 与纤维化微环境最相关的NMF因子基因得分空间分布及关键基因对各因子的贡献度。
i) 标准Visium数据中Tnc基因表达解剖分布的空间特征图。
j) Visium HD空间转录组数据中NMF因子与细胞类型反卷积得分相关性热图。
k) Visium HD数据中与纤维化微环境相关的NMF因子(NMF3与NMF11)空间分布及其对应的高贡献基因。
l) Visium HD数据集中Tnc表达解剖分布的空间特征图。
m) 免疫荧光染色显示TNC与巨噬细胞(F4/80+)在CMJ间质区域的共定位。从上至下:整体合并图像(Merge),同区域TNC、Vimentin和F4/80染色的放大视图,以及底部的放大合并图像(Enlarged Merge)。
3. TNC富集微环境促进巨噬细胞活化
研究进一步分析单侧输尿管梗阻(UUO)模型的单细胞及空间转录组数据。虽然UUO诱导的纤维化主要定位于外髓内带-内髓交界区,与UIRI好发于皮质-髓质交界区的分布特点不同,但该区域同样出现了TNC富集的成纤维细胞-巨噬细胞微环境,提示TNC在不同纤维化模型中的相同作用。基因集变异分析(GSVA)显示,TNC表达水平升高与ECM重塑、细胞黏附和Wnt通路激活呈正相关。空间配体-受体分析发现皮质-髓质交界处存在显著的成纤维细胞-巨噬细胞通讯枢纽。单细胞互作预测提示,成纤维细胞来源的TNC可能通过其纤维蛋白原(FBG)样球状结构域与巨噬细胞TLR4结合。
为了验证TNC在介导成纤维细胞-巨噬细胞相互作用中的功能,研究构建了TNC-shRNA敲低模型,并结合脱细胞肾脏组织支架(dc-KTS)进行体外共培养实验。结果显示,TNC富集的微环境能显著诱导骨髓来源巨噬细胞(BMDMs)表达TLR4、p-P65、P65、甘露糖受体(MR)、精氨酸酶-1(Arg-1)和肿瘤坏死因子-α(TNF-α),而敲低TNC则显著抑制此效应。实验结果明确显示,TNC富集的微环境能够促进巨噬细胞活化并加剧肾纤维化(图3)。
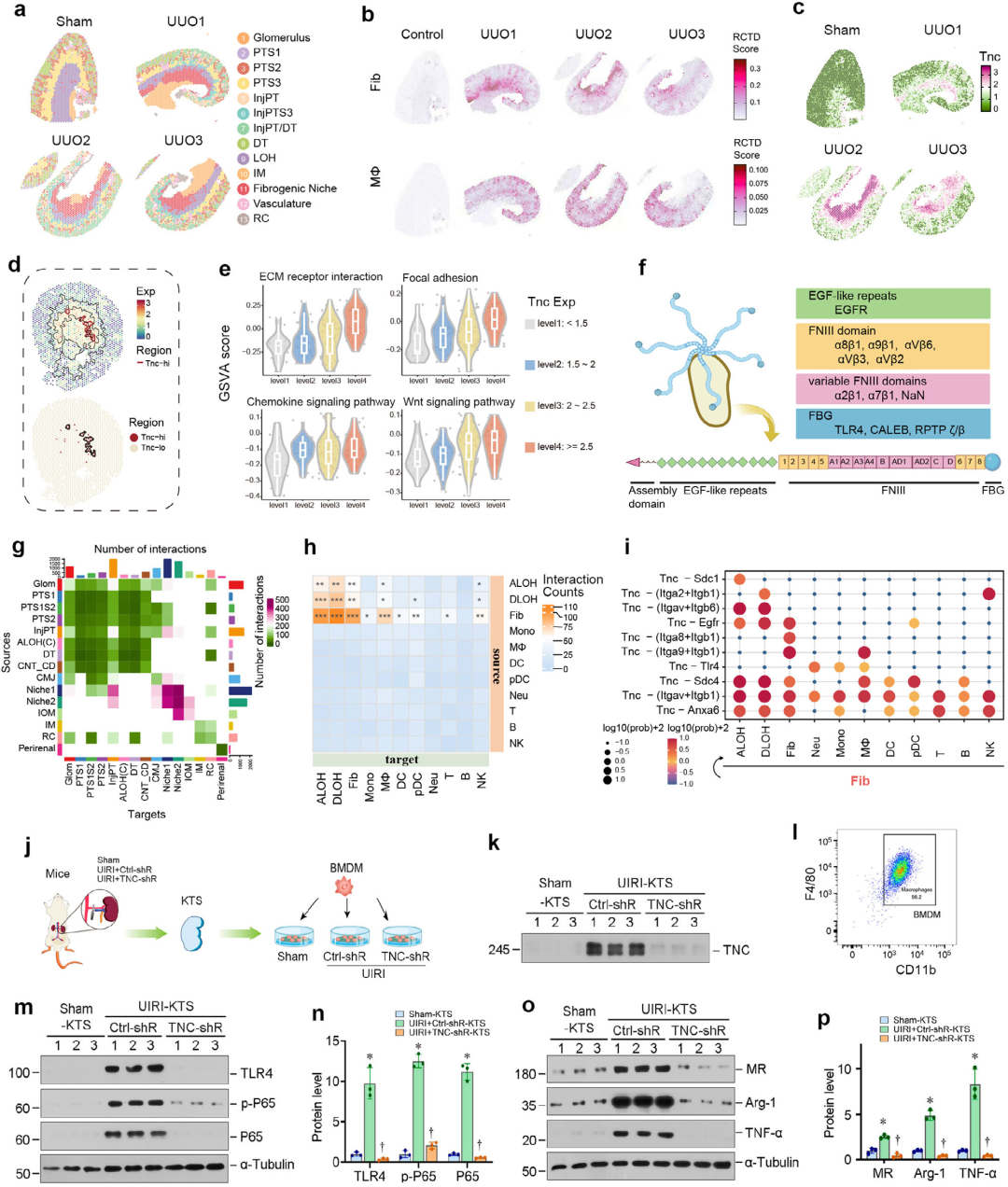
图3. TNC富集微环境促进巨噬细胞增殖与活化
a)Sham组与UUO模型肾脏细胞区域解剖分布空间图谱。
b)Sham组与UUO组基于RCTD分析的成纤维细胞(Fib)和巨噬细胞(Mϕ)得分空间特征图。
c)Sham组与UUO样本中Tnc基因表达模式的空间分布图。
d)Tnc在纤维化肾脏中的空间表达谱(上图)。红色斑点代表Tnc高表达区域(Exp ≥ 2.5)(下图)
e)按Tnc表达水平将UIRI组空间点分为四类,采用limma进行差异通路分析(P值≤0.1)并通过小提琴图可视化。
f)Tnc结构域及其对应受体示意图。
g)CellChat预测的UIRI组各空间区域配体-受体相互作用热图,颜色深度代表显著相互作用对的数量。
h)UIRI组成纤维细胞富集区细胞相互作用数量热图,颜色强度与配体-受体对数量相关。"Sender"指信号源,"Target"指信号接收方。
i)气泡图显示成纤维细胞通过Tnc与各细胞类型的相互作用,颜色深度与气泡大小反映log10(Prob+1)值。"Prob"表示相互作用概率,阈值为0.01。
j)将BMDMs培养于TNC富集或缺失的肾脏组织支架(KTS)的实验方案示意图。KTS制备自假手术、UIRI+对照shRNA和UIRI+TNC-shRNA小鼠肾脏。将BMDMs接种于不同KTS上培养48小时。
k)小鼠体内敲低TNC导致KTS中TNC蛋白水平下降。Western blot显示各组KTS中TNC蛋白表达水平。
l)流式细胞术通过CD11b和F4/80染色显示BMDMs纯度,CD11b+F4/80+细胞比例>95%。m,n) TNC富集KTS诱导TLR4、p-P65和P65表达。Western blot显示各组TLR4、p-P65和P65蛋白水平。代表性Western blot图(m)及定量数据(n)。*与假手术组相比p < 0.05,†与UIRI+Ctrl-shRNA组相比P < 0.05(n = 3)。
o,p) TNC富集KTS诱导BMDMs中MR、Arg-1和TNF-α表达。Western blot显示各组MR、Arg-1和TNF-α蛋白水平。代表性Western blot图(o)及定量数据(p)。*与假手术组相比p < 0.05,†与UIRI+Ctrl-shRNA组相比P < 0.05(n = 3)。
4. TNC在体外促进巨噬细胞增殖与活化
为明确验证TNC对巨噬细胞活化的介导作用,研究团队通过将BMDMs与人源TNC蛋白直接共培养,并采用RNA测序分析其基因表达谱。结果显示,TNC刺激组与对照组基因表达存在显著差异;基因本体富集分析发现免疫应答、细胞因子受体结合及免疫受体活性相关基因显著富集;KEGG通路分析进一步表明,细胞因子-受体相互作用、TNF、TLR及NF-κB等炎症通路被明显激活(图4a-d)。为评估TNC作用的特异性,使用浓度匹配或更高的胶原蛋白I和纤连蛋白进行对比。结果显示,二者均未改变BMDMs中TNF-α、CCL2、c-Fos及PCNA的蛋白表达。综上,TNC在体外可特异性促进巨噬细胞的活化、增殖、迁移、吞噬及细胞因子产生。
5.TNC通过TLR4/NF-κB信号通路激活巨噬细胞
研究发现TLR信号通路在TNC刺激的巨噬细胞中显著富集,为验证TNC是否直接与TLR4相互作用,研究团队进行了免疫共沉淀实验。结果显示,无论使用抗TNC还是抗TLR4抗体进行沉淀,均能检测到TNC与TLR4的结合,证实二者存在直接相互作用。进一步体外实验表明,TNC以剂量依赖方式上调巨噬细胞中TLR4、p-P65、TNF-α及CCL2的表达,提示其可激活TLR4/NF-κB信号通路。采用TLR4特异性抑制剂TAK-242处理后,TNC诱导的TLR4表达、P65活化以及TNF-α、CCL2、c-Fos和PCNA蛋白水平均被显著抑制,说明TLR4信号是TNC介导巨噬细胞增殖与活化的必要条件。功能实验进一步证实,阻断TLR4可抑制TNC诱导的DNA合成细胞迁移及S期细胞比例增加(图4)。
为深入验证该机制,在TLR4阻断抗体存在下以TNC刺激BMDMs,结果显示TLR4/NF-κB通路激活及相关蛋白表达均被抑制。以上结果表明,TNC通过激活TLR4/NF-κB信号通路促进巨噬细胞活化。
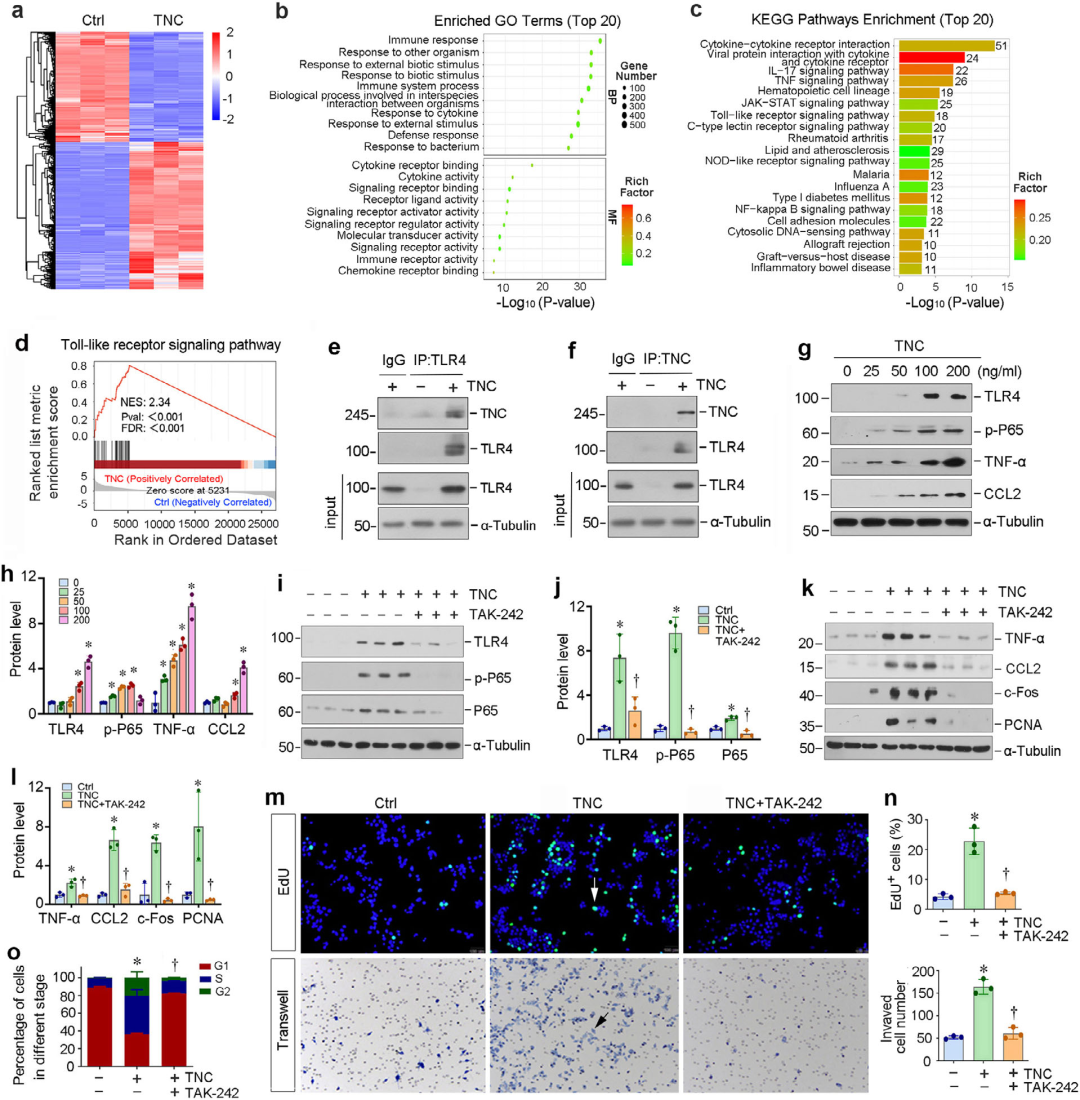
图4. TNC通过触发TLR4/NF-κB信号级联反应在体外诱导巨噬细胞增殖与活化
a)mRNA聚类分析显示对照组与TNC刺激24小时巨噬细胞的基因表达存在显著差异。
b)GO富集分析显示多个信号通路被显著富集。
c)KEGG富集分析揭示多个信号通路被激活。
d)GSEA富集分析表明Toll样受体(TLR)信号通路在TNC刺激的巨噬细胞中富集。NES:标准化富集分数;FDR:错误发现率。
e,f) 免疫共沉淀实验证实TNC与巨噬细胞中TLR4结合。将BMDMs在TNC存在或不存在条件下培养,细胞裂解液分别用IgG、抗TLR4或抗TNC抗体进行免疫沉淀,再用抗TNC和抗TLR4抗体进行免疫印迹分析。
g,h) TNC在体外激活TLR4/NF-κB信号级联。用不同浓度TNC处理BMDMs 48小时,代表性Western blot图(g)及定量数据(h)。*与对照组相比p < 0.05,†与TNC组相比P < 0.05(n = 3)。
i,j) 阻断TLR4抑制TNC诱导的BMDMs中NF-κB信号激活。BMDMs用TLR4抑制剂TAK-242(5 nM)预处理2小时,再用TNC(100 μg ml−1)处理48小时。Western blot图(i)及定量数据(j)。*与对照组相比p < 0.05,†与TNC组相比P < 0.05(n = 3)。
k,l) 阻断TLR4/NF-κB信号通路消除TNC诱导的巨噬细胞增殖与活化。BMDMs用TAK-242(5 nM)预处理2小时,再用TNC(100 μg ml−1)处理48小时。Western blot图(k)及定量数据(l)。*与对照组相比p < 0.05,†与TNC组相比P < 0.05(n = 3)。
m,n) 阻断TLR4抑制TNC诱导的巨噬细胞增殖与迁移。EdU掺入实验显示TLR4抑制剂TAK-242抑制TNC诱导的BMDMs DNA合成,代表性EdU掺入实验图(m)及定量数据(n)。Transwell实验显示阻断TLR4抑制TNC诱导的巨噬细胞迁移,代表性Transwell迁移实验图(m)及定量数据(n)。*与对照组相比p < 0.05,†与TNC组相比P < 0.05(n = 3)。
o) 流式细胞术显示TNC(100 ng ml−1)处理48小时后BMDMs细胞周期各时相分布。定量数据(m)。*与对照组相比p < 0.05,†与TNC组相比P < 0.05(n = 3)。
6. 内源性TNC在体内加剧肾脏炎症
为阐明TNC在体内对巨噬细胞活化的作用,在UIRI模型第4天通过静脉注射TNC-shRNA质粒以敲低其表达。免疫组化显示,TNC高表达区域伴随大量F4/80⁺巨噬细胞浸润,而敲低TNC后该部位巨噬细胞数量相应减少。体内实验表明,敲低TNC可抑制UIRI肾脏中MR、Arg-1、iNOS和TNF-α等巨噬细胞活化标志物的蛋白表达,并降低iNOS、TNF-α、IL-6和IL-1β的mRNA水平。同时,TLR4/p-P65/P65蛋白表达也随TNC敲低而下降。免疫荧光进一步显示,UIRI小鼠CMJ区F4/80⁺与TLR4⁺细胞共定位增多,该现象在TNC敲低后被抑制。流式分析证实UIRI肾脏中F4/80⁺/CD11b⁺/CD45⁺巨噬细胞数量显著增加,而TNC敲低使其减少。Masson染色亦表明敲低TNC可减轻CMJ区纤维化病变。以上结果说明内源性TNC在体内通过促进巨噬细胞活化驱动肾脏纤维化进程。
7. 抑制或敲除TLR4可减轻肾脏炎症与纤维化
为验证TNC/TLR4/NF-κB信号级联在肾脏炎症与纤维化中的作用,在UIRI模型中使用TAK-242抑制TLR4信号。结果显示,TLR4抑制显著降低UIRI引起的血清肌酐和BUN升高,并下调肾脏中MR、Arg-1、TNF-α及CCL2的表达。TAK-242还抑制了TLR4表达及P65磷酸化,同时降低TNC、纤连蛋白和α-SMA等纤维化标志物水平。流式与免疫荧光分析进一步表明,TAK-242处理可减少UIRI肾脏中F4/80⁺/CD11b⁺/CD45⁺巨噬细胞浸润,抑制CMJ区α-SMA表达,并减轻胶原沉积与纤维化病变。
进一步采用TLR4基因敲除(KO)小鼠进行研究。Western blotting显示TLR4-KO可抑制UIRI后的NF-κB信号活化,降低TLR4、p-P65及P65蛋白表达,并改善肾功能指标。RNA-seq分析表明,与WT-UIRI组相比,TLR4-KO-UIRI组中TLR4、CCL2、Arg-1和TNF-α等基因表达下调。基因本体富集分析显示,WT-UIRI组中巨噬细胞活化、免疫调节及NF-κB相关通路显著富集,而TLR4-KO可逆转此趋势。热图与GSEA进一步确认TLR4缺失可抑制多种炎症因子表达及巨噬细胞活化。蛋白水平上,TLR4-KO有效降低MR、Arg-1、iNOS、TNF-α等炎症蛋白,以及TNC、FN和α-SMA等纤维化蛋白的表达,免疫染色也显示其减轻巨噬细胞浸润与胶原沉积。
8. 巨噬细胞中TLR4的激活是肾脏炎症与纤维化的关键环节
为明确巨噬细胞特异性TLR4激活在肾脏病变中的作用,研究团队构建了骨髓嵌合体模型:将野生型(WT)或TLR4敲除(KO)小鼠的骨髓移植给经辐照清髓的WT受体。结果显示,与移植WT骨髓的受体(WT-WT)相比,移植TLR4 KO骨髓的受体(TLR4 KO-WT)在UIRI后血肌酐和BUN水平显著降低。Western blot分析表明TLR4 KO-WT组TLR4/NF-κB通路活化减弱,免疫荧光共染色显示肾间质中TLR4⁺/F4/80⁺巨噬细胞浸润减少。同时,该组肾脏中MR、Arg-1、iNOS、TNF-α、CCL2等炎症标志物,以及TNC、FN和α-SMA等纤维化蛋白表达均显著下降。以上结果证实,巨噬细胞中TNC触发的TLR4激活是驱动损伤后肾脏炎症与纤维化的关键机制。
肾脏纤维化通常始于特定局灶区域,通过形成纤维化微环境促进炎症细胞与成纤维细胞的活化和显著扩增。本研究整合单细胞RNA测序与空间转录组学技术,系统解析了纤维化肾脏中的细胞异质性、空间构象及分子互作网络。研究首次揭示了纤维化微环境中成纤维细胞、细胞外基质成分与巨噬细胞之间驱动肾脏炎症与纤维化的复杂相互作用机制,为深入理解该微环境的细胞组成、空间构架、细胞通讯及分子调控网络提供了新的视角。
研究证实了TNC通过激活巨噬细胞 TLR4/NF-κB 通路驱动炎症-纤维耦合的信号枢纽。未来,通过在人类肾组织中进一步验证该机制的普适性,并开发靶向TNC-TLR4相互作用的小分子或抗体药物,有望开创以“阻断促纤维化微环境”为核心的全新治疗策略。值得注意的是,TLR4作为进化上保守的模式识别受体,不仅调控先天性与适应性免疫应答,在心血管、肾脏、肺脏及肝脏等器官的非感染性炎症疾病发病机制中也扮演着关键角色,因此本研究建立的空间组学解析局部病理微环境的研究范式,可拓展至肝、肺、心脏等多器官纤维化疾病研究,为系统揭示器官微环境重塑的精细调控网络提供全新维度。
点击“阅读原文”,查看文献
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。仅供HCP观看。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)