
为研究AMA阴性PBC的潜在机制,Wasik等对AMA阴性和阳性PBC患者血清中的微小RNA(microRNA)进行检测,发现AMA阴性PBC患者血清中miR-21的表达显著升高,并与AMA抗体滴度呈负相关。推测miR-21可能通过影响B细胞的分化和功能,以及调节免疫细胞的甲基化状态,间接导致AMA减少。AMA通过识别人胆管上皮细胞(BEC)凋亡小泡内的PDC-E2,诱发自身反应性CD4+和CD8+T细胞对BEC的损伤,但AMA阴性PBC患者BEC损伤的机制尚不明确。Deng等利用生信技术对AMA阴性和阳性PBC患者的血清抗原进行比较,发现AMA阴性组中参与B细胞活化、吞噬识别及补体激活的蛋白表达显著上调,而参与线粒体中电子传递和细胞代谢过程的蛋白显著下调,与AMA阳性组患者相反。因此,AMA阴性PBC患者可能存在不同机制介导的BEC损伤。
AMA阴性PBC患者的临床表现、实验室指标、组织学特征、治疗反应与AMA阳性患者大致相同,但存在细微差异。相较于AMA阳性PBC患者,AMA阴性PBC患者发病年龄可能更小,组织学上的炎症程度更严重,血清免疫球蛋白M水平更低。然而,两者在肝脏相关并发症、死亡率或

1抗核抗体(ANA)作为无创性诊断指标的临床应用
在30%~50%的PBC患者中,可以检测出多种ANA。借助IF将ANA分为核包膜模式和多核点模式2种特定荧光类型。核包膜模式用于检测抗核包膜抗体,主要针对核孔复合体(NPC)蛋白,如糖蛋白210(gp210)、核孔蛋白p62(NUP62)等自身抗体;多核点模式主要检测抗核点抗体,主要针对嗜酸性粒细胞
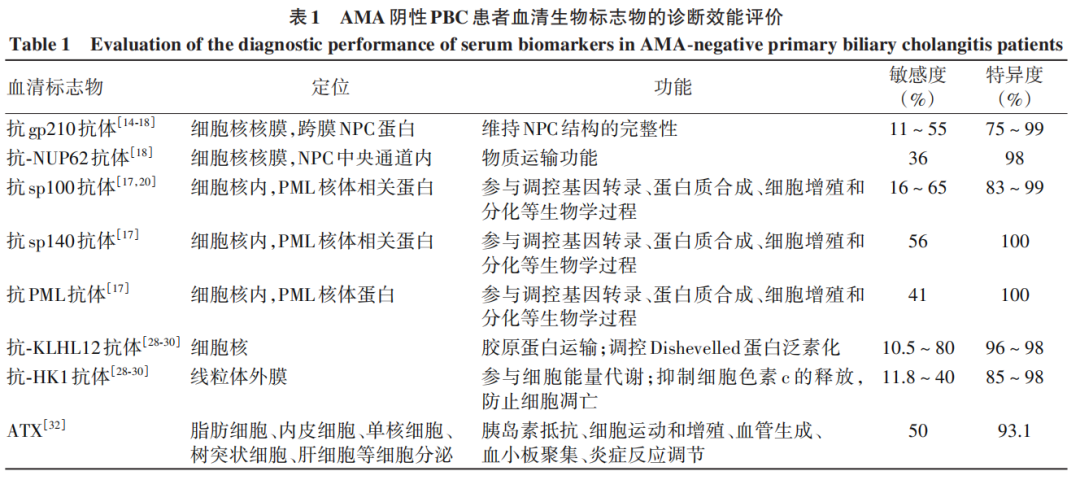
gp210是一种跨膜核孔蛋白,位于NPC的内核膜和外核膜之间,其主要功能是维持NPC结构的完整性,确保NPC在核质运输、基因表达调控及DNA修复等过程中正常发挥作用。抗gp210抗体主要识别gp210羧基末端15个
NUP62位于NPC的中央通道内,富含
sp100是一种与PML核体相关的蛋白,其免疫荧光染色遍布整个细胞核但不涉及核仁。sp100同样与线粒体和大肠埃希菌存在PDC-E2的分子模拟现象。与抗gp210抗体不同,PBC患者的sp100自身抗体可识别多个表位,因此部分患者在疾病进展和
sp140结构与sp100相似,其氨基酸末端部分与sp100的相应区域具有约50%的同源性,均为PML核体蛋白。PML作为PML核体骨架结构的主要成分,其核体主要定位于细胞核中,参与基因转录调控、蛋白质合成、细胞增殖和分化等生物学过程。抗sp140和抗PML抗体通常伴随抗sp100抗体出现,反之则不成立,因此单独针对抗sp140或抗PML抗体在PBC诊断中作用的研究相对较少。尽管PML抗原在PBC的肝脏组织中高表达,提示其可作为区分其他胆汁淤积性肝病的潜在组织学标志物,但在临床实践中,检测血清抗sp140或抗PML抗体水平的无创性辅助诊断方法尚未普及。

2其他生物标志物
KLHL12位于细胞核内,包括BTB/POZ、Kelch和BACK共3个结构域,其中BTB/POZ结构域负责与Cullin 3蛋白结合;Kelch结构域用于识别和招募底物;BACK结构域则连接上述2个功能区。KLHL12主要负责胶原蛋白的运输及Dishevelled蛋白的泛素化调控。HK1位于线粒体外膜,作为三羧酸循环的关键酶,可催化
Norman等利用高密度人类重组蛋白微阵列的蛋白组学技术,发现PBC患者中抗-KLHL12和抗-HK1抗体水平异常升高;在后续ELISA验证中,这2种抗体在AMA阴性PBC患者中的检出率分别为35%和22%。随后几年,Norman在欧洲和北美5个临床试验中心的PBC人群中开展抗-KLHL12和抗-HK1抗体的检测研究,结果显示,这2种抗体在AMA阴性PBC患者中的阳性率分别为10.3%~80.0%和11.8%~40.0%,数据结果存在较大波动,可能与各临床中心样本数量和种族人群异质性相关。联合检测结果显示,AMA阴性患者中至少对一种抗体呈阳性的比例为38.4%,因此联合检测抗-KLHL12和抗-HK1抗体可提高AMA阴性PBC患者的诊断覆盖率。我国最新研究报告显示,抗-KLHL12抗体诊断AMA阴性PBC的敏感性、特异性分别为12.5%、98%,抗-HK1抗体的敏感性、特异性分别为33.3%、98%,与以往研究结果一致;亚洲人群数据的补充,进一步验证了这2种抗体作为全球通用生物诊断标志物的可行性。此外,多数研究显示抗-HK1抗体水平高于抗-KLHL12抗体,这可能与两者的抗原定位差异相关(HK1位于细胞质中,而KLHL12位于细胞核内)。
ATX是一种由外核苷酸焦磷酸二酯酶基因编码的分泌型溶脂磷酶,通过催化溶血磷脂酰胆碱水解生成具有生物活性的溶血磷脂酸,参与

3AMA阴性PBC传统血清标志物的临床挑战
虽然抗gp210抗体和抗sp100抗体已被纳入国内外指南的诊断标准,但在AMA阴性PBC患者中,仅部分患者表现为ANA阳性,存在漏诊风险。ANA产生机制的复杂性及检测方法的局限性是其低敏感性的主要原因。在产生机制方面,遗传和感染因素均可能影响ANA的生成;此外,ANA主要的抗原靶点位于细胞核内,与AMA所针对的细胞质线粒体存在显著差异。在检测方法方面,临床上用于检测ANA的主要方法包括IF、ELISA和IB,这些技术通常用于定性或半定量分析,且自动化水平有限。为了提升检测技术的准确性,一种基于多颗粒载体的检测技术逐渐成为研究热点,该技术构建的包被特异性抗原表位的不同微球载体可同时检测多种自身抗体,实现联合诊断。Wang等研究表明,使用多重微球流式荧光免疫技术(MBFFI)联合检测AMA-M2、抗gp210和抗sp100抗体,结果与传统IF方法一致,且能提高AMA阴性PBC患者诊断的敏感性。Villalta等研究建议将抗-KLHL12和抗-HK1抗体纳入联合检测体系,但该新型检测技术在临床实际应用中仍面临成本高昂、缺乏统一的临界值标准、数据解读复杂等诸多挑战。未来需通过多中心验证研究,建立标准化的检测流程。
sp140、PML与sp100均属于PML核体组分。研究显示抗sp140和抗PML抗体几乎仅出现在抗sp100阳性患者中,反之则不成立。这表明sp100可能是针对PML核体免疫反应的首要靶点,随后通过抗原表位扩散机制扩展至sp140和PML,因此抗sp100抗体更常作为临床诊断标准。
目前,针对抗-KLHL12抗体、抗-HK1抗体和ATX的研究多基于小样本,缺乏大规模队列验证,研究数据有限,临床证据不足,因此尚未广泛应用。未来可借助MBFFI等新型高通量检测技术进行多种抗体联合检测,实现AMA阴性PBC诊断从单一抗体依赖向多抗体谱分析的转变(图1)。
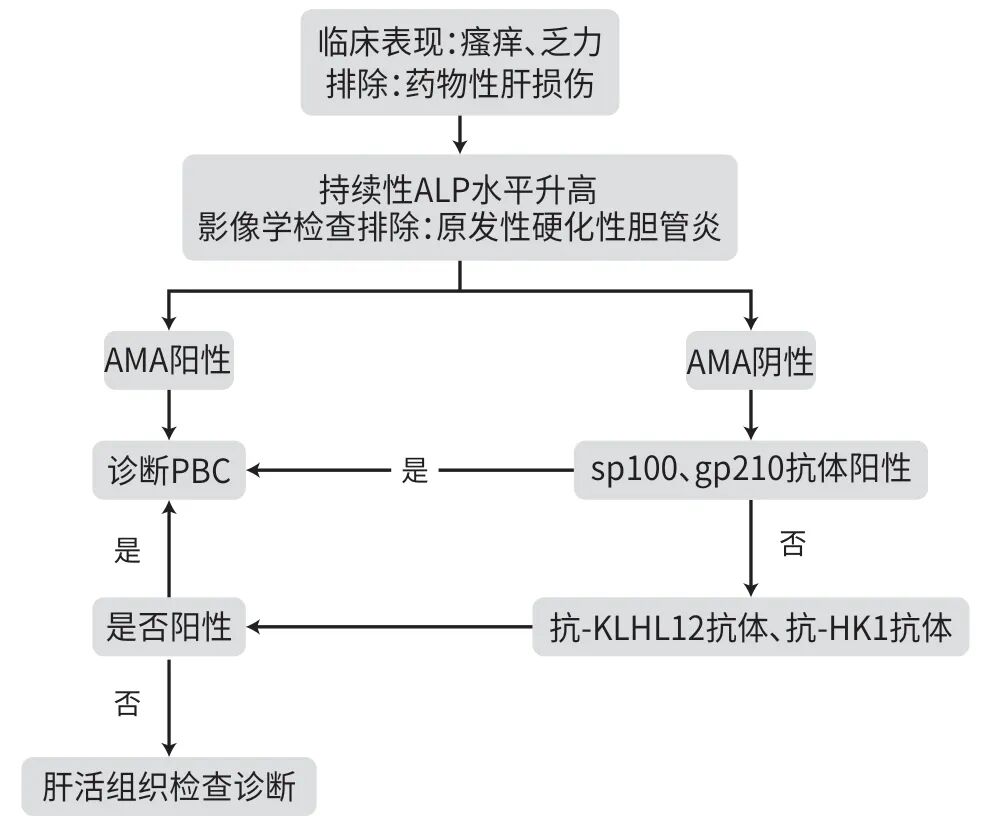
图1 AMA阴性PBC的分层诊断流程

4可溶性免疫检查点和抗细胞因子抗体的诊断潜力
目前,在AMA阴性PBC患者的血清标志物识别中,普遍存在高特异性、低敏感性的问题。尽管新发现的ATX在AMA阴性PBC患者中的敏感性高达50%,但为了验证其在临床应用中的可行性,仍需开展进一步的临床研究。因此,持续探寻对AMA阴性PBC患者具有高效识别能力的诊断生物标志物具有必要性。
免疫检查点是免疫细胞产生的一类调节自身免疫功能的蛋白分子,能够抑制或促进免疫活动。PBC是肝脏免疫系统异常激活并攻击胆管上皮细胞的结果,因此研究PBC患者免疫检查点的组织学表达有助于理解PBC的发病机制,而血清可溶性免疫检查点的检测可为AMA阴性PBC患者的无创性诊断提供新思路。最新研究发现,PBC患者中可溶性CD134、淋巴细胞活化基因3蛋白(LAG-3)、程序性死亡受体1(PD-1)、程序性死亡-配体1(PD-L1)及T淋巴细胞免疫球蛋白黏蛋白3(TIM-3)的水平显著高于健康对照组,与疾病进展呈正相关。其中,可溶性PD-L1和CD134的受试者操作特征曲线下面积(AUC)分别为0.970 4和0.966 7,其诊断性能优于GGT(0.957 7)和ALP(0.959 1)。CD134作为一种刺激性免疫检查点分子,能够增强单核细胞抗原呈递能力,放大T细胞活化效应,并促进促炎性细胞因子生成;PD-L1作为一种维持免疫耐受的抑制性免疫检查点分子,在抑制T细胞活化和扩增的初始阶段和再次免疫应答中发挥重要的调节作用。然而,这2种可溶性免疫检查点与多种肝脏疾病相关。例如,可溶性CD134与非酒精性脂肪性肝病的进程相关,可溶性PD-L1受体在自身免疫性肝炎和炎症性肠病中呈升高趋势。因此,若将可溶性免疫检测点纳入AMA阴性PBC患者无创性辅助诊断工具,需进一步扩大研究样本数量和病种范围,以提高其诊断特异性。
抗细胞因子抗体(ACAA)是体内可中和或改变细胞因子活性的小分子,可调控细胞因子信号通路或改变细胞因子在循环中的半衰期,具备致病或缓解疾病的潜力,因此可用于疾病的早期诊断。例如,IFN-1抗体可用于诊断婴儿的抗磷脂综合征,IL-12和IL-23抗体可用于监测胸腺恶性肿瘤,高水平的抗B细胞激活因子抗体可能预示系统性红斑狼疮进入缓解期。尽管ACAA的产生机制及其在自身免疫性疾病发病中的具体作用尚未明确,但通过检测这些抗体的存在及水平变化,可实现疾病的早期识别与监测。目前,关于PBC患者中ACAA的水平及其与疾病进程的关联尚无文献报道,未来可对其进行探索性检测。

5小结与展望
血清生物标志物检测是诊断AMA阴性PBC患者的一种经济高效且无创的方法,尽管抗gp210、抗sp100、抗sp140、抗PML、抗-KLHL12和抗-HK1等抗体在诊断时展现出较高的特异性,但敏感性普遍较低,这可能与抗体产生机制、靶点定位和检测方法相关。因此,AMA阴性PBC患者的无创性诊断仍面临临床挑战。可溶性免疫检查点和ACAA可能为新生物标志物的发现提供方向,未来研究应聚焦于优化已知生物标志物的检测手段,致力于发现具有更高敏感性的新生物标志物,以提高诊断效率和准确性。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH250927

周嘉, 周靖媛, 高沿航. 抗线粒体抗体阴性原发性胆汁性胆管炎的无创诊断[J]. 临床肝胆病杂志, 2025, 41(9): 1896-1901
来源:临床肝胆病杂志
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
