目前已开发多种靶向CD123免疫疗法并在人体临床研究中测试,包括抗体、ADC药物和细胞疗法(图1)。图2报告了至今临床试验报告的毒性反应。
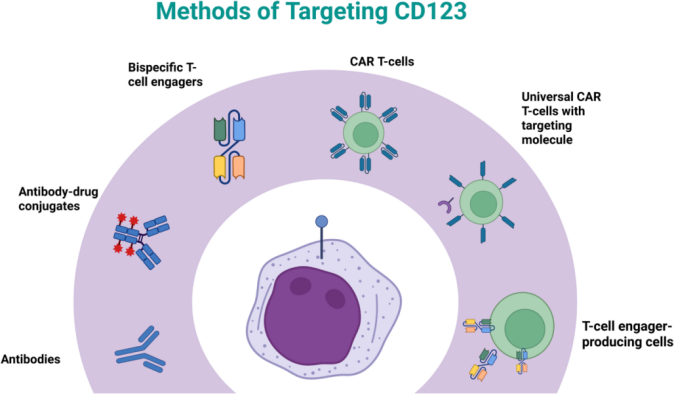
图1
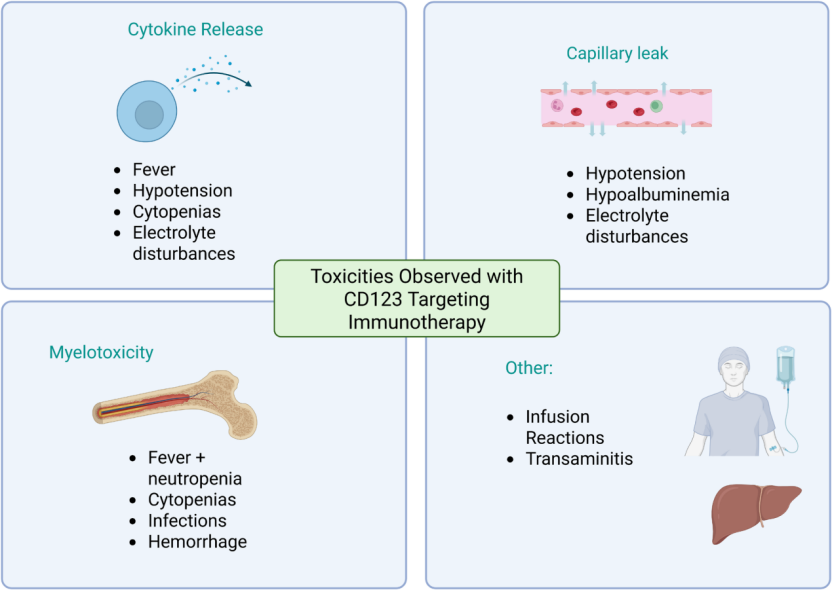
图2
CD123抗体单药治疗的疗效有限。Talacotuzumab(JNJ-56022473, CSL-362)是一种人源化IgG1型抗CD123单克隆抗体,曾在一组无法耐受化疗和/或对去甲基化药物(HMA)耐药的难治性AML患者中进行测试。单药治疗可导致毒性(输注反应和感染),而没有明显的疾病缓解。另一项针对处于形态学缓解期但高复发风险患者的talacotuzumab试验中,结果更为乐观:20例接受治疗的患者中有10例在6个月时维持了持续完全缓解(CR)。
基于抗体的结合与细胞毒性有效载荷传递相结合的疗法通常比单独使用抗体更有效。tagraxofusp是一种将人IL-3与
另一种ADC药物——pivekimab sunirine(IMGN632)是一种与DNA烷化剂药物相结合的CD123抗体。体外证明了IMGN632对表达CD123的AML和ALL细胞系的疗效。一项I/II期试验(NCT03386513)对91例接受R/R AML患者进行了治疗。在确定的目标剂量(每3周0.045mg/kg)下,17%的患者达到CR,<10%的患者出现输液反应和血细胞减少。正在进行的IMGN632联合维奈克拉和阿扎胞苷(NCT04086264)治疗R/R AML患者的I/II期试验中,61例接受治疗的患者客观缓解率达51%,CR率为31%,未观察到毛细血管渗漏综合征。
双特异性衔接分子是一类具有双重靶向能力的免疫治疗药物,设计目的是将两种不同的细胞类型结合在一起。flotetuzumab就是这样一种衔接分子,它是一种双亲和重定向抗体(DART),包含一个结合CD123的scFv和一个结合CD3ε的scFv。flotetuzumab最初作为挽救治疗用于R/R AML患者的临床试验(NCT02152956)中,治疗缓解率达到30%。APVO436是另一种双特异性抗体。它在一项针对 R/R AML 患者的 I 期临床试验(NCT03647800)中进行了测试,剂量从每周 0.3μg 递增至 60μg。研究观察到输液反应和细胞因子释放综合征(CRS),但即使在最高剂量下,这些反应也既非剂量限制性毒性,也与疾病负荷无关。令人鼓舞的是,在34例AML患者中,2例先达到PR,随后在输液后90天以上达到CR。此外,22例接受治疗的患者在最佳缓解时达到疾病稳定,其中8例维持该稳定状态超过3个月。第三种CD123×CD3小分子衔接分子vibecotamab(XmAb14045)在一项纳入 120 例R/R AML 患者的 I期临床试验(NCT02730312)中进行了测试。大多数接受治疗的患者(59.2%)出现轻度(≤2 级)CRS,提示药物具有活性,但仅 9% 的患者达到 CR。
虽然T细胞接合分子作用时间短且疗效取决于患者自身效应细胞的适应性,CAR-T细胞可以提供活化的靶向效应细胞增殖库。单靶点自体 CD123 CAR-T 细胞目前正处于治疗儿童和成人患者的临床试验阶段。尽管这些研究的大部分数据仅以摘要形式发布,但它们为该疗法的潜在毒性和疗效提供了重要见解。首个 CD123 CAR-T 细胞应用的报道来自 1 例经多线治疗无效、异基因骨髓移植(BMT)后复发的 AML 患者,该患者最终接受了靶向 CD123 的 CAR-T 细胞治疗。细胞治疗输注后患者出现 CRS,且对 IL-6 受体阻断抗体
CD123 CAR-T细胞抗AML活性的首个证据来自希望之城(City of Hope)开展的一项 CD123 CAR-T 细胞产品剂量递增研究:6 例接受治疗的患者中有 2 例达到 CR,1 例为起始剂量(5×107 个 CAR-T 细胞),1 例为 2 级剂量(2×108 个 CAR-T 细胞)。
新型靶向CD123免疫疗法目前正处于临床前研究阶段,这些疗法可能会解决目前观察到的一些障碍,从而达到最佳的抗AML活性。具有前景的创新性策略包括:多抗原靶向、药物疗法和细胞疗法的联合治疗以及使用非患者来源的效应细胞(如异体T细胞或NK细胞,图3)。
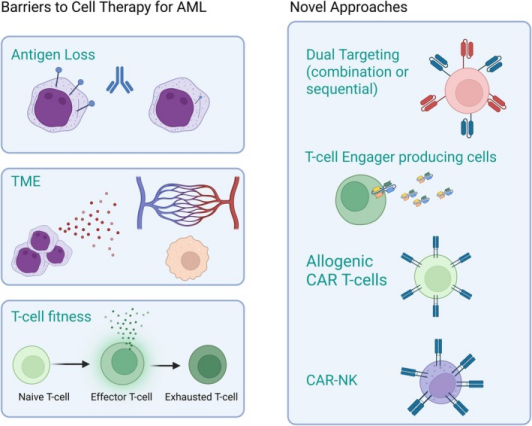
图3
总之,尽管体外实验明确显示靶向 CD123 具有细胞活性,但作为 AML 免疫治疗的一部分,其临床应用仍受限于抗肿瘤细胞毒性不足。尽管多数接受CD123靶向免疫治疗的患者仅出现轻度CRS,但仍有部分患者发生了严重的相关并发症甚至死亡,这凸显了在免疫治疗前识别毒性因素的必要性。
随着靶向CD123疗法及免疫治疗领域的进步,关键问题将在于如何将这些新疗法融入现行标准化疗方案。类似于靶向CD33的gemtuzumab,tagraxofusp等ADC药物可能更容易整合到一线化疗中,具体取决于诊断时的CD123表达情况。免疫治疗可作为联合治疗的有效辅助手段或复发后的二线疗法。最终,靶向CD123治疗AML要取得最佳效果,最可能作为多药联合治疗方案的一部分发挥作用。
参考文献:
Dreyzin A, Holtzman NG, Bonifant CL. CD123-targeting immunotherapeutic approaches in acute myeloid leukaemia. Br J Haematol. 2025 Oct;207(4):1178-1191. doi: 10.1111/bjh.70019. Epub 2025 Jul 24. PMID: 40707180; PMCID: PMC12512072.

戳“阅读原文”,查看更多内容
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)