WHO最新的CML分类中已删除“加速期”CML,转而关注TKI治疗失败、BCR::ABL1激酶区突变或其他预示急变高风险的其他细胞遗传学异常等指标。虽然TKI显著改善了CML-CP预后,但CML-BP患者中位总生存期仍不足1年。异基因
该研究回顾性纳入了2005年7月至2023年11月期间在美国四家医疗中心接受allo-HSCT的75例成年CML患者,包括60例CML-BP(26例髓系,34例淋系),和15例TKI耐药CML-CP。
研究评估了不同治疗方案的疗效,包括针对急变期的强化/非强化化疗以及各代TKI的使用。移植后TKI维持治疗基于残留病灶、基因突变等风险因素实施。
对于MBP患者,强化化疗方案定义为同时包含
TKI的使用按代次分类:第一代包括
研究的主要终点为无白血病生存期(LFS)和总生存期(OS)。
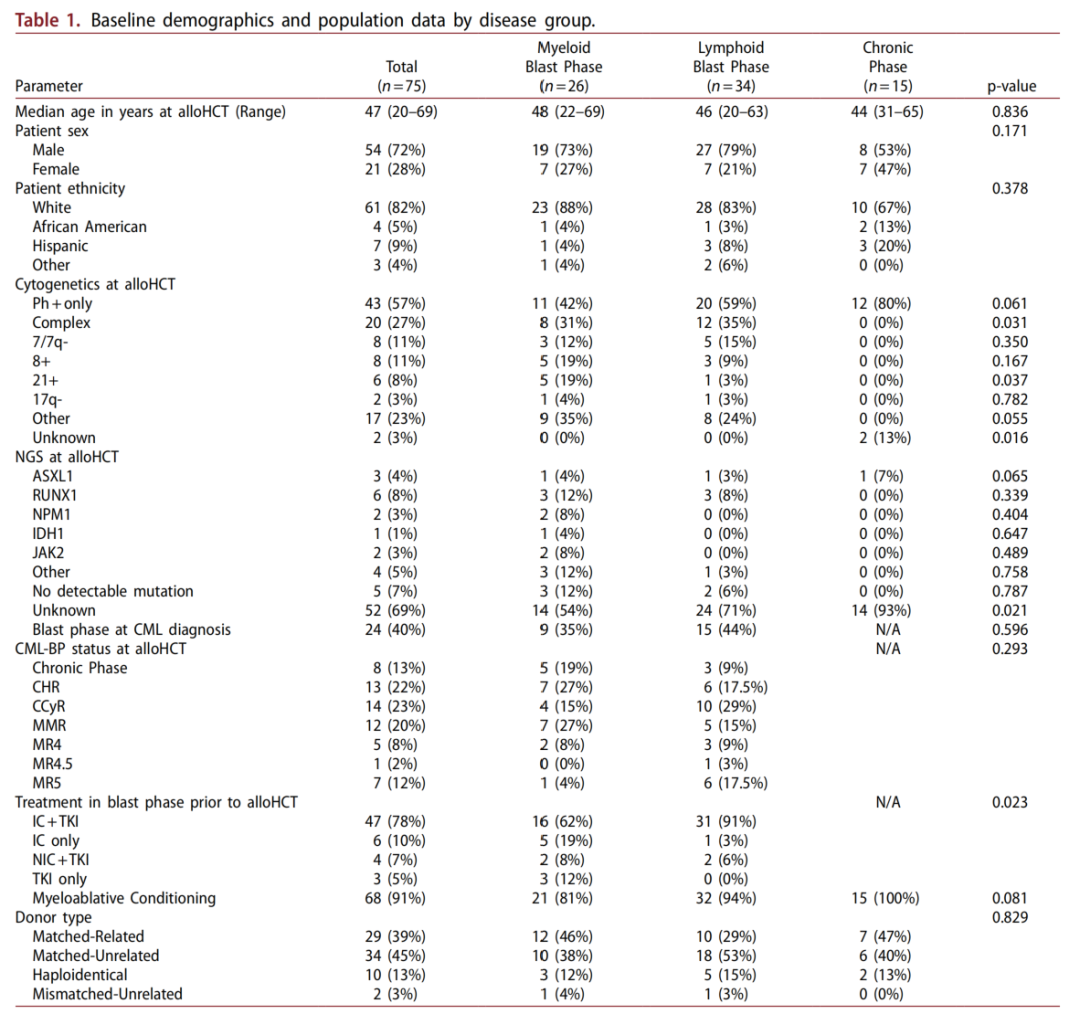
75例CML包括26例MBP(35%)、34例LBP(45%)、15例TKI耐药CML-CP(20%),3组患者的基线特征详见表1。移植时中位年龄为47岁(范围:20-69岁)。
42.7%(n=32)的患者存在Ph+以外的异常。T315I突变发生率为28%(n=19)。在本研究中,鉴于CML-CP患者因TKI耐药而接受移植,ABL1激酶区突变在CML-CP组(87%)中比在CML-BP组(10%)中更常见(p<0.001)。MBP、LBP、CML-CP患者从确诊到allo-HSCT的中位时间分别为13.5、10.6和51.7个月(p=0.008)。
表1
allo-HSCT后全队列和各疾病临床结局的单因素分析结果如表2和表3所示。在75例接受移植的患者中,从移植时开始计算的中位随访时间为41.1个月(范围:0.6-192.9个月),从CML确诊时开始计算的中位随访时间为62.5个月(范围:6.9-221.1个月)。未发现NGS分子突变与临床结局相关(仅有31%患者数据)。部分细胞遗传学异常与临床结局相关,但这些差异主要反映了疾病状态(急变期与慢性期)的不同分布特征。
表2
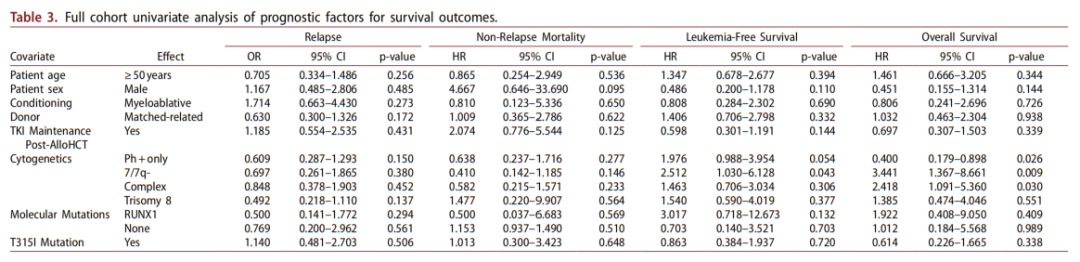
表3
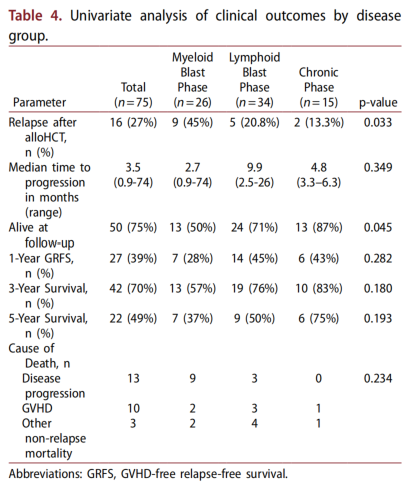
全队列患者的中位LFS和OS均未达到。在MBP、LBP以及CML-CP中,采用Kaplan-Meier估计得到的中位LFS分别为46.6个月、69.3个月和NR,差异无统计学意义(p=0.178)(图1)。在本研究数据回顾时,50例患者仍存活,其3年OS率和5年OS率分别为70%和49%。其中,MBP患者的中位OS为50个月,LBP和CML-CP患者的中位OS均未达到,差异接近统计学意义(p=0.057)(图2)。
亚组分析中,由慢性期转化的MBP的OS和LFS均显著差于原发MBP。移植前达到深度分子学缓解(MR 4.5/5.0)与急变期患者移植后复发风险降低显著相关。
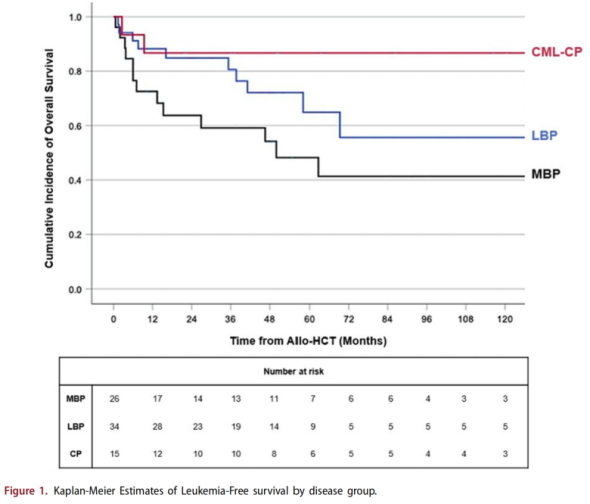
图1
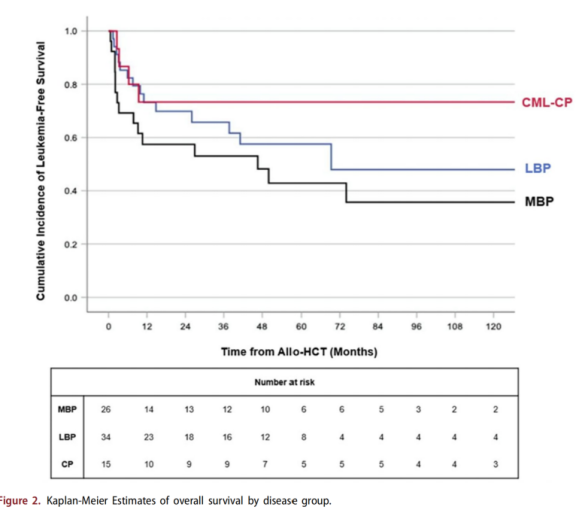
图2
allo-HSCT是CML-BP和TKI耐药CML-CP的有效治疗选择。与CML-BP患者相比,CML-CP患者的复发率、复发相关死亡率更低,且3年和5年生存率更高,这可能是因为CML-BP患者在移植前的细胞遗传学异常负荷更高。因此,随着TKI治疗的不断发展,必须开展更大样本量的亚组分析,以明确allo-HSCT的最佳实施时机,尤其是针对接受多种TKI治疗后仍进展的CML-CP患者。

戳“阅读原文”,查看更多内容