医脉通编辑整理,未经授权请勿转载。
导读
近日,2025年世界肝炎日宣传大会暨第七届慢乙肝临床治愈学术大会在北京圆满举办!肝病领域专家学者共聚一堂,围绕慢乙肝临床治愈的最新研究进展及热点议题展开深度交流与精彩分享,携手见证慢乙肝临床治愈的全新阶段。
大会上,北京大学基础医学院鲁凤民教授就“免疫重建治愈慢性乙肝的问题与挑战”这一主题进行了精彩演讲,医脉通对主要内容进行整理,以飨读者。
我国五次血清HBsAg流行率调查显示,围产期感染
而我国
HBV感染自然史漫长,部分患者30~60年的疾病进程中可能发展为肝硬化和/或肝癌,也可能出现病毒自发清除。急性乙型肝炎呈自限性,病毒可被快速清除,通常不会造成严重
因此,及早进行抗病毒治疗非常重要。对此,《慢性乙型肝炎防治指南(2022年版)》指出,对>30岁的乙肝人群即启动抗病毒治疗,同时对优势人群追求临床治愈,以进一步显著降低乙肝肝病相关死亡风险,也降低病毒负荷减少传播风险。
目前临床常用的核苷(酸)类似物(NAs),主要阻断HBV DNA复制逆转录过程,对病毒蛋白抗原的表达几无影响;对整合源头的HBsAg无直接作用。因此,其累积血清HBsAg清除率有限。但NAs可通过显著减少cccDNA 及整合DNA,为治愈带来优选人群,从而为治愈创造条件。同时,NAs治疗也有助于阻止再感染,从而阻断母婴垂直传播、水平传播。
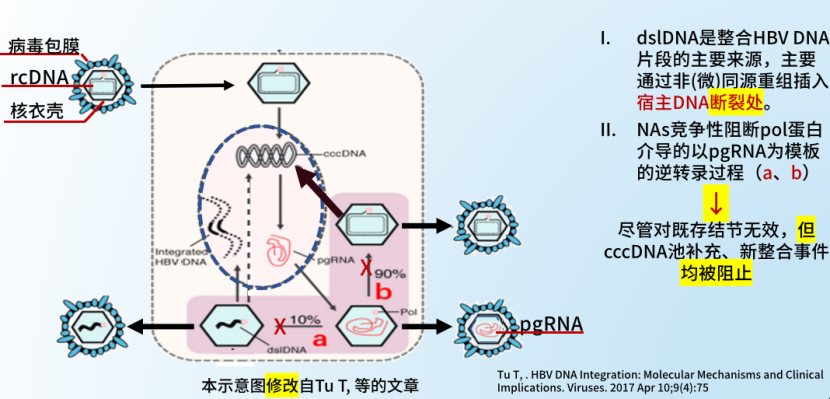
我国在追求乙肝治愈过程中,较早针对优势人群开展治疗,采用以干扰素为基础的治愈方案,而国外仍在探讨干扰素的应用价值。我国学者的Switch、New Switch探索性研究发现HBsAg<1500 IU/mL的人群可尝试追求治愈。卫健委创新大会上和贾继东教授总结出:达到准临床治愈的 “治愈优势人群”序贯/联合免疫调节药物,更有机会实现临床治愈。2018年启动的大型真实世界研究“珠峰” 项目进一步证实这一策略,珠峰计划的8848例“治愈”已经实现,随着治愈门诊在全国的开展,未来会有更多的患者被治愈。
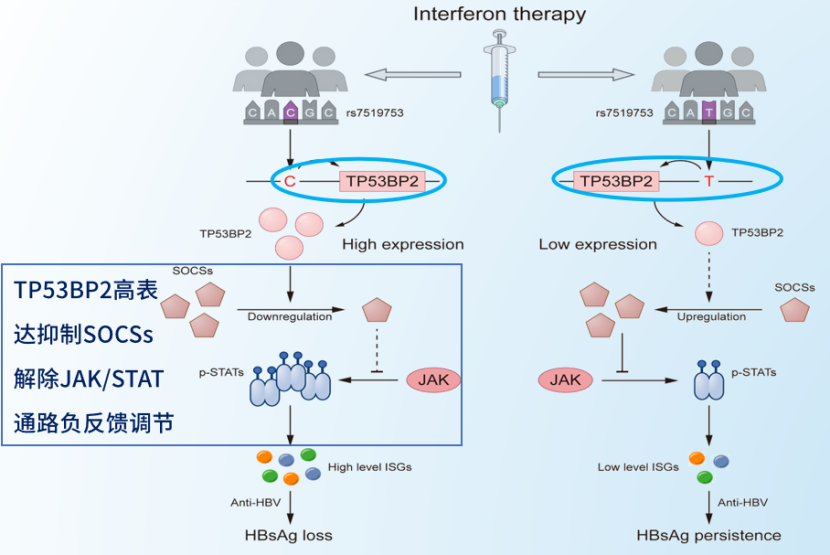
然而,仍有部分优势患者未获得临床治愈,其原因可能与宿主对干扰素应答的负反馈机制有关。干扰素治疗可增强宿主免疫应答,增强抗病毒免疫功能,但也受到负反馈调节机制的影响。而GWAS 研究发现,某多态位点对应TP53BP2高表达可抑制负反馈调节因子SOCSs水平,解除JAK/STAT通路负反馈调节,提高治愈率。对此,有欧美学者提出以治愈为目的的
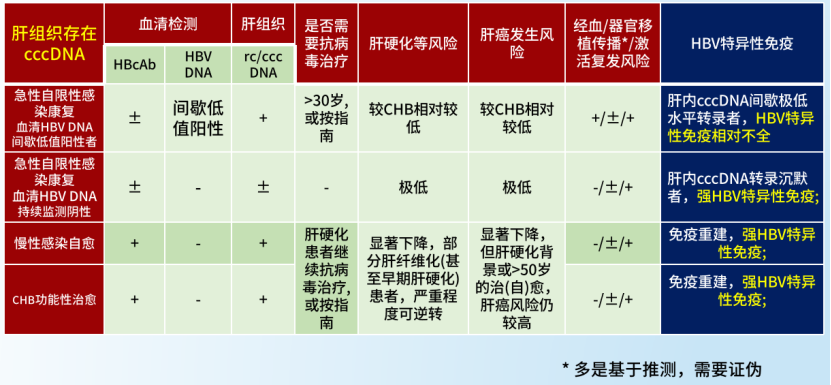
进行有效抗病毒治疗降低病毒负荷,实现抗病毒免疫重建对乙肝治愈具有重要作用。研究显示,不同状态的血清HBsAg持续消失/检测阴性(灵敏试剂),但若肝组织存在cccDNA,尽管其转录活性被显著抑制或沉默,仍有一定的肝硬化和肝癌风险,相关人群需遵循指南进行抗病毒治疗。
有别于未治愈患者,临床治愈患者免疫重建的一大特点是:靶向Pol、HBs的特异性细胞毒性T淋巴细胞(CTL)显著增加。同时,在漫长的疾病进展中,针对Core蛋白的CTL也发挥重要作用。而慢性乙肝难以治愈的主要障碍,除了长期持续炎症死亡与再生的肝脏改变外,还面临宿主HBV特异性免疫应答受损以及宿主免疫选择压力下的HBV适应性突变的挑战。HBV可通过抗原表位突变,逃避CD8+T细胞的识别;而HBV-core的突变频率(71.9%)远高于其他抗原。例如,慢乙肝患者携带前核心蛋白(PC)和基本核心启动子(BCP)突变的发生率随年龄的增长逐渐升高。病毒PC、BCP突变不仅能通过下调或消除HBeAg的表达获得免疫逃逸优势,同时还利用core和pol蛋白的表达增加和HBV复制能力的增强维持慢性HBV感染状态。或许,为了更有效地开展抗病毒治疗和临床治愈,我们该重新关注与疾病进展和转归密切相关的HBV常见突变。
免疫重塑有助于实现乙肝功能性治愈。如何做到免疫重塑?这依赖于恢复有效的宿主抗HBV特异性细胞免疫。持续地抑制病毒蛋白的产生或可恢复患者的特异性抗HBs免疫细胞活性。尽管抗病毒药物可有效降低病毒负荷,但单用难以带来治愈,而抗病毒药物联合Peg-IFN等免疫调节剂,可追求临床治愈。未来,在新药研发下,通过联合/序贯免疫调节治疗或可使乙肝患者获得更广泛的治愈,以进一步消除乙肝危害。

鲁凤民 教授
北京大学感染病研究中心二级教授、主任
北京大学基础医学院病原生物学系暨北京大学第三医院感染疾病中心双聘教授。
科技部及北京市实验室安全专家委员会委员
北京市医学病毒学分会主委
曾任“国家传染病防治科技重大专项”实施方案肝病学组秘书和教育部学位委员会基础医学组委员
研究方向为乙型肝炎病毒及相关肝病、肝癌的发病机制和诊断标志物的研发。提出了受HBV整合影响的宿主基因功能在整合致癌中的关键作用;更新了隐匿性HBV感染(OBI)的定义并建立了相应的实验室诊断方法;实验证实了HBV RNA病毒样颗粒的存在,完善了HBV的生命周期,并与企业合作研发的试剂盒获批临床应用;明确了血清GP73是不同病因慢性肝病肝硬化的可靠诊断指标;提出肝脏弹性指数测定(LSM)是反映肝脏炎症活动度的评价指标,进一步拓展了LSM在慢性肝脏疾病评估中的应用。
作为课题负责人先后承担了国家 “传染病防治” 重大科技专项“11.5、12.5 及13.5”课题、国家自然基金面上项目、北京市科委重大项目以及“863”、“973”计划项目等课题二十余项。
作为第一完成人获得中华医学科技二等奖一项,作为完成人获得国家科技进步二等奖两项。
在国内外期刊发表研究论文近二百篇,被引用近万次。获得授权国家发明专利18项,转化7项。
参考文献
[1] Hui Z,王宇等,Lancet Reg Health West Pac 2024.
[2] 中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2022年版) [J] . 中华传染病杂志, 2023, 41(1) : 3-28.
[3] Toy M, Hutton D, Jia J, So S. Costs and health impact of delayed implementation of a national hepatitis B treatment program in China. J Glob Health. 2022;
[4] 中华医学会肝病学分会. 扩大慢性乙型肝炎抗病毒治疗的专家意见 [J]. 中华肝脏病杂志%, 2022, 30(2): 131-6.
[5] Tu T, . HBV DNA Integration: Molecular Mechanisms and Clinical Implications. Viruses. 2017 Apr 10;9(4):75
[6] Chow N, Wong D, Lai CL, Mak LY, Fung J, Ma HT, Lei MW, Seto WK, Yuen MF. Effect of antiviral treatment on hepatitis B virus integration and hepatocyte clonal expansion. Clin Infect Dis. 2022
[7] 鲁凤民,王杰,陈香梅,江建宁,张文宏,赵景民,任红,侯金林,夏宁邵. 乙型肝炎病毒RNA病毒样颗粒的发现及其对抗病毒治疗临床实践的潜在影响. 中华肝脏病杂志,2017,
[8] Mo ZS, et al. AASLD2022. Abstract (25).
[9] 关贵文, 张婷, Ning J,et al. Higher TP53BP2 expression is associated with HBsAg loss in peginterferon-α-treated patients with chronic hepatitis B. J Hepatol. 2024 Jan;80(1):41-52.
[10] 李明慧,等. Dynamic Changes of Cytokine Profiles and Virological Markers Associated With HBsAg Loss During Peginterferon Alpha-2a Treatment in HBeAg-Positive Chronic Hepatitis B Patients. Front Immunol. 2022
[11] 曹振环,等.Front Cell Infect Microbiol. 2025 doi: 10.3389/fcimb.2025.1615327.
[12] Narmada BC, et.al. J Hepatol. 2024.
[13] Antonio Bertoletti, Gastroenterology. 2020
[14] Ito K, et al. J Virol, 2009.; Tan WS, et al. World J Gastroenterol, 2014.
[15] Schwarz, T., et.al. J Hepatol. 2025.
[16] Li G, Yang D, Liu X,et al. Precore mutation enhances viral replication to facilitate persistent infection especially in HBeAg-negative patients. Virol Sin. 2024 Apr;39(2):319-330.
[17] Daryl T.Y. Lau. Hepatology. 2021
[18] 李明慧,王麟,鲁凤民.慢性乙型肝炎常见PC/BCP突变的可能致病机制[J].肝脏,2024,29(4):371-373.
[19] Balakrishnan, et.al. J Hepatol. 2024.
[20] Chen J, Ji D, Jia J,et al. Functional cure with new antiviral therapy for hepatitis B virus: a systematic review and meta-analysis. Hepatol Int. 2025 Aug;19(4):773-795.
注:图片引自讲者会议幻灯
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)