“基于循证,立足临床;聚焦争议,表达观点”——欢迎来到医脉通特别栏目《话题》

前言
近日,2026全国

医脉通:近日,《肿瘤学年鉴》发表了OPTIMAL研究结果,首次证实口服
孙涛 教授
辽宁省肿瘤医院
研究背景
紫杉醇作为乳腺癌化疗的基石药物,在临床中发挥着重要作用,但其传统静脉制剂也带来了一系列现实挑战。一方面,患者需频繁往返医院,输注耗时长,就医负担重;另一方面,溶媒相关超敏反应需预处理,外周神经毒性等不良事件亦对患者生活质量产生持续影响。因此,开发兼具疗效与便利性的口服剂型,成为临床亟待解决的问题。在这一背景下,基于脂质自乳化技术开发的新型口服紫杉醇制剂DHP107应运而生。该制剂无需联合P-糖蛋白抑制剂即可实现有效吸收,且不含引起过敏和神经损伤的溶剂,有望在保证疗效的同时进一步提升给药便利性与患者依从性,改善整体治疗体验。
研究设计
OPTIMAL研究是一项国际多中心、随机、开放标签的III期临床试验,旨在验证DHP107相较标准静脉紫杉醇的非劣效性。研究共纳入549例既往未接受化疗的HER2阴性复发/转移性乳腺癌患者,按1:1随机分为口服组(277例)与静脉组(272例),每28天为一个周期,于第1、8、15天给药。
口服组接受DHP107 200 mg/m²,每日两次;
静脉组接受紫杉醇80 mg/m²。
研究主要终点为研究者评估的无进展生存期(PFS),预设非劣效风险比(HR)界值为1;次要终点为总生存期(OS)、客观缓解率(ORR)、疾病控制率(DCR)、安全性及生活质量。
研究结果
结果显示,在符合方案集(PPS)人群中,DHP107组和静脉组相比:
中位PFS:10.0个月vs. 8.5个月(HR=0.869;95%CI 0.707–1.068)
中位OS:32.6个月vs. 31.8个月(HR=0.967;95%CI 0.762–1.227)
ORR:43.3% vs 38.8%(OR=1.215;95%CI 0.860–1.718)
DCR:89.2% vs 84.4%(OR=1.533;95%CI 0.927–2.536)
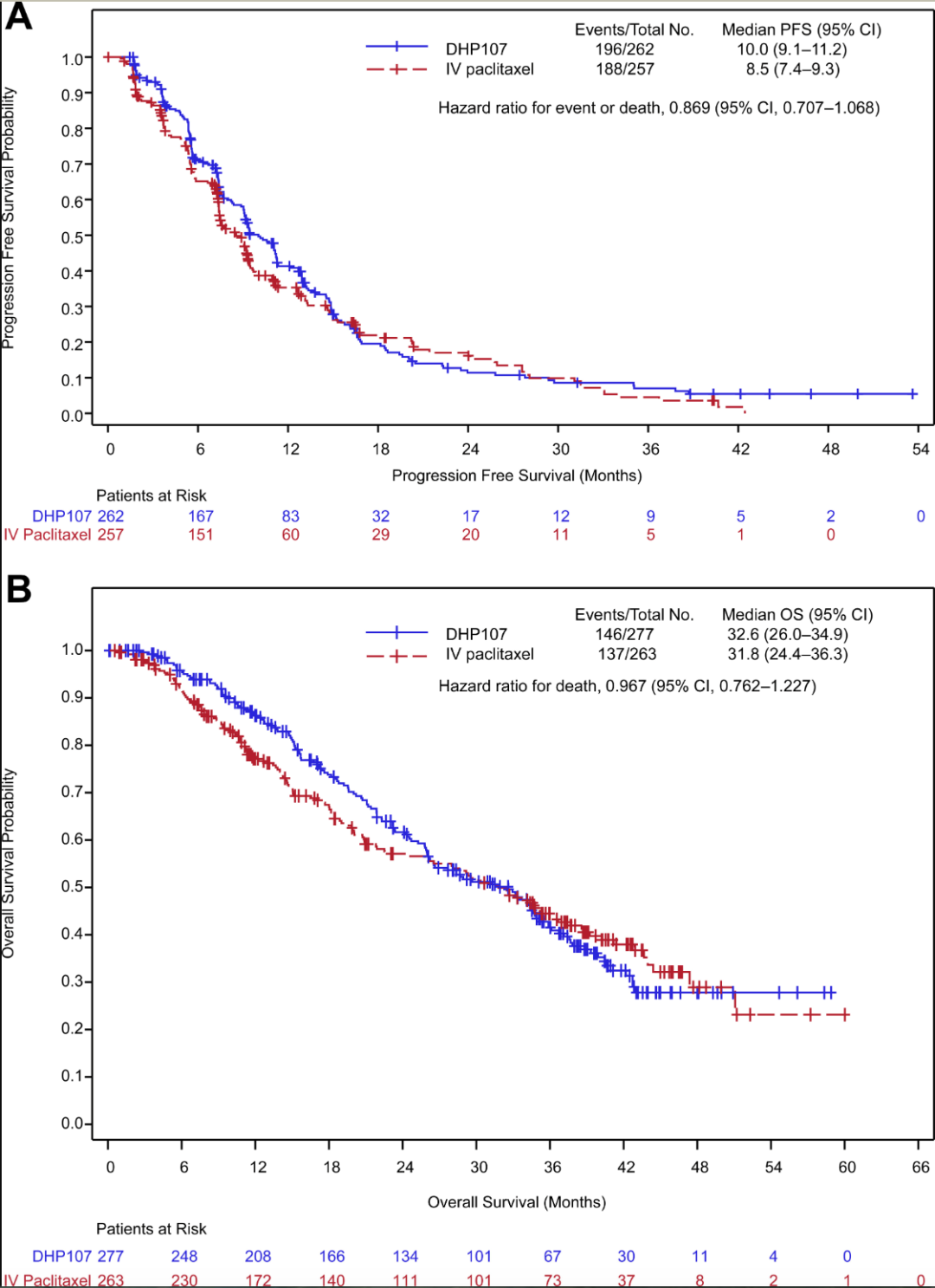
图1 DHP107组和静脉组PFS和OS疗效对比[1]
安全性方面,DHP107呈现出与静脉紫杉醇不同的毒性谱。口服组中性粒细胞减少(81.6% vs 59.3%)、

医脉通:近年来,给药方式的创新和诊疗管理模式的持续优化,让日间化疗成为可能,而口服化疗药物的出现则进一步拓展了治疗场景。从临床实践的角度来看,OPTIMAL 研究结果将会给乳腺癌患者的治疗模式带来怎样的变化?它又将为临床实践带来哪些新的启发?
孙涛 教授
辽宁省肿瘤医院
OPTIMAL 研究是全球首个在乳腺癌领域证实口服紫杉醇非劣于静脉紫杉醇的III期研究,其结果填补了口服紫杉醇在乳腺癌治疗中的证据空白。DHP107无需静脉输注和抗过敏预处理、居家就可接受抗肿瘤治疗,极大地提升了患者用药便利性。对于需要长期维持治疗的人群,以及医疗资源相对不足地区或行动受限的患者而言,这一转变尤具现实价值,有望在减轻治疗负担的同时进一步改善生活质量。此外,给药路径的转变有效降低了患者的住院频次,有助于降低医疗服务压力及护理成本,具有一定的潜在药物经济学优势。
事实上,近年来随着口服化疗药物的不断发展,乳腺癌治疗模式正逐步由“医院中心化”向更加灵活的治疗场景延伸。然而作为乳腺癌治疗基石药物之一的紫杉醇,受限于制剂工艺及递送技术,长期以来缺乏成熟的口服方案。DHP107的问世在一定程度上打破了这一技术壁垒,使紫杉醇这一经典药物得以以新的给药形式融入临床实践。
目前,DHP107已在韩国和中国获批上市,随着其临床应用经验的不断积累及循证证据的持续完善,未来有望在更广泛人群中推广应用。从“给药方式的改变”到“治疗模式的重塑”,口服紫杉醇的发展或将成为推动乳腺癌化疗格局演进的重要一环。

医脉通:随着乳腺癌诊疗模式日渐精准化,临床决策维度也变得更加复杂:从患者分层、治疗方案选择再到疗效与安全性的平衡,每个环节都可能存在不同的挑战。医脉通特此打造《话题》栏目,邀请行业专家围绕临床实践中的争议与困惑展开深度研讨。能否请您结合临床经验,分享三个您认为当前乳腺癌领域值得深入讨论的临床话题?
孙涛 教授
辽宁省肿瘤医院
治疗手段的日益丰富,在拓展临床选择空间的同时,也显著提升了决策的复杂度——从人群分层到方案取舍,再到疗效与安全性的动态平衡,每一环节均需更加精细的判断。
话题一:口服化疗浪潮下,如何构建“居家抗肿瘤治疗”的安全网与疗效保障体系?
以OPTIMAL研究为代表的循证证据表明,口服紫杉醇已具备与静脉制剂相当的疗效,这一进展也正在推动着化疗从传统的医院场景向家庭场景延伸。然而,治疗场景的转移也带来新的管理挑战:其一,患者依从性与用药规范难以实时监控;其二,骨髓抑制、胃肠道毒性等不良事件在院外的识别与干预存在滞后;其三,严重不良事件发生时的责任界定及应对路径尚不清晰。如何构建覆盖“医院—社区—家庭”的连续管理体系,并借助数字化工具实现毒性预警与分级干预,将成为口服抗肿瘤治疗规范化应用的关键。
话题二:HER2低表达提出后,晚期乳腺癌的治疗路径是否需要重新审视?
随着ADC药物的突破性进展,“HER2低表达”逐渐从单纯的检测现象转变为具有明确治疗指向的生物学分层,但这一变化也对既有治疗框架提出了挑战。首先,HER2低表达的判读一致性仍有待提升,不同中心间的检测差异可能直接影响患者的治疗机会。其次,对于内分泌耐药的HR阳性/HER2低表达晚期乳腺癌患者,ADC的介入时机及其与标准化疗的序贯次序仍有待高等级证据支持;三阴性乳腺癌中,当HER2低表达与PD-L1阳性并存时,免疫治疗与ADC之间的优先选择策略同样存在不确定性。而随着ADC药物的广泛应用,其进展后的治疗策略亦成为新的临床难点:HER2低表达状态是否会在治疗过程中发生动态改变,是否需要重复活检以指导后续决策,均有待更多证据加以明确。因此,如何将HER2低表达作为动态变化的生物标志物,融入个体化的全程治疗决策,仍是当前亟需厘清的核心问题。
话题三:早期乳腺癌新辅助治疗后non-pCR患者的“降阶梯”与“升阶梯”博弈——我们是否在过度治疗?
基于既往研究结果,针对non-pCR患者实施术后强化辅助治疗已逐步成为临床共识,但在实际应用中仍存在诸多争议。一方面,对于残留病灶负荷较低的患者,是否需要完全沿用强化方案,抑或可依据RCB分级进行个体化降阶梯治疗,尚缺乏清晰界定;另一方面,部分患者因耐受性的限制难以完成足量治疗,其剂量调整后的真实获益仍有待进一步验证。与此同时,ctDNA/MRD检测为风险分层提供了新的可能,但其在指导治疗强度调整中的证据尚未成熟,如何避免技术应用先于证据落地,亦需审慎权衡。归根结底,如何在“避免漏治高危人群”与“减少不必要毒性暴露”之间取得平衡,并在疗效获益与生活质量之间实现更为理性的取舍,是这一领域持续需要面对的关键命题。
总体而言,所有治疗策略的优化与路径的重构,仍应回归患者本身,以实现长期生存获益与生活质量提升的协同改善为总体目标。未来,我们仍需在循证证据与临床实践的持续交汇中,不断推动医学认知向更深处延展,让技术的进步真正沉淀为患者可感知的改变与希望。
孙涛 教授
辽宁省肿瘤医院孙涛教授
辽宁省肿瘤医院乳腺内科主任、博导
国务院特殊津贴专家、二级教授
辽宁青年名医、“兴辽”领军人才
中国抗癌协会肿瘤标志物专委会 副主委
中国抗癌协会肿瘤异质性与个体化治疗专委会 副主委
中国抗癌协会肿瘤靶向治疗专委会 常委
中国抗癌协会多发和不明原发肿瘤专委会 常委
中国抗癌协会乳腺癌专委会 委员
中国临床肿瘤学会(CSCO)肿瘤心脏病学专委会 副主委
中国临床肿瘤学会(CSCO)乳腺癌专委会 常委
中国医药教育协会乳腺疾病专委会 副主委
中国研究型医院精准医学与肿瘤MDT专委会 副主委
辽宁省抗癌协会化疗专委会 主任委员
辽宁省药学会抗肿瘤药物专委会 主任委员
辽宁省药学会药物临床评价研究专委会 副主委
参考文献:
[1]Xu B, Jeong H, Sun T, et al. OPTIMAL: A Multinational Phase III Study of Oral Paclitaxel (DHP107) versus Intravenous Weekly Paclitaxel in HER2-Negative Recurrent or Metastatic Breast Cancer. Ann Oncol. Published online March 13, 2026.
编辑:Ocean
审校:孙涛教授
排版:Ben
执行:Ocean
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。