编译:昆明医科大学附属昭通医院甲状腺乳腺外科 刘为民 蒋睿
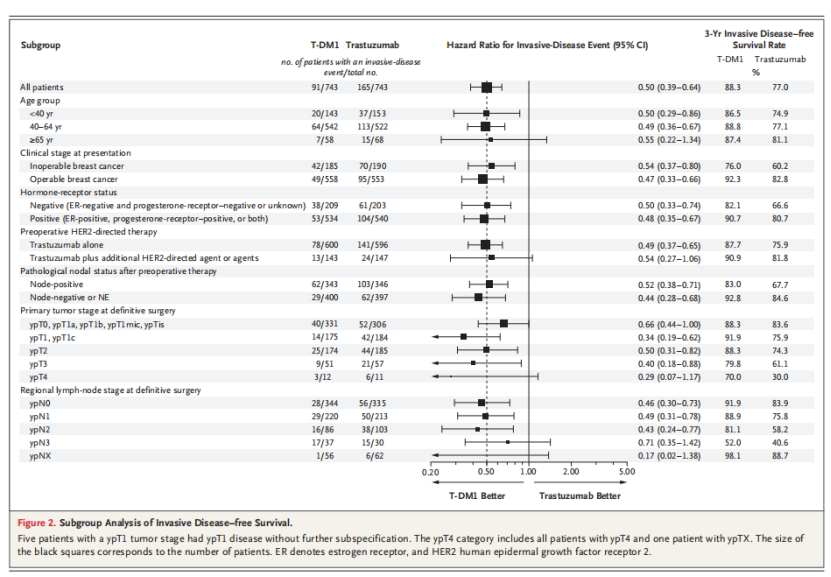
为了追踪学术前沿,更好地服务甲状腺乳腺疾病患者,本人特意订阅了一些国际权威学术杂志,包括:Thyroid、clinical thyroidology等。其中电子版Medscape时效性最佳。每周该平台把国际最新进展发到我的邮箱之中。鉴于我们科室肩负着区域医疗中心的职责,我们甲状腺乳腺团队会把相关部分重要内容编译成中文,经整理加工后分享到昭通地区乃至毕节六盘水地区同行中,其一完成履行政府交付的行政职责,更重要的是希望同行能够尽快获得最新知识,让我们的病人活的再久一点,生活质量再高一点。本篇文章是2025年ESMO年会上英国伦敦皇家自由医院巴尼特医院MRCP肿瘤内科顾问医师和美国宾夕法尼亚州匹兹堡市匹兹堡大学医学中心NSABP 基金会(美国乳腺与肠道外科辅助治疗研究组)希尔曼癌症中心恶性血液病与肿瘤内科查尔斯・盖耶主任医学博士的谈话记录,内容是——HER2 阳性早期乳腺癌:最新研究数据对临床实践的指导意义此间得到昆明医科大学延安医院肿瘤中心丁万宝教授的指导在此表示衷心感谢!未尽事宜和有争议之处敬请同行批评指正并交流。朱迪・金哲学博士,英国伦敦皇家自由医院巴尼特医院MRCP肿瘤内科顾问医师查尔斯・盖耶医学博士,内科学教授 美国宾夕法尼亚州匹兹堡市匹兹堡大学医学中心NSABP 基金会(美国乳腺与肠道外科辅助治疗研究组)希尔曼癌症中心恶性血液病与肿瘤内科主任大家好,欢迎收看本次专题节目——《HER2 阳性早期乳腺癌:最新研究数据对临床实践的指导意义》。我是朱迪・金,来自英国伦敦皇家自由医院,肿瘤内科顾问医师。今天与我共同主持的是查尔斯・盖耶教授,他来自美国匹兹堡大学医学中心,担任内科学教授。欢迎您,查尔斯。那么我们正式开始。首先简要介绍一下HER2 阳性早期乳腺癌患者的当前诊疗策略。众所周知,根据现行ESMO 指南,总体而言,治疗策略主要分为两类:一是先行手术治疗,再行辅助治疗;二是采用新辅助治疗。对于绝大多数患者而言,如果肿瘤直径小于2 厘米,即 T1 期肿瘤,通常先进行手术,随后接受辅助化疗联合抗 HER2 单抗治疗。而对于肿瘤较大(T2 期及以上)或存在淋巴结转移的患者,则通常推荐先采用化疗联合抗 HER2 靶向单抗进行新辅助治疗。但我认为,当我们考虑未能满足这类患者的临床需求时,大概可以将其归结为两个方面。2期及以上这一群体范围非常宽泛,举例来说:同样是T2及以上,一枚2.2cm,淋巴结阴性的肿瘤,与一枚6 cm、累及4~5枚淋巴结的肿瘤,差异极大。因此,明确何时升级治疗、何时降阶梯治疗,是一个非常值得探讨的重要课题。基于以上考虑,我们先来探讨辅助治疗阶段的相关内容。众所周知,新辅助治疗后,未获得病理完全缓解的患者,其复发风险更高。那么Charles,我们来谈谈 DESTINY-Breast05 研究的最新数据,并将其与当前标准治疗方案 ——KATHERINE研究所采用的T-DM1进行对比。好的!提醒大家一下:KATHERINE 研究是我们早在2018年于圣安东尼奥乳腺癌研讨会(SABCS) 上公布结果的一项研究,研究确实改变了新辅助治疗领域的临床标准方案,也就是刚刚 Judy 所描述的、针对T2期或淋巴结阳性患者的治疗策略。该研究中,我们将未获得病理完全缓解、且入组时肿瘤分期至少为T1c N0的患者进行随机分组。我们排除了T1a、T1b期患者。简言之,研究纳入了范围较广、存在残存病灶、未达到病理完全缓解的患者,一组接受当时的标准方案曲妥珠单抗,另一组则接受T-DM1治疗。DESTINY-Breast 05 是 KATHERINE 的一项随访/后续验证研究,其研究设计基本相同,但入组人群更聚焦:即我们最初公布 KATHERINE 研究时,3 年随访中已显示风险高于理想水平的患者—— 也就是存在未被满足临床需求的人群,包括肿瘤较大或术后淋巴结阳性的患者。我们当时确实重点关注这一群体。这也是两项研究入组标准不同的原因。大家应将 DB-05 视为 KATHERINE 的后续研究,旨在解决 KATHERINE 研究中尚未满足的临床需求。我认为,观察3 年无侵袭性疾病生存率(iDFS)的森林图是很有意义的。因为你可以很快明白,我们为什么会选择初诊时为不可手术病灶,或术后淋巴结阳性的患者。这些患者的复发率当时已接近或超过 20%。所以,这就是我们重点关注的人群 ——存在未被满足临床需求的人群。当我们获得7 年随访数据时——也就是KATHERINE研究的成熟随访数据,我们非常欣慰地看到无侵袭性疾病生存率(iDFS)得到显著改善。50%的风险降低这一获益一直稳定维持到第7年。我们观察到了生存获益。我确实认为,在解读DESTINY-Breast 05 研究数据时,参考 KATHERINE 研究的长期数据、观察患者接受 TDM1 治疗后 7 年(而非3年)的表现是很有意义的,因为这更能真实反映患者的远期预后。而且我认为,这正是大家应该关注的重点。从表格中(谈话原文没有给出表格)可以看到,即便那些未被纳入DB-05研究的患者亚组,在我看来仍然存在一定的未被满足的临床需求。那么,在我们所选择的这一高危人群中,DESTINY‑Breast05 研究观察到了什么结果?这部分人群在 3 年时就已明确存在未被满足的临床需求。令人非常欣慰的是,研究观察到风险比0.47;3年无侵袭性疾病生存率(iDFS)从83.7% 提升至92.4%,获得显著改善。次要研究终点——无远处复发间期(DRFI)也表现出极为强劲的获益。这是因为大部分复发事件均为远处转移,并且我们观察到早期信号提示,T-DXd 或许能够对脑转移这一问题产生影响,而这是我们在KATHERINE 研究中未曾观察到的。生存获益也呈现出积极的趋势。当你再次查看森林图时,会非常欣慰地看到,试验中所有亚组均观察到一致的获益。而且我认为,当你观察各个患者亚组时,会发现许多有意义的数据,这些数据有助你为个体患者提供咨询建议。当年我在欧洲肿瘤内科学会(ESMO)上报告这项研究时,有一项数据是我们当时未能提供的,那就是HER2 2+ 与3+ 患者的疗效对比情况。在 KATHERINE 研究中我们观察到,从预后角度来看,HER2 2+ 这部分患者最初的表现似乎比3+ 患者略好一些;但随着 T-DM1 治疗随访时间的延长,她们最终的复发率达到了 30%。而我们从 DB-05研究中可以看到,相较于T-DM1,HER2 2+ 患者从 T-DXd 治疗中获得的获益尤为显著。当然,T-DXd 用于早期乳腺癌治疗时,最需要注意的安全问题间质性肺病(ILD)。我们知道高危患者需要进行放射治疗,因此我们设置了动态CT监测,采用低剂量非增强CT,力求早期识别ILD,以便及时停药,避免患者出现严重的毒副反应。这是我们报道的T-DXd 总体相关数据,间质性肺病(ILD)总发生率为9.6%。所幸的是,8.5%的患者为1级或2级。研究中确实出现了2例死亡病例,也有3级不良事件。最初我们对此并没有太多详细数据。Loibl 医生在圣安东尼奥乳腺癌会议上报道,中位发生时间为74天,范围46~106天。一旦发生,需要较长时间才能缓解。因此,在早期乳腺癌中应用该药时,这一重要问题必须牢记于心。没错!正因为如此,我认为本研究非常出色。我想,这就是我们大家一直都在期待、极具影响力的重磅研究之一。我确实认为这项研究会改变我们的临床实践。我完全理解你所说的,希望看到这个时间点之后的长期随访数据。但我认为,这是一个高危人群,我们知道,即便使用T-DM1,对于未达到病理完全缓解(non-path CR)的患者,仍然有部分人预后不佳。所以,这对这类患者而言,确实是备选治疗方案中一个非常重要的选择。不过也存在一些问题,包括每6周一次CT检查、间质性肺病(ILD)风险,在稍后几分钟我们会在DB-11研究部分讨论这一问题。但我想问的是,你觉得在临床实际开展/落地方面会不会存在问题?我想,如果患者接受了新辅助治疗但未获得病理完全缓解,这对他们来说是一个非常好的选择,但你觉得在实施层面会有问题吗?是的!我认为在常规临床实践中开展系列扫描监测,无疑会是一大挑战。因为我们需要放射科安排检查——这通常是诊断性 CT,要求扫描整个胸腔,但重点关注肺部、排查ILD,同时要低剂量、不打增强。所以,在沟通检查目的、判读标准、观察重点这几方面都会存在困难。我本人已经和本院放射科沟通过,也深入了解了现代诊断科室运作的细节。很多工作其实和检查项目编码直接挂钩,不是我们口头说怎么做就行,关键在编码。因此,我认为各家医院必须与放射科合作,制定一个专用编码,明确这项检查怎么做、如何读片,否则真的会造成混乱。此外,这类检查还需要快速预约安排,毕竟要每 6 周、9 周或 12 周做一次,预约落实本身就会很有难度。所以这确实会是个问题。还有一件事需要注意。当然,这也并非唯一的治疗选择。而且我们已经观察到,随着T-DXd治疗周期数的增加ILD风险会同步升高。接下来我们再来看看2025年ESMO年会同期公布的另一项临床试验 ——该研究将 T-DXd 用于新辅助治疗阶段。这就是DESTINY-Breast11 研究。简单来说,该研究共设有3个试验组。其中单用 TDXd 组已终止入组,因此研究最终实际为2个组。一组采用标准剂量密集型蒽环类方案,序贯紫杉类药物联合双靶点HER2 单抗治疗;另一组则是用4个周期T-DXd替代蒽环类药物,后续同样序贯紫杉类联合双靶点HER2单抗治疗。研究主要终点为病理完全缓解(pCR),次要终点则包含了所有常规预设的相关指标。因此,我认为所有人都对这项数据印象极为深刻——在意向治疗人群(ITT人群)中,病理完全缓解(pCR)率的绝对提升值(delta值)超过了11%。此外,当我们针对那些化疗敏感性极高的患者,按雌激素受体(ER)阳性与ER阴性进行分层分析时发现:其中ER阴性亚组的pCR率绝对提升值达到了16%,且该亚组最终实现了83%的pCR率——这是迄今为止临床试验中记录到的最高病理完全缓解率。其他一些次要终点数据,例如无事件生存期(EFS)等,目前尚不成熟,但当前趋势已非常令人鼓舞。这一点很有意思,因为仅仅只需4 个周期的治疗。而且从毒性反应方面来看,其结果与蒽环类方案非常、非常接近。这项研究引发了大量讨论。很多临床医生并不使用含蒽环类的方案,他们更倾向于采用紫杉类联合卡铂这类方案。此外,对于无效患者该如何处理这一问题,目前也存在争议。无人知晓这些未达到pCR 的患者我们后续该怎么办。查尔斯,我一直和同行们在讨论这个问题,我也想了解一下您那边的临床经验是怎样的。我发现目前的观点分歧很大。一部分人认为:应该尽早使用T-DXd,即在新辅助阶段就给予4个周期治疗即可。只要获得病理完全缓解(pCR),术后辅助阶段就无需再过度担心。而另一部分人则主张:仍按照标准方案治疗,仅对新辅助治疗后未达到 pCR 的患者,再选用T-DXd 进行后续治疗。观点确实存在分歧。其实,这两项研究的结果都算不上意外。在这些研究设计之初,大家就预期它们均会达到主要终点。毕竟这款药物在晚期/ 转移性疾病中已经展现出非常强劲的疗效,所以能看到这样的结果,一点也不奇怪。在我看来,关键在于这项研究的初衷究竟是什么?要知道,DESTINY-Breast05 研究的目的,就是明确回答这个问题:在我们目前面临的最高危患者中,该药的疗效究竟如何。我们已经明确,无论患者分型如何,该药在高危人群中,对早期无浸润性疾病生存期(iDFS)均能产生显著改善。DB-11 研究告诉我们:如果采用该方案,我们可以用T-DXd 替代AC方案,并能将pCR 率提升至非常可观的水平。无事件生存期(EFS)数据呈现出积极的获益趋势,这一点令人鼓舞。但我们也知道,辅助治疗对最终预后有着重大影响,因此我尚不确定该如何解读这项研究的长期数据——该研究对EFS这一终点的统计效能并不充足。不过,后续结果依然值得我们关注。在我看来,这项研究真正关键、且值得一提的另一点是:它确实显示出ILD(间质性肺病)发生率更低,这一点也在意料之中。一组是4 个周期,另一组是14个周期,ILD发生率几乎只有原来的一半。而且从我们之前的DB-05研究中也可以看到,出现ILD的中位时间大约是4个月。因此,所有数据都是高度一致、相互印证的。但我认为,正如你所提到的,难点在于:对于未达到pCR 的患者,我们该如何处理?而且,我们是否会有研究数据来指导下一步该怎么做?就我个人而言,我一直在思考:如果我用了4个周期 T-DXd,而某位患者影像学提示肿瘤明显退缩,但4个周期下来并未达到pCR,那我是否需要继续追加治疗,把周期数从4周期补足到14周期?如果肿瘤就停在那个状态不再退缩,那治疗还有什么意义?但除此之外,我们又能怎么办呢?所以我认为这其中存在很大的挑战。这套方案对于达到pCR 的患者效果非常好,但对于未达到 pCR 的患者,仍存在诸多疑问。我不太担心对照组的结果。确实,现在很多临床医生已经不再使用蒽环类方案,但我认为 TCHP 方案与 AC-THP 方案的疗效结局非常接近。因此我认为可以接受、也能够合理推断该对照组的结果。我个人没有(顾虑)。我同意。我认为两者差异不大。可以预见,其获益程度也会是相似的。我的意思是,我认为在同一场会议中,我们也看到了一些来自降阶梯临床试验的数据。这些研究未必针对的是高危人群,而是更多聚焦于Ⅱ 期患者这类人群。我们看到了NEO-CARP研究,其结果提示:我们或许可以对化疗进行降阶梯——不使用TCHP方案,而仅采用紫杉类药物联合HP(曲妥珠单抗+帕妥珠单抗) 方案。因此,与我交流过的一些临床医生提出,或许可以采用一种更基于疗效应答的个体化方案。我们能否先采用标准的紫杉类药物联合HER2 双靶向抗体治疗?对于 4 个周期后疗效不佳、无明显应答的患者,在此时再强化升级治疗。但我必须说明,在英国及其他一些国家,从医保报销政策来看,有些国家严格按照临床试验方案原文执行,只能采用研究中允许的用药顺序。而另一些国家则更为灵活。那么您认为,这种思路是否值得临床关注与探索?我想说的是,在美国,我们确实就是这么做的。这也正是后续临床试验设计会跟进、借鉴的方向。另外我想说,关于降阶梯治疗:我们在ASCO上看到的是降阶梯的主题,而到了ESMO,则更多是升阶梯的主题。所以大体就是这样。而且我认为,把THP方案提前到一线使用是合理的。我们看到,它能让很多患者达到理想的治疗效果。我认为,最终我们会走向降阶梯治疗,这才是这类患者的管理方向。我认为我真正的收获是,和很多人交流之后发现:有些人绝对更倾向于DB-05方案,另一些人则明显更支持 DB-11 方案。在我看来,这两种都是非常好的选择,而且正如你所说,两者本身并没有绝对的对错之分。所以,其实只是存在两条可行的治疗路径,都能很好地服务患者。单就这一点而言,对我们整个领域来说就是一个积极的结果。但就像你提到的,关于治疗降级这个问题,我们不可能一边升级治疗、一边又做降级。因此,真正把 “哪些患者能从中获益” 区分清楚,依然是最棘手的部分。同样重要的是,我们要意识到这并非该领域唯一的药物。目前还有多项关于抗体药物偶联物(ADC)在辅助治疗与新辅助治疗领域的临床研究正在开展。因此,我们期待未来几年能看到这些研究的结果公布。查尔斯,非常感谢你抽出时间参与这场精彩的讨论。也感谢各位观众的收看与参与。请大家继续完成节目末尾的答题环节。非常感谢各位。
刘为民
昆明医科大学附属昭通医院甲状腺乳腺外科 副主任医师
外科学博士
欧洲疝学会中国会员
美国甲状腺学会会员
广东省中西医结合微创外科分会常委
发表论文19篇 其中SCI三篇
丁万宝
昆明市延安医院肿瘤科副主任医师,硕士生导师
昆明市医学科技学科带头人
昆明市肿瘤放射治疗医学技术中心 负责人
昆明市肿瘤疾病诊疗质量控制中心 负责人
中国抗癌协会肿瘤微创治疗专业委员会粒子分会 委员
中国抗癌协会肿瘤组织间植入治疗专委会 委员
中国医药教育协会肿瘤内照射医学专业委员会 委员
中国医师协会放疗专委会转移癌学组 委员
中国抗癌协会肿瘤消融治疗专业委员会 委员
中华医学会放射肿瘤治疗分会骨与软组织肿瘤学组 委员
云南省抗癌协会第七届理事会 理事
云南省抗癌协会第二届肿瘤消融治疗专业委员会 主任委员
云南省转化医学学会肿瘤精准放疗专业委员会 副主任委员
云南省抗癌协会肿瘤MDT专业委员会 副主任委员
云南省医院协会肿瘤医学专委会 副主任委员
云南省医师协会第三届肿瘤转化医师分会 副主任委员
云南省健康管理促进会肿瘤与危重症专业委员会 副主任委员
云南省医学会介入学分会消融学组 副组长
云南省医学会肿瘤放射治疗专委会 常委
西部放射治疗协会胸部肿瘤诊疗分会 常委
云南省抗癌协会整合肿瘤学专委会 常委
擅长肿瘤放疗、肿瘤消融治疗及I125粒子植入治疗。主持省级、厅局级课题10项,SCI收录论文8篇
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)