近几十年来,我们对双相障碍(BD)遗传学及神经生物学的认识不断拓展。来自遗传学、神经影像、炎症紊乱及环境因素研究的发现共同支持一种模型,即双相障碍是一组多因素所致的疾病,并经常共病其他疾病,因而需要复杂的治疗策略。
双相障碍是一类慢性

双相障碍的全球患病率约为2%,且在很大程度上与社会人口学因素无关。双相 I 型在两性中的发病率大致相当,但双相 II 型及其他双相障碍谱系疾病(如环性心境)在女性中更为常见。双相 II 型患者中,首次发作为抑郁发作的比例约为轻躁狂的10倍,而约半数双相 I 型患者的首发症状为抑郁。双相 I 型中,发病年龄较任何单一病程模式更能稳定地预测转归。
药物治疗和社会心理治疗可以有效改善双相障碍急性心境发作的严重程度及降低发作频率,但在发作间期,功能损害仍持续存在。此外,即便接受了有效的治疗,双相障碍患者仍存在过早死亡的现象。相较于一般人群,双相障碍患者死于
约三分之一的双相障碍患者被误诊长达10年,这一时长也对应患者未能确诊的平均时间。环境因素,如社会污名、医疗系统的实际情况、专业医师的可及性,以及双相障碍自身临床表现的变异性,均会导致该病迟迟难以被识别(表1)。这种延迟与更差的临床结局、功能结局及经济结局相关,而未治疗的心境发作所累积的负担则与难治性相关。
表1 双相障碍的常见鉴别诊断
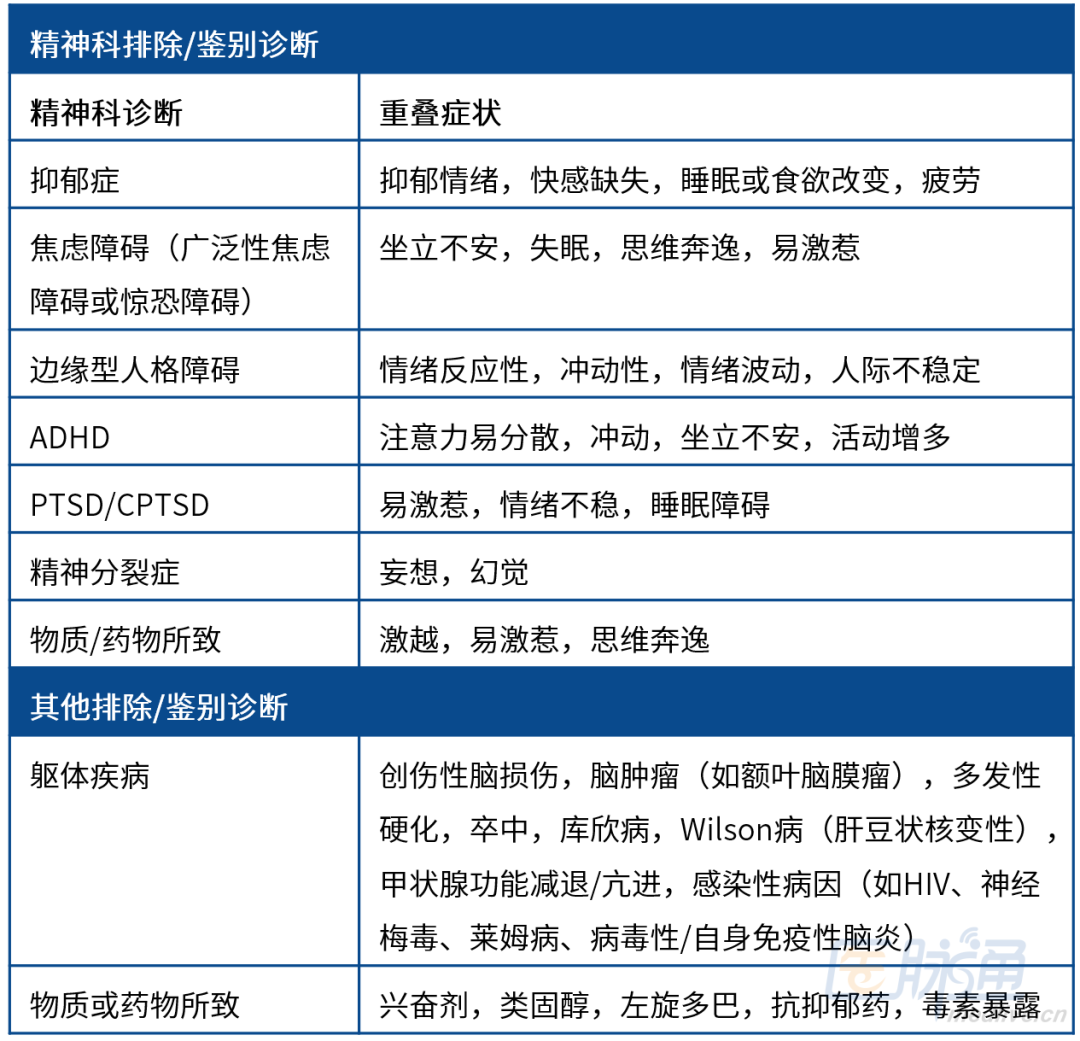
双相障碍常共病其他精神障碍,且病程模式多变,致使准确诊断和有效管理更加困难(表2)。系统性的筛查和评估工具可以帮助临床医生更精准地进行鉴别诊断,但这些方法至多仅得到了缺乏一致性的应用。
表2 双相障碍的常见精神科共病
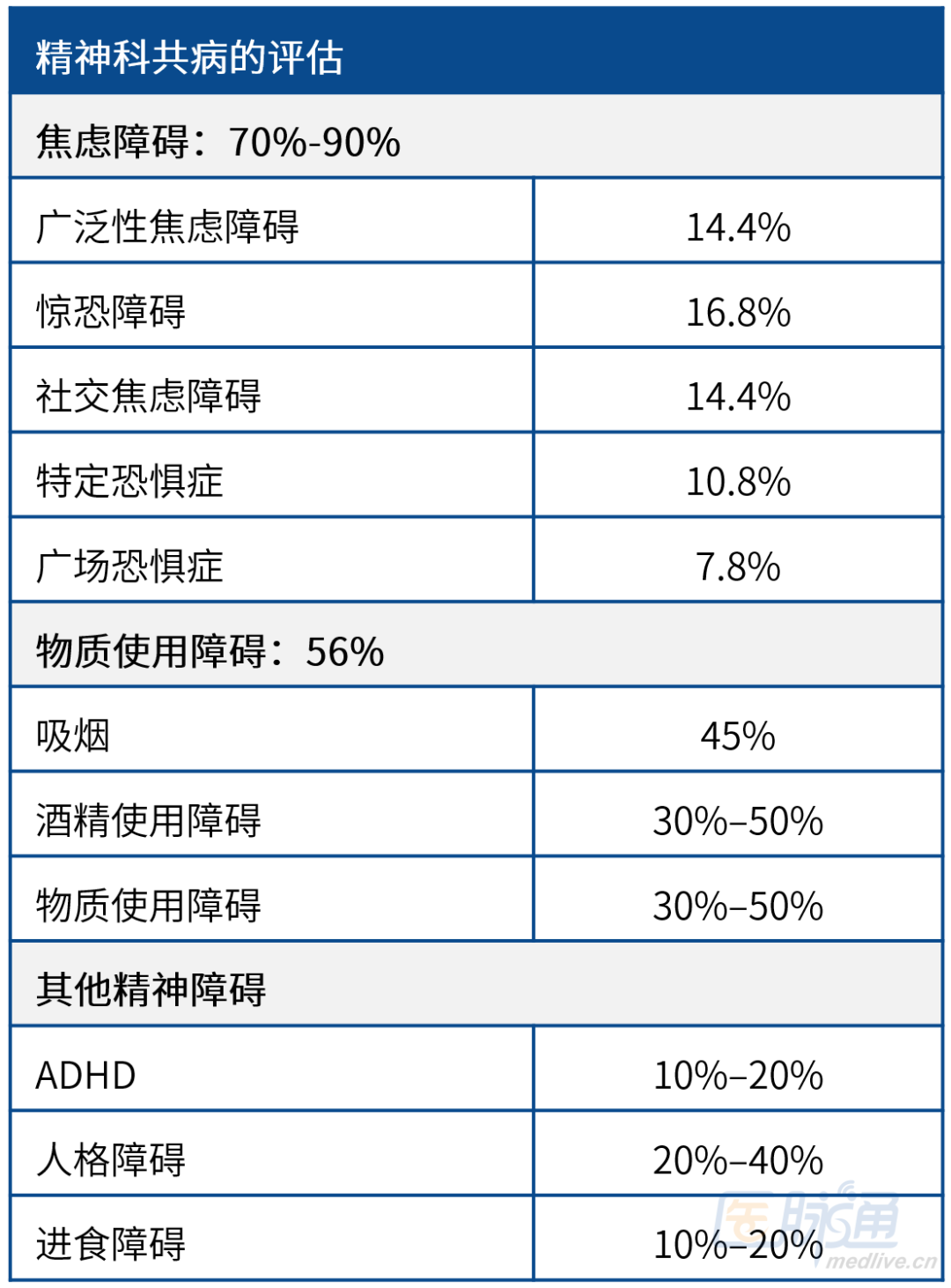
遗传学研究
家系研究、双生子研究及寄养子研究估计,双相障碍的遗传率为60%-85%。双生子meta分析显示,同卵双生子的双相障碍共病率约为40%-70%,异卵双生子为5%-10%;这一发现既支持了遗传的显著作用,也提示有大量非共享环境因素在发挥作用。现代基因组学研究提示一种复杂的多基因模式,即大量微效变异共同影响双相障碍的易患性。近年来开展的多族裔全基因组关联研究(GWASs)则发现,不同族裔间能够重复验证的全基因组位点数量显著增加;这些位点富集在钙信号通路、突触传递以及神经发育通路等方面。
双相障碍与
系统生物学
高通量转录组学、蛋白质组学、代谢组学和表观基因组学方法可捕捉DNA序列本身无法揭示的动态、状态依赖性变化及治疗效应。来自外周血及尸检脑组织研究的转录组学及RNA生物标志物结果均发现,昼夜节律、免疫炎症反应、能量代谢及突触功能相关基因存在紊乱现象;躁狂状态下细胞因子通路呈状态依赖性改变,而在缓解期部分恢复正常。对患者来源类器官开展的RNA测序分析显示,突触基因表达下调,同时免疫通路表达上调;线粒体功能障碍与锂盐治疗反应存在相关性。蛋白质组学分析结果与上述代谢及炎症主题一致,包括补体级联反应、脂质代谢以及MAPK、PI3K‑Akt、JAK‑STAT等信号转导通路。代谢组学研究揭示
多组学整合将遗传学、转录组学、表观遗传学和蛋白质组学数据统一整合,形成可在通路水平上进行检验的假说。例如,GWAS后分析富集了涉及突触功能、钙信号和
机制领域
遗传风险除能量代谢及炎症‑免疫信号通路失调外,还汇聚于脑网络组织,可能参与心境的发作性波动及极性转换。然而,其因果关系、相关性与继发改变之间的界线尚不明确。
昼夜节律与生物钟系统
临床及前临床证据表明,双相障碍患者存在生物钟基因功能改变、睡眠‑觉醒紊乱及光敏感性异常。不规律的睡眠‑觉醒模式、紊乱的社会节律及晚间时型与复发风险、快速循环及混合特征相关。昼夜节律紊乱有时先于心境发作出现。睡眠‑觉醒时相变化可带来心境症状的短期改善。
线粒体与能量代谢
双相障碍患者的线粒体功能障碍表现为电子传递链活性降低、氧化应激增强及三羧酸循环中间产物紊乱,并与情绪不稳和认知损害相关。在临床层面,锂盐和丙戊酸盐可调节线粒体膜电位并减轻氧化应激;其中,锂盐可特异性改善锂盐治疗有效者的线粒体指标及细胞活力。
钙信号、突触可塑性及细胞兴奋性
钙通道基因,尤其是CACNA1C和CACNB2,是双相障碍显著的风险位点,其变异预计可改变兴奋性神经元中L型钙通道的功能。钙信号异常与线粒体功能障碍及突触可塑性相互关联。未用药患者中,血小板和淋巴细胞的基础游离细胞内钙水平升高29%,对刺激的钙反应升高25%。锂盐和丙戊酸盐可调节细胞内钙水平,提示其心境稳定效应可能反映了钙依赖性可塑性的正常化。
HPA轴、炎症及应激‑免疫相互作用
抑郁发作或混合发作期间,下丘脑‑垂体‑肾上腺(HPA)轴发生改变,包括基础皮质醇升高、昼夜下降减弱以及夜间皮质醇升高;双相障碍与HPA轴失调相关。HPA轴过度活跃可促进免疫激活,因为促炎性细胞因子会降低
研究表明,与神经可塑性、昼夜节律调节及免疫通路相关的信使RNA及非编码转录本存在改变,其中部分改变在
网络层面的大脑变化
机制模型
去同步级联模型(Desynchrony cascade model,图1左)将多基因风险(富集于突触、钙通道及昼夜节律相关基因)定位为导致生物节律去同步化的易感因素,该去同步化继而通过下丘脑‑垂体‑肾上腺轴‑免疫、线粒体‑能量及大脑网络通路进行传播。该模型起始于昼夜节律紊乱(如晚间时型、褪黑素分泌延迟、皮质醇曲线平坦化),后者可能作为更广泛节律失调的早期启动因素;而线粒体功能障碍则作为昼夜节律紊乱的放大器,其作用机制可能涉及电压门控钙通道亚基α1C(CACNA1C)的失调,进而导致线粒体相关膜处细胞内钙负荷过度增加,并引发后续的内质网应激。这些细胞水平的扰动可激活免疫‑炎症轴(表现为前额叶‑边缘区域IL‑6水平升高及小胶质细胞激活);应激反应性非编码RNA则可稳定或破坏突触程序,例如锂盐治疗有效者中线粒体RNAlet‑7家族表达下调即为此类调控的例证,凸显了RNA调控与治疗反应之间的关联。在宏观层面,上述依次发生的分子级联反应可改变大脑网络模式,导致默认模式网络与突显网络过度连接,以及前额叶活动低下,这与临床上观察到的双相障碍患者情感不稳及认知控制受损现象一致。该多节点通路得到如下证据支持:锂盐的治疗效应很可能靶向钙稳态、线粒体活性、时钟基因表达及炎症通路。该模型的主要缺陷在于其所假设的事件发生顺序——该顺序系基于已发表的横断面研究推断得出,而非直接观察所得。
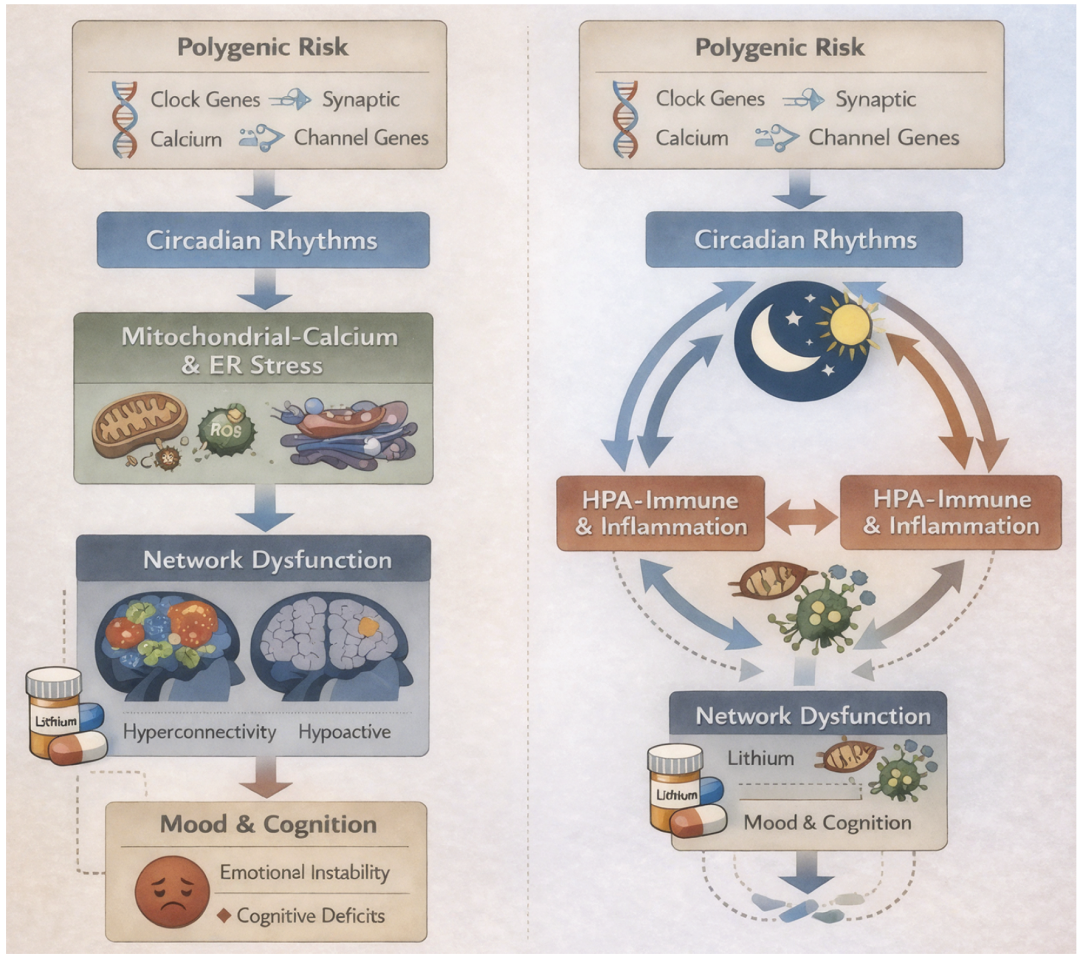
图1 去同步级联模型(左)和枢纽模型(右)
另一种模型,即枢纽模型(Nexus model,图1右),强调昼夜节律、线粒体‑钙及下丘脑垂体‑肾上腺轴‑免疫系统之间的双向环路,其中任一节点的扰动均会以相互反馈的方式传播。例如,环境应激源与遗传易感性共同作用可改变昼夜节律,进而影响线粒体功能与钙稳态,最终可能导致下丘脑‑垂体肾上腺轴敏感性升高。以双向方式,过度激活的下丘脑‑垂体‑肾上腺轴功能又可反过来影响昼夜节律及线粒体能量生成,从而调节免疫转运与昼夜节律,并使炎性细胞因子破坏时钟基因表达。昼夜节律钟与线粒体在分子水平上存在动态关联。CLOCK/BMAL1调控氧化磷酸化与线粒体动力学;而线粒体活性氧与钙反馈则可同步外周振荡器,2型糖尿病即为该类关联性的佐证。下丘脑‑垂体‑肾上腺轴‑免疫轴与昼夜节律轴呈相互耦合关系:糖皮质激素削弱昼夜节律并调节免疫转运;而炎性信号(如IL‑6)则破坏时钟基因表达及视交叉上核输出。线粒体功能障碍是连接这些环路的关键环节:下丘脑‑垂体‑肾上腺轴来源的糖皮质激素可通过线粒体相关膜与内质网应激促进线粒体钙负荷;而免疫细胞因子则可产生线粒体活性氧与钙紊乱。
概述
药物治疗是双相障碍管理的基础。加拿大心境和焦虑障碍治疗网络(CANMAT)和国际双相障碍学会(ISBD)联合发布的指南依据疗效、耐受性、安全性及心境转相风险,提供了分层级的治疗推荐。在药物治疗的基础上联合心理社会干预是双相障碍的理想治疗模式,包括心理教育(一线),认知行为疗法和家庭治疗(二线),以及人际与社会节律疗法(三线)。以正念为基础的干预方法(如,正念认知疗法)和辩证行为疗法,或可通过跨诊断治疗而提供与疾病阶段相适配的获益。互联网心理治疗,如移动App、面对面干预的线上改编版本,以及基于虚拟现实(VR)的认知矫正治疗,虽尚处于初步发展阶段,但似乎具有拓展服务可及性与推广范围的潜力。时间疗法,包括针对双相抑郁的强光疗法(Bright light therapy)和针对躁狂的去光疗法(Dark therapy),已在研究中展现出潜力;生活方式干预(如稳定的睡眠‑觉醒周期、日常规律作息),以及持续监测,则对预防复发至关重要。
药物治疗
锂盐仍是双相障碍的金标准药物,其在躁狂和维持治疗中的疗效已获证实,还具有潜在的抗自杀及神经保护作用。尽管锂盐治疗具有明确的获益,但全球范围内的锂盐处方量却呈下降趋势,其中以北美地区最为显著(2010年之前为27.7%,之后降至17.1%),欧洲地区下降幅度则相对较小。可能的原因包括:临床医生对新型药物更为熟悉,以及对锂盐监测难度或其副作用风险存在误解。
► 急性躁狂
治疗重点在于控制症状并保障患者安全。单药治疗与联合治疗的选择取决于症状严重程度、是否存在精神病性症状、激越程度及既往治疗反应。

一线治疗药物的优先级顺序由高到低依次为:锂盐、喹硫平、双丙戊酸钠、阿塞那平、阿立哌唑、帕利哌酮、利培酮和卡利拉嗪。
相较于心境稳定剂单药治疗,抗精神病药联合心境稳定剂治疗可使汇总治疗有效率提高20%,且治疗3周和6周时的耐受性无临床显著差异。
► 双相 I 型抑郁发作
治疗重点在于减轻抑郁症状,同时维持情绪稳定,并最大限度降低转为躁狂的风险。

一线治疗药物的优先级顺序由高到低依次为:喹硫平、锂盐、拉莫三嗪、卡利拉嗪、鲁拉西酮以及作为心境稳定剂辅助治疗的卢美哌隆。
不推荐抗抑郁药单药治疗;尽管抗抑郁药可作为心境稳定剂或抗精神病药的辅助治疗使用,但其应用仍存在争议。同时推荐联合心理社会治疗。
► 双相 II 型抑郁发作
根据CANMAT指南,喹硫平是唯一的一线单药治疗。抗抑郁药可作为二线治疗,但需要在严密监测下使用。
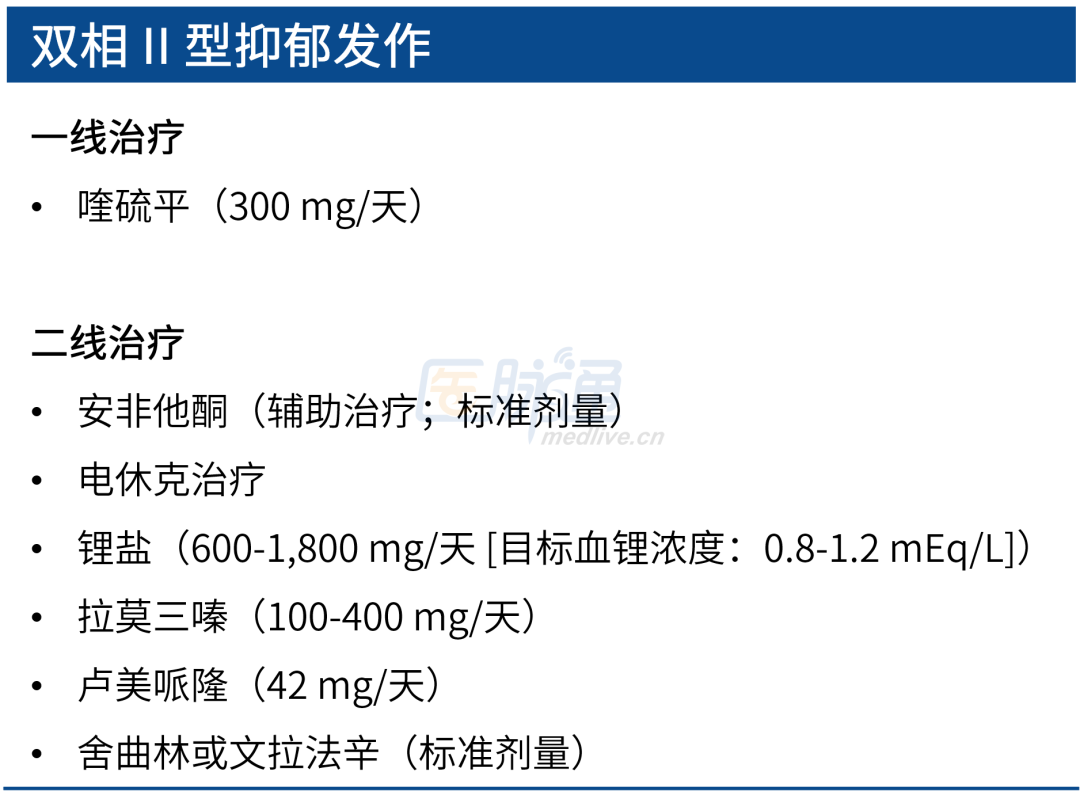
对于目前双相 II 型抑郁的大多数推荐意见,其制定所依据的直接证据较双相 I 型抑郁更为有限。
► 伴混合特征
第二代抗精神病药和丙戊酸盐为首选治疗方案。尽管锂盐已获FDA批准用于混合发作的治疗,但CANMAT指南并未将其视为有效的治疗手段。
推荐用药包括阿立哌唑、阿塞那平、卡马西平、卡利拉嗪、双丙戊酸钠、伊潘立酮、卢美哌隆、奥氮平、喹硫平,以及作为辅助治疗的利培酮和齐拉西酮;鲁拉西酮则被列为伴混合状态抑郁的二线治疗药物。
抗抑郁药单药治疗通常属于禁忌,因其可能诱发情绪不稳。
► 维持治疗和复发预防
长期治疗旨在降低心境发作的复发率、改善功能水平,并促进治疗依从性。急性期有效的治疗措施通常应延续至维持治疗阶段,但抗抑郁药除外。一项针对双相抑郁患者、在抗抑郁药联合抗躁狂药物治疗起效后进行的安慰剂对照停药研究中,持续使用抗抑郁药并不具有优势;但如果将生存曲线分析的起始时间点设为随机化的时间而非稳定期起始的时间,则数据提示持续使用抗抑郁药具有优势。

一线治疗药物的优先级顺序由高到低依次为:锂盐、喹硫平、双丙戊酸钠、拉莫三嗪、阿塞那平、锂盐/双丙戊酸钠联用喹硫平/阿立哌唑,以及阿立哌唑。
此外,宜定期随访评估,同时辅以心理社会治疗,以促进药物依从性、健康生活方式及整体健康状况。
双相抑郁的治疗缺口
抗抑郁药可能对部分双相抑郁患者有益,但存在诱发病情不稳的风险,尤其在双相 I 型及单药治疗的患者中。伴精神病性症状的躁狂发作后,抗精神病药增效治疗的最佳持续时长尚不明确。尽管多药维持策略在临床实践中被广泛使用,但支持其疗效的证据仍十分有限。双相抑郁持续导致功能结局受损及自杀倾向,但目前有效的治疗选择依然匮乏,且针对新作用机制的重大突破较为有限。这是本领域一个熟悉的紧张状态——临床需求迫切,但证据基础参差不齐,因此临床实践往往先于确证性试验而推进。
功能结局
患者的认知表现、工作功能、关系稳定性往往持续受损,且未被充分干预,而生活质量与这些领域的关系比与症状评分更为密切。神经心理学缺陷甚至可以在情绪正常期持续存在,且功能恢复通常滞后于症状恢复。由于患者常以功能指标来定义康复,目前学术界使用的结局指标尚不理想。临床目标应是改善患者在真实世界中的功能,而不仅限于控制症状。然而,针对双相障碍患者认知与功能的干预手段仍十分有限且分布不均。
新兴治疗策略
精准精神医学通过将多组学和神经影像数据与临床表现及环境暴露相结合,有望超越试错性质的用药选择。目前的期望是,生物标志物能够改善诊断亚型,优化预后判断,并指导治疗选择;然而,该领域尚未明确哪些生物标志物具有临床实用性。
针对双相抑郁,多项试验正在评估神经类固醇调节剂、谷氨酸调节剂(如氯胺酮)、重复经颅磁刺激、电休克治疗以及致幻剂,这标志着治疗策略正从传统的单胺策略转向干预不同生物学通路。这些干预措施在不同亚组人群及更长随访期中的疗效持久性仍有待验证。
鉴于能量代谢障碍在双相障碍中十分常见,代谢相关的干预措施正日益增多。针对胰岛素敏感性和血糖的药物,包括二甲双胍和GLP‑1受体激动剂,其潜在的情绪改善与功能增强作用正在研究中。线粒体调节剂,如N‑乙酰半胱氨酸,在双相抑郁中仍备受关注,但其治疗获益及应答亚组尚需更明确的界定。
我们对双相障碍神经生物学机制的理解持续成为研究重点,但迄今仍未形成全面、整合的理论模型。大量双相障碍患者的治疗结局仍不理想,凸显了进一步研发药物治疗及心理社会治疗的迫切需求。精准精神病学与个体化治疗有望带来更优的治疗结局,而多组学方法或将最终实现这一目标。

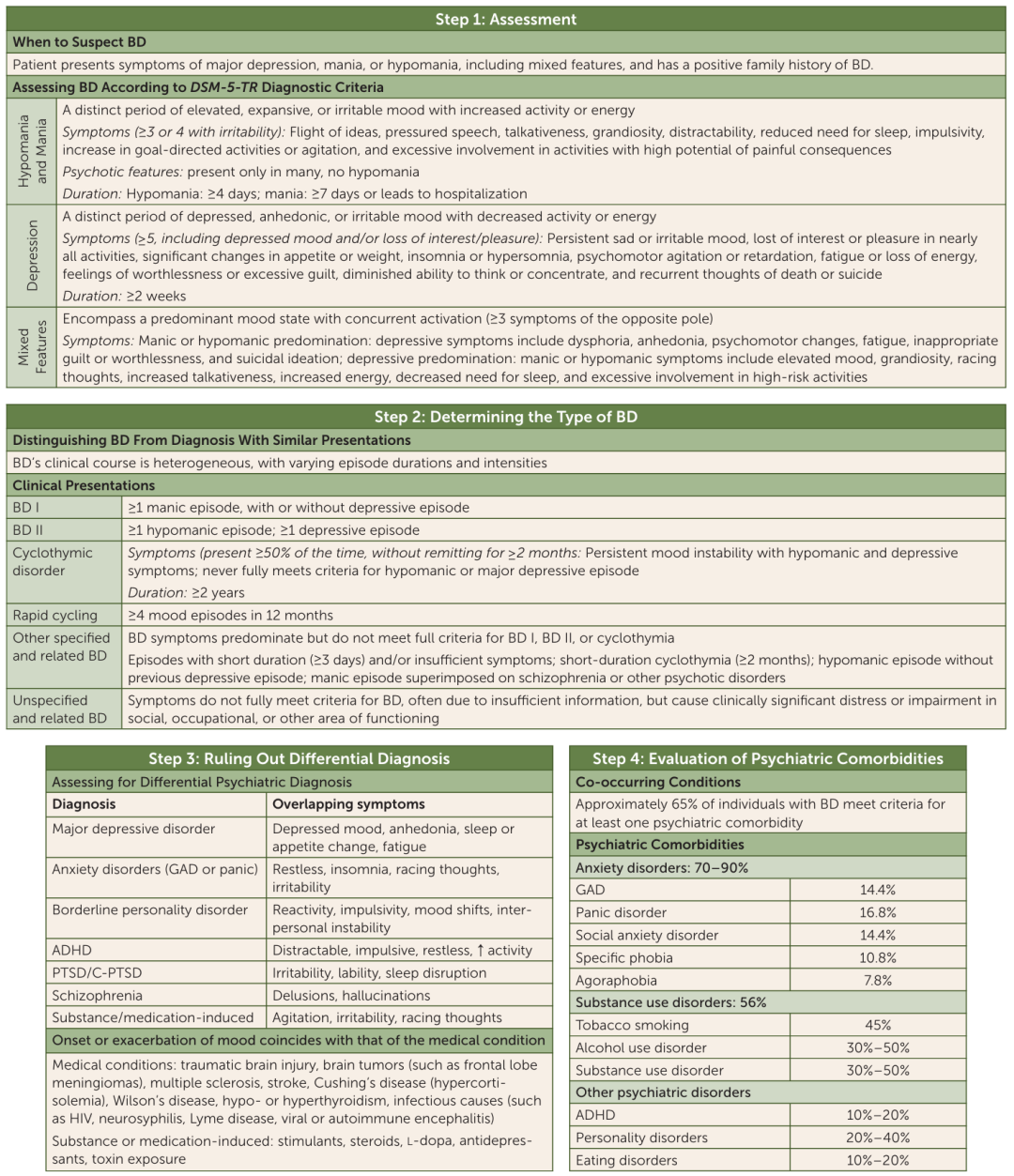
附:双相障碍逐步诊断框架,从Step1至Step4整合了亚型、发作表型、情绪模式、纵向病程、鉴别诊断及共病
2025-05-15

文献索引:Soliman MA, Khafif T, Sylvia L, et al. Bipolar Disorder: An Update on Neurobiology and Treatment. Am J Psychiatry. 2026 Mar 1;183(3):159-168. doi: 10.1176/appi.ajp.20260051. Epub 2026 Mar 1. PMID: 41764059.
点击「阅读原文」可查看及检索历史文章。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)