彭志友 冯智英△ (浙江大学医学院附属第一医院疼痛科)
在中国,脑卒中发病率居高不下,每年新发脑卒中病人约 200 万例,现存脑卒中病人已超过 1700万。脑卒中病人不仅可出现运动、感觉及认知功能障碍,还可能伴发卒中后疼痛。
卒中后中枢性疼痛 (CPSP) 可在卒中后亚急性期或数年内发生,其发生率为10.6%~55%。疼痛的持续存在使病人无法有效配合功能康复训练,还严重影响其生活质量,并造成沉重的社会负担。CPSP病程较长,可引发抑郁、焦虑等精神心理异常,这会加剧疼痛的持续时间和严重程度,并导致疼痛和负面情绪之间的恶性循环。目前常规的药物治疗和微创介入治疗效果远不能令人满意。脊髓电刺激 (SCS) 技术以微创、可逆、可调节的特点,已被证实对腰椎术后综合征、复杂性区域疼痛综合征、带状疱疹后神经痛、幻肢痛及糖尿病周围神经病变具有较好的治疗效果。SCS在CPSP治疗中的应用仍存在争议。
本文从 CPSP的临床特征及 SCS 在该病中的应用进展等方面展开综述,以期为 SCS 更有效地治疗 CPSP 提供理论依据与临床参考。

卒中后疼痛通常分为卒中后非中枢性疼痛和CPSP,卒中后非中枢性疼痛主要表现为伤害感受性疼痛,包括卒中后头痛、肩痛、肌肉骨骼痛、复杂性区域疼痛综合征及痉挛痛等。而CPSP则多表现为自发性疼痛、痛觉过敏、痛觉超敏和感觉异常等神经病理性疼痛。不同研究中CPSP的患病率存在较大差异,介于1%~35%之间,造成该差异的主要原因包括研究选择标准不同、病灶存在异质性、卒中后评估时间的差异,以及疼痛发作时间的不同等。
研究结果表明,CPSP病人的疼痛及异常感觉由皮质和皮质下病变引起。其患病率与卒中病灶所在位置有关,CPSP的丘脑损伤发生率占50%,延髓为24%,脑桥为12%,皮质为4%~5%。一项基于医院的前瞻性研究对319例卒中病人进行随访后发现CPSP患病率为20.7%,病灶涉及丘脑及丘脑外区域,其中57.6%的病灶位于右侧。不同研究中CPSP的卒中后发病时间差异显著。一项队列研究显示,多数病人在卒中后1~3个月出现症状。CPSP的发病机制尚未完全阐明,现有研究认为中枢敏化、中枢脱抑制、丘脑功能改变、胶质细胞及促炎细胞因子调控等均可能参与CPSP的发生与维持。
CPSP的典型特征为自发性或诱发性疼痛及感觉异常,与躯体感觉功能受损相关。在大多数病例中,疼痛表现为烧灼痛、搏动痛、刺痛、酸痛、痛觉过敏、撕裂痛、冷冻痛、压榨痛等。疼痛可呈持续性或间歇性,强度通常不固定,遇寒冷、活动、触摸或压力等外界刺激时加重,放松或注意力转移时减轻。总体而言,疼痛部位多局限于与中枢神经系统病灶相对应的感觉异常区域。一项研究纳入了 39 例 CPSP 病人,其中 79.5% 的病人疼痛位于上肢、面部和下肢。丘脑是感觉系统的重要中继核团,丘脑腹侧和后前枕部、岛叶后部、内侧顶盖参与伤害性感觉处理,这些部位损伤更容易造成CPSP。在临床检查中,病灶位置也与身体功能障碍部位相关:丘脑病灶病人的症状多表现为对侧半身不适;延髓病灶的症状则因病灶位于内侧或外侧而具有部位特异性—内侧病灶的功能障碍局限于四肢和躯干,病人常以麻木和刺痛描述疼痛;外侧病灶则表现为面部功能障碍,可累及对侧或同侧,疼痛描述多为冷痛或烧灼痛。此外,若病灶位于豆状核囊,下肢疼痛症状的发生率高于上肢和面部。CPSP可对卒中病人的情绪、睡眠质量、康复进程及生活质量产生明显的负面影响。
CPSP的治疗首选药物治疗。阿米替林和加巴喷丁类分别被视为治疗CPSP的一线和二线药物。此外也可以使用阿片类镇痛药和中枢性骨骼肌松弛剂(如巴氯芬等)。对于顽固性病例,还可考虑使用其他药物,如氟伏沙明、糖皮质激素,以及静脉输注利多卡因、氯胺酮等。临床实践中发现,抗抑郁药物与加巴喷丁类药物联合使用更有效,且可降低药物剂量。
对于药物治疗无效的病人,可考虑采用非侵入性治疗方法,包括重复经颅磁刺激 (rTMS)、经颅直流电刺激 (tDCS)、有创运动皮质刺激、深部脑刺激 (DBS) 以及运动疗法和脑机接口等治疗手段。目前CPSP的治疗选择有限,因此迫切需要关注新的治疗手段,以在优化疗效的同时最大限度地减少不良反应。SCS作为一种神经调控技术,近年来在治疗CPSP方面逐渐受到关注。

SCS 是目前应用最广泛的慢性神经病理性疼痛神经调控疗法之一,适应证从慢性顽固性疼痛扩展至脊髓损伤、卒中后疼痛等领域。其广泛应用的原因包括创伤较小、并发症发生率低且疗效确切。
国内2003年开展首例手术,2016年启动国产设备研发,后续专家共识的发布推动了技术规范化应用。2024年中美脊髓电刺激管理慢性疼痛共识工作组发布的《脊髓电刺激管理慢性疼痛共识 (2024)》中SCS 的适应证包括脑卒中后疼痛,其净获益证据等级为中,推荐强度为B。SCS用于治疗CPSP的部分研究结果见表1。
表1 SCS治疗CPSP部分研究的一般资料与临床数据
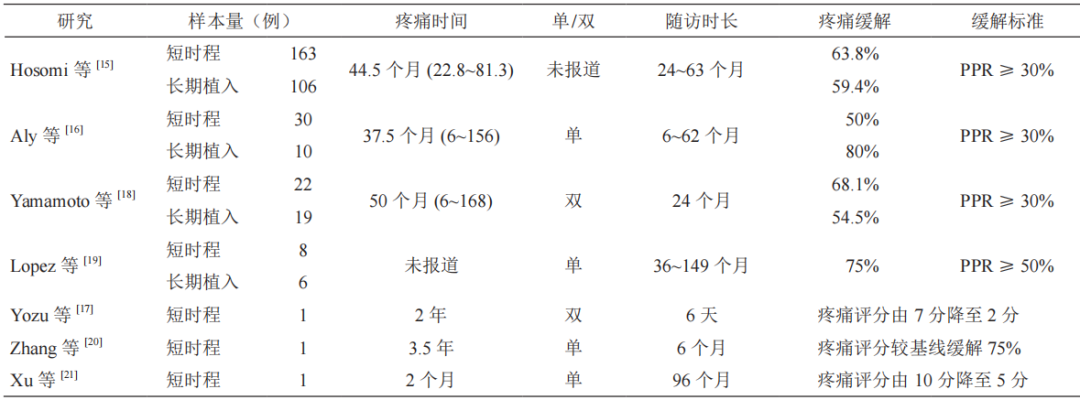
PPR:疼痛缓解百分比
目前越来越多的研究报道了SCS可用于治疗CPSP。
而更多的研究结果来自于病例数较少的病例报道。
然而SCS治疗CPSP的效果仍存在争议。欧洲神经学会联合会和国际疼痛研究小组神经病理性疼痛特别兴趣小组 (NeuPSIG) 发布的指南与建议中,目前不推荐将SCS用于CPSP的治疗,这主要是由于目前仍然缺乏高质量的临床证据,且研究结果并非认为SCS用于CPSP均能取得满意的效果。
同时,SCS对脑卒中病人的运动功能恢复具有积极作用。脑卒中可破坏从运动皮质区到脊髓的下行指令,进而导致永久性的手臂和手部运动功能障碍。然而,病灶下方控制运动的脊髓环路仍保持完整,可作为神经技术的干预靶点以恢复运动功能。
SCS可通过提高脊髓环路的兴奋性,改善卒中后残余皮质脊髓束的功能有效性。与脊髓损伤相比,SCS用于卒中后疼痛的效果可能更显著,因卒中病灶下方的脊髓环路结构完整。
SCS对于CPSP的疗效和预测因素尚未完全明确。

SCS 缓解疼痛的机制之一是基于“门控理论”。该理论假设在病灶水平以上存在疼痛抑制系统,通过在病灶水平以上施加电刺激可驱动该抑制机制。然而,CPSP 的疼痛产生原因主要源于脑内躯体感觉神经传导通路的损伤,引起脑内中枢神经元高反应性或自发性异常放电。既往观点认为,对疼痛下游通路实施神经调控,难以对疼痛产生抑制作用。但研究发现即使疼痛原因位于脑内,脊髓节段的神经调控对部分病人确实起到了的镇痛作用。然而,因为电极刺激作用于卒中病灶水平以下,SCS 治疗CPSP 的疼痛缓解机制无法用门控理论解释,因此,目前认为 SCS 可同时在脊髓节段水平发挥抑制作用,并激活脊髓上区域,包括 SCS 对多区域脑活动的影响。既往研究表明,SCS 可诱导 γ-氨基丁酸和乙酰胆碱释放,从而抑制脊髓背角的谷氨酸释放,这在疼痛缓解中起重要作用。SCS 可能通过改善感觉门控机制产生镇痛效应,感觉门控通过初级传入纤维去极化和突触前抑制实现,二者均能调控向整个脊髓节段以及特定运动神经元的突触传递。突触前抑制和初级传入纤维去极化均由 γ-氨基丁酸能神经元产生,这些神经元接收初级传入纤维的直接支配。
刺激脊髓后索中的传入纤维可将刺激输入传递至脑干和丘脑核团,并可能到达皮质-丘脑通路,该通路可能在可塑性中发挥作用。这些效应在卒中病人中可能会增强,与脊髓损伤病人不同,卒中病人的脊髓感觉上行通路通常未受损,从而使脊髓上通路得以参与其中。有研究利用神经影像学技术探讨了 SCS 对脊髓上区域的影响,结果显示 SCS 可调节大脑感觉和情感区域的活动,这些区域被称为“疼痛矩阵”,疼痛矩阵由一系列脑结构网络组成,包括丘脑、前扣带回皮质、躯体感觉皮质及其他区域。丘脑是这些疼痛矩阵区域的中继站和中心,因此当丘脑腹后外侧核受损时,SCS可能无法在脑矩阵内诱导足够的神经调控效应,这可能是丘脑病灶与非丘脑病灶所致CPSP病人SCS治疗成功率存在差异的原因之一。

SCS 治疗具有多方面显著优势。其一,作为非药物治疗手段,它相较于传统药物治疗可完全避免药物不良反应。其二,该治疗具备可逆可调的特点,具有高度灵活性,能更好地适应个体差异以提升疗效。其三,它不仅能缓解疼痛,还能积极改善运动功能,通过降低肌张力、改善肌肉痉挛、促进神经可塑性帮助病人恢复运动能力。
然而,SCS 治疗仍面临着多方面的挑战。首先是个体差异问题,由于不同病人的脑卒中类型、损伤部位、程度、病程、身体状况及心理状态等均存在不同,导致其对治疗的反应差异较大,这种不确定性也给治疗方案制定带来困难。其次是刺激参数优化的难题,目前该治疗的最佳刺激参数尚未完全明确,不同病人需适配不同的频率、脉宽、强度等参数组合,且治疗中病情变化还需及时调整参数,影响了治疗效果的一致性与可重复性。第三是成本问题,该治疗费用相对高昂,让许多经济条件较差的家庭难以接受治疗,也在一定程度上限制了该技术的广泛应用。

综上所述,SCS治疗CPSP已在临床研究中展现出一定的有效性和独特优势。在SCS治疗的未来研究方向上,
首先需确定最佳刺激方案和参数,即进一步深入研究病人年龄、性别、卒中类型、病程等个体特征与刺激频率、脉宽、强度等参数之间的关系,通过大数据分析和人工智能技术建立个性化参数优化模型,以实现精准治疗并提升疗效的一致性与稳定性。
其次应开展多中心、大规模且长期随访的随机对照试验,扩大样本量并覆盖更广泛病人群体,从而更全面准确地评估 SCS 治疗 CPSP 的疗效与安全性,为临床应用提供更具说服力的证据。
此外,还应借助功能磁共振成像、弥散张量成像等神经影像学技术、脑机接口技术、脑磁图、诱发电位等神经电生理技术,以及基因测序、蛋白质组学等分子生物学技术,从神经环路、神经递质、基因表达等多层面深入研究 SCS 治疗 CPSP 的作用机制,为治疗方案优化提供坚实理论基础。
来源:彭志友, 冯智英.脊髓电刺激在卒中后中枢性疼痛中的应用进展[J].中国疼痛医学杂志,2026,32(2):98~103
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)