在缺血性卒中的二级预防领域,
该研究不仅补充了房颤相关卒中预后机制的重要证据,也在一定程度上提示,单纯基于“心源性栓塞”的传统认知,或难以完整解释这类患者的长期风险结构。
本项分析纳入11项前瞻性研究,共计10,080例卒中或
研究首先从炎症表型入手,对IL-6与
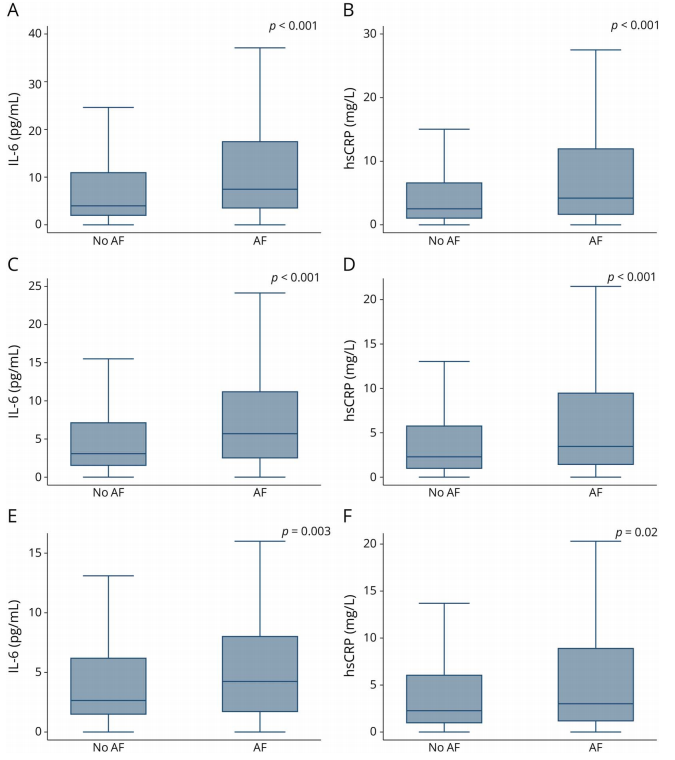
图1 缺血性中风或短暂性脑缺血发作事件中的 IL-6 和 hsCRP 水平
(A,B:所有患者;C,D:轻型卒中;E,F:TIA)
进一步分析提示,这种炎症升高并非仅限于急性期。在不同时间窗口的分层中,hsCRP在从超急性期至亚急性期均持续高于非房颤患者,而IL-6除发病最初24小时外,在后续各时间点同样维持较高水平。值得注意的是,在一项随访接近1年的研究中,房颤患者的IL-6与hsCRP仍高于对照组,提示炎症反应具有长期持续性。
这一结果从表型层面提示,房颤相关卒中并非单一事件驱动的急性过程,而更可能发生在持续的全身炎症背景之中。
在总计约21,000人年的随访中,共有1,677例患者发生主要不良心血管事件(MACE),1,342例发生卒中复发。
在预后分析中,hsCRP与MACE之间呈现出稳定的正相关关系。在房颤患者中,每对数单位hsCRP升高,MACE风险增加14%(aRR=1.14,95% CI 1.04–1.25);按四分位分层时,最高四分位较最低四分位风险增加约51%(aRR=1.51,95% CI 1.04–2.18)。
在非房颤患者中,hsCRP与MACE同样呈现相似趋势(aRR=1.08,95% CI 1.03–1.13),且两组之间未观察到显著交互作用(Pinteraction=0.30)。
IL-6的结果整体一致,但在房颤亚组中未达到统计学显著。在非房颤患者中,IL-6与MACE及复发卒中均存在独立相关性,例如复发卒中风险增加(aRR=1.15,95% CI 1.05–1.25)。
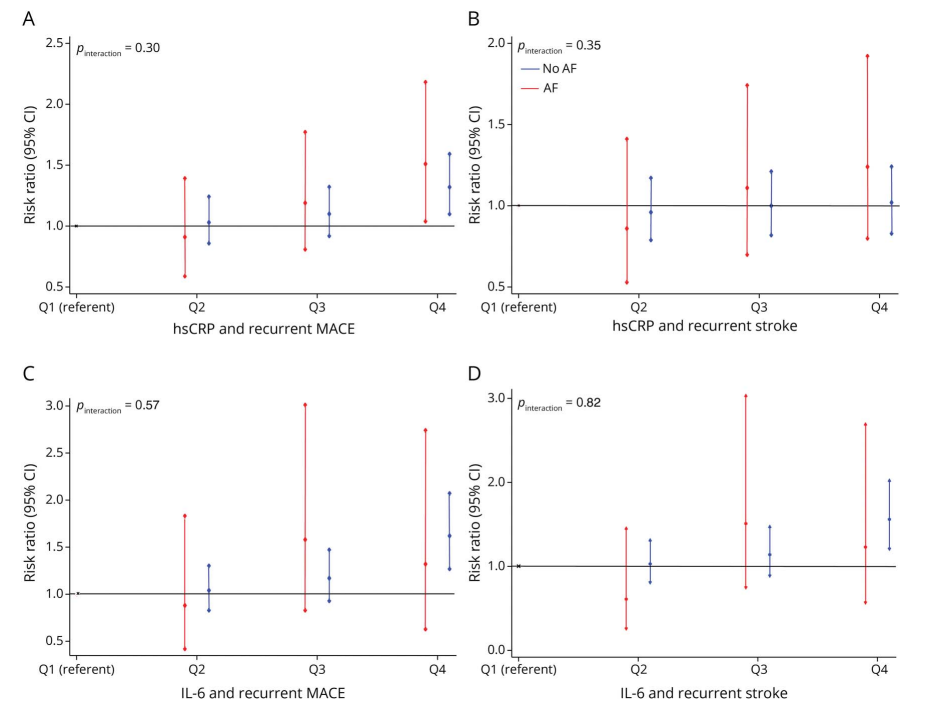
图2 hsCRP、IL-6与MACE、卒中复发之间的关系
值得关注的是,无论是hsCRP还是IL-6,其与卒中复发的关联均不如与MACE的关联稳定。特别是hsCRP,在房颤与非房颤人群中均未显示与复发卒中的明确相关性。
总体来看,炎症标志物与不良血管事件之间呈现出“剂量依赖”的关系,而这一关系并不因是否合并房颤而发生本质改变。
这项Meta分析结果的意义并不仅限于风险预测,更在于其对卒中机制理解的补充。
传统上,房颤相关卒中被归类为“心源性栓塞”,而炎症更多被认为与
在这一框架下,所谓“心源性”与“动脉源性”的划分,或更多反映事件表现形式,而非其上游驱动因素。炎症可能作为共同的上游机制,贯穿不同卒中亚型的发生与复发过程。
从研究结论来看,最直接的启示在于:房颤患者不应在抗炎治疗研究中被系统性排除。
既往多项抗炎治疗随机对照试验(如
研究进一步提示,与其基于卒中病因进行简单分层,不如考虑基于炎症表型进行患者选择。IL-6与hsCRP所反映的“炎症高反应状态”,可能代表一种跨越病因分类的风险亚型,这一思路为未来精准医学导向的二级预防研究提供了新的方向。
综合本项Meta分析及其评论,可以看到,炎症在房颤相关卒中中的作用正在逐步被重新认识。研究显示,房颤患者在卒中后存在持续的炎症激活状态,且炎症水平与不良血管事件风险呈剂量依赖关系,这一关联并不因是否合并房颤而改变。
这一发现提示,房颤相关卒中的残余风险,可能并非完全由抗凝未覆盖的栓塞机制所驱动,炎症作为潜在上游因素,或在其中发挥重要作用。围绕这一方向展开的进一步研究,有望为卒中二级预防提供新的干预靶点与分层策略。
参考文献:
1. Acampa M, Lazzerini PE. Inflammation in Atrial Fibrillation-Related Stroke: Time to Rethink Therapeutic Strategies. Neurology. 2026;106(6):e214784.
2. McCabe JJ, Harris K, Gorey S, et al. Systemic Inflammation and Recurrence After Atrial Fibrillation-Related Stroke: An Individual Participant Data Meta-Analysis. Neurology. 2026;106(6):e214701.
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)