前言
自身抗体作为多种肾小球肾炎的重要致病因素,其产生和致病机制已成为该领域的研究重点。基于这一病理生理学基础,目前临床上已成功开发出针对抗体生成的靶向治疗策略,这些干预措施显著提高了此类疾病的临床缓解率。
近期,《CJASN》杂志发表了一项综述“How I Treat Challenging Cases of Antibody Mediated GlomerularDiseases”,系统梳理了自身抗体相关肾小球肾炎的发展历程、诊疗现状及未来研究方向,旨在为临床诊疗工作提供参考与借鉴。
20世纪70-80年代,美国国立卫生研究院等机构证实,
20世纪90年代至21世纪初,临床实践转向以
进入21世纪中期,B细胞靶向治疗药物
基于"自身反应性B细胞激活→浆母细胞分化→
尽管不同疾病类型及患者个体间存在治疗反应差异,但针对抗体介导的自身免疫性疾病,存在一个普适性的核心治疗原则。临床实践表明,对大多数患者而言,早期实施"联合治疗方案"不仅能显著提高临床缓解率,还可有效降低糖皮质激素的累积使用剂量。
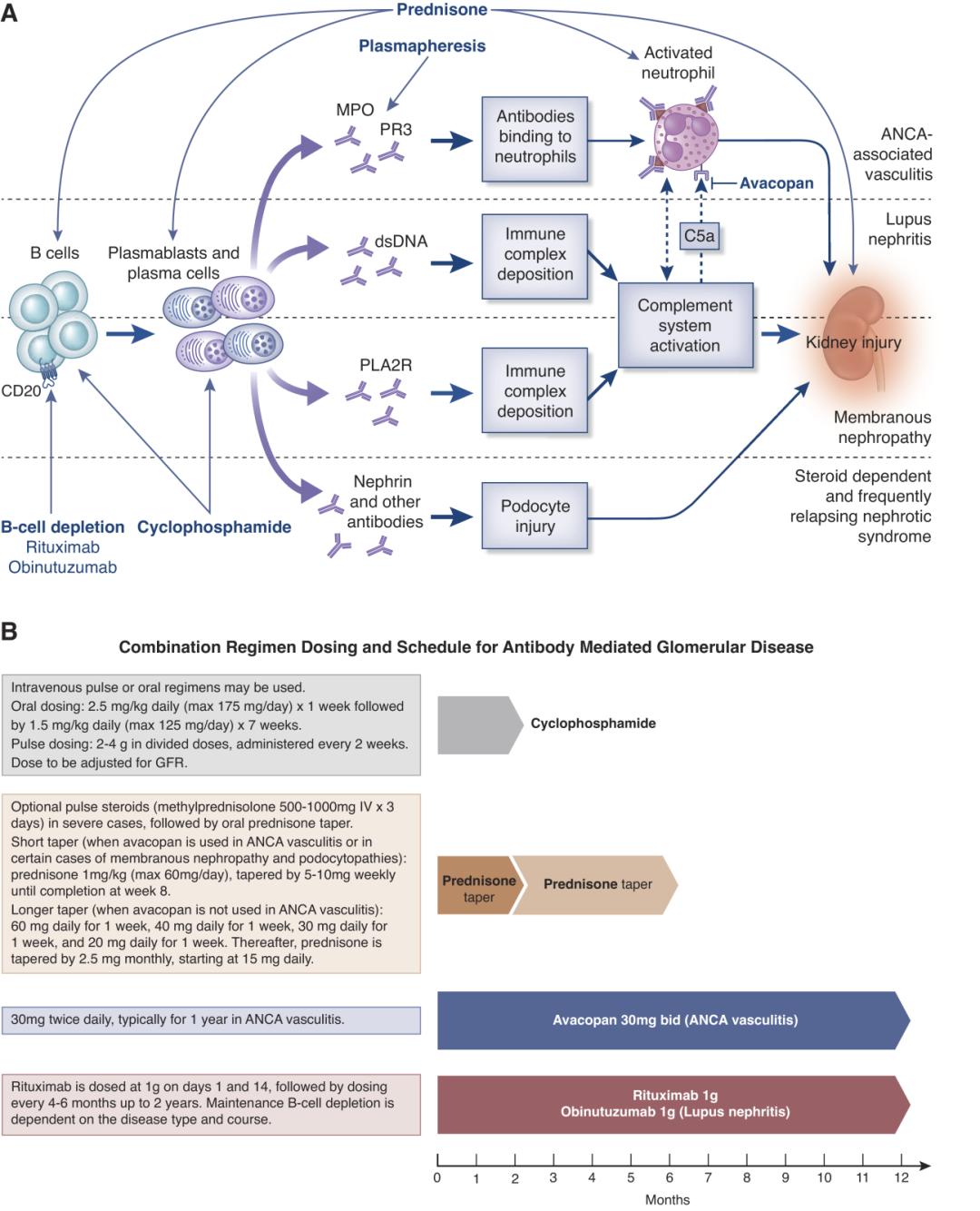
图1. 抗体介导性肾小球疾病的治疗(A)与联合治疗方案用药剂量与疗程(AB)
1.环磷酰胺(CYC)
口服方案:2.5mg/kg/d(最大175mg/d)×1周,继以1.5mg/kg/d(最大125mg/d)×7周
脉冲方案:2-4g分次给药,每2周一次(需根据GFR调整剂量)
2.
重症患者:可选
短程方案(适用于ANCA血管炎使用
初始1mg/kg/d(最大60mg/d),每周递减5-10mg,8周完成减量
长程方案(ANCA血管炎未使用阿伐可泮时):
60mg/d×1周→40mg/d×1周→30mg/d×1周→20mg/d×1周→15mg/d起始,每月递减2.5mg
3.阿伐可泮:30mg每日两次,ANCA血管炎通常持续用药1年
4.B细胞清除治疗:
利妥昔单抗标准剂量:第1天、第14天各1g
维持治疗:每4-6个月给药一次,持续至2年(具体方案需根据疾病类型和病程调整)
(注:所有剂量方案需根据患者肾功能及临床反应个体化调整)
狼疮性肾炎
根据《2024 KDIGO
自LUNAR研究(利妥昔单抗治疗狼疮性肾炎评估试验)开展以来,B细胞清除疗法尚未被推荐作为狼疮性肾炎的一线诱导方案,这是因为部分患者会出现B细胞早期重建(<3个月)的情况,从而影响治疗效果。不过,LUNAR试验的亚组分析显示,实现外周B细胞清除的患者,其完全缓解率有显著提高。最新数据表明,对于能够实现持续B细胞清除的患者,奥妥珠单抗可能更具应用优势。
作者所在中心针对重症或难治性狼疮性肾炎,常采用“联合方案”(利妥昔单抗+短期环磷酰胺+激素)进行治疗,且疗效显著。而对于B细胞清除失败或出现早期重建的患者,我们会考虑调整给药频次,或换用其B细胞清除剂(如奥瑞利珠单抗、奥妥珠单抗)。
膜性肾病
根据《2021 KDIGO 肾小球肾炎管理临床实践指南》,对于需要接受免疫抑制治疗的高危膜性肾病患者,推荐采用利妥昔单抗方案,或环磷酰胺联合糖皮质激素方案。MENTOR研究(利妥昔单抗治疗膜性肾病试验)的数据显示,单独使用利妥昔单抗治疗时,患者的完全缓解率较低,且缓解持续时间较短——12个月时完全缓解率为14%,24个月时为35%。
作者所在中心采用"联合治疗方案"的临床数据显示:
- 完全缓解率显著提高(12个月45%,24个月83%)
- 所有PLA2R阳性患者在治疗6个月内均达到免疫学缓解
- 2年随访期内无复发病例
ANCA相关性血管炎
RAVE研究(利妥昔单抗治疗ANCA相关性血管炎诱导试验)结果表明,利妥昔单抗与环磷酰胺联合大剂量激素治疗的总体疗效相当,但两组分别有36%和47%的患者未能达到主要治疗终点。值得注意的是,后续针对重症患者的研究证实,采用短期环磷酰胺联合利妥昔单抗和激素的"三联方案"可显著提高治疗效果。
作者所在中心临床数据显示,该"三联方案"可实现84%的早期完全缓解率(随访5个月时)。在ADVOCATE试验证据支持下,进一步优化方案:加用阿伐可泮以促进激素快速减量;同时严格掌握血浆置换指征,仅用于急性肾损伤严重(需快速控制疾病活动以保护残肾功能)的患者。
上述治疗策略与《2024 KDIGO 抗中性粒细胞细胞浆抗体(ANCA)相关血管炎管理的临床实践指南》推荐高度吻合:
- 严重肾功能不全(血肌酐>4mg/dL)考虑联合治疗
- 血肌酐>3.4mg/dL或快速升高、或需透析时行血浆置换
- 使用阿伐可泮作为激素替代方案
足细胞病
频复发型、激素依赖型及激素抵抗型肾病综合征的治疗往往颇具挑战。《2021 KDIGO 肾小球肾炎管理临床实践指南》对此作出推荐:针对频复发或激素依赖的微小病变型肾病,可选用利妥昔单抗、环磷酰胺、钙调磷酸酶抑制剂或霉酚酸;对于激素抵抗型局灶节段性肾小球硬化(FSGS),则建议采用钙调磷酸酶抑制剂。
结合作者所在中心的临床经验,“联合治疗方案”对激素敏感的患者(包括激素依赖型和频复发型)疗效显著,但对激素抵抗型患者效果欠佳。Gauckler等人开展的大型研究也证实了这一结论:激素依赖或频复发患者的完全缓解率可达82%,而激素抵抗型患者仅为18%。目前,抗nephrin抗体检测能否为阳性患者的治疗决策提供指导,仍有待进一步研究验证。
在血管炎治疗中,采用“联合方案”诱导期间,ANCA水平每月平均下降47%,而总IgG仅降低6%。由于该方案(利妥昔单抗+有限剂量环磷酰胺+减量激素)相对保护了T细胞功能,严重感染的发生率较低(10%),机会性感染几乎可避免。同时,短期使用小剂量环磷酰胺(静脉或口服)的耐受性良好,且因累积剂量较低(<8g),生育功能受影响等副作用也得到了有效控制。
尽管单用利妥昔单抗诱导缓解的速度较慢,但在通过联合治疗获得抗体应答并实现缓解后,每4-6个月进行一次利妥昔单抗维持治疗,可使大多数患者维持长期缓解,且无需持续使用激素。在维持治疗阶段,多数患者仅需接受B细胞清除治疗即可;而对于免疫学应答或临床应答欠佳的患者,则可选择性联用其他药物。
-B细胞长期清除的副作用考量
尽管治疗初期感染较为罕见,且未出现肺孢子菌肺炎、巨细胞病毒感染等典型机会性感染,但长期抑制B细胞会引发功能性或绝对性低丙种球蛋白血症。这可能增加多种风险,包括反复发生肺部感染(如支气管炎、支气管扩张症)、需要长期抗病毒治疗及静脉注射免疫球蛋白的新冠肺炎,以及易被忽视的炎症性阴道炎等。
-停药时机选择
关于停药时机的选择:ANCA相关性血管炎患者停用利妥昔单抗后,5年内复发率仍达30%-50%,而无限期维持治疗会增加感染风险。我们开展的B细胞清除两年后维持策略研究显示,根据B细胞重建情况调整给药方案的患者,3年复发率显著降低(4% vs 20%),且严重不良事件发生率无差异。两年后,我们会根据B细胞恢复情况延长给药间隔,最终疗程则依据患者的临床特征和感染风险进行个体化调整;若出现感染问题,需暂停治疗,直至B细胞恢复且感染痊愈。《2024 KDIGO 抗中性粒细胞细胞浆抗体(ANCA)相关血管炎管理的临床实践指南》建议,最佳维持疗程为18个月至4年,期间需权衡复发与感染风险。
对于膜性肾病患者,由于其复发进展相对缓慢,完成两年B细胞清除治疗后复发率较低,因此我们通常在治疗满两年时停药。而足细胞病和狼疮性肾炎患者的治疗疗程,因疾病应答情况和临床进程的不同而存在较大差异。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)