免疫球蛋白A 近期,北京大学第一医院研究团队于《JASN 》杂志发表了TESTING试验的病理学亚组研究“Predictive Value of the Oxford Classification for the Effect of Glucocorticoid Therapy in IgA Nephropathy”,探讨了中国IgAN患者的病理学特征与临床结局的关联,该研究结果证实:肾小球新月体和细胞性节段性硬化病变可作为
研究背景
组织病理学指标长期以来一直是评估IgAN疾病活动度、慢性化程度及预后的重要依据。IgAN的组织学评估主要依赖牛津分型(MEST-C)评分系统,该体系被KDIGO指南采纳并纳入国际预测工具,但其未纳入C评分(新月体评分),原因在于新月体病变与主要预后的相关性可能受到后续免疫抑制治疗的干扰,且该病变特征存在显著的种族/民族差异。此外,KDIGO指南强调,不应仅依据新月体存在与否或数量决定免疫抑制治疗,因其缺乏前瞻性随机数据支持,且活检与治疗启动间存在时间变异性。
“TESTING”是一项国际多中心、双盲、随机临床试验,旨在评估甲基强的松龙治疗对高进展风险IgAN患者的获益与风险。该研究初始队列中大多数为中国受试者,且所有受试者均在活检后短期内完成随机分组治疗。研究证实,6-9个月的甲基强的松龙递减疗法可显著降低IgAN患者的肾功能衰竭风险,但同时也存在严重感染性不良事件的风险。 基于此,TESTING试验的受试者成为评估组织病理学参数能否预测糖皮质激素对IgAN肾脏结局疗效的理想队列。
研究方法
TESTING试验的研究方案及结果已发表。该试验最初纳入2012年5月至2019年11月间,来自5个国家的503例IgAN受试者,第一阶段接受足量糖皮质激素治疗,随机分配至口服甲基强的松龙0.6~0.8mg/kg/d,治疗2个月后每月递减8mg/d,总疗程6~8个月。2019年,由于感染相关严重不良事件发生率较高,第二阶段将剂量减少为0.4mg/kg/d(最大剂量32mg/d),治疗2个月后每月递减4mg/d,并联合使用抗肺孢子菌药物以预防感染,总疗程6~9个月。本次病理学亚组研究仅纳入TESTING试验中国受试者,这些受试者的肾活检与糖皮质激素治疗间隔时间较短,且通过收集全国各地方中心的病理切片,可对牛津分类进行集中病理审核。
入组时,各中心病理医师根据肾活检报告记录牛津分型。试验初期,牛津分型尚未纳入C病变,因此研究者手动计算了细胞性/纤维细胞性新月体涉及的肾小球数目,并据此评定C评分。共有379例中国受试者同意参与病理学亚组研究,最终获得289例受试者的肾活检切片用于中心评估,排除10例肾小球数<8个的活检标本后,共279例受试者纳入最终分析(图1)。 研究收集了患者随机分组时的年龄、估算肾小球滤过率(eGFR)、24小时尿蛋白排泄量、血压及
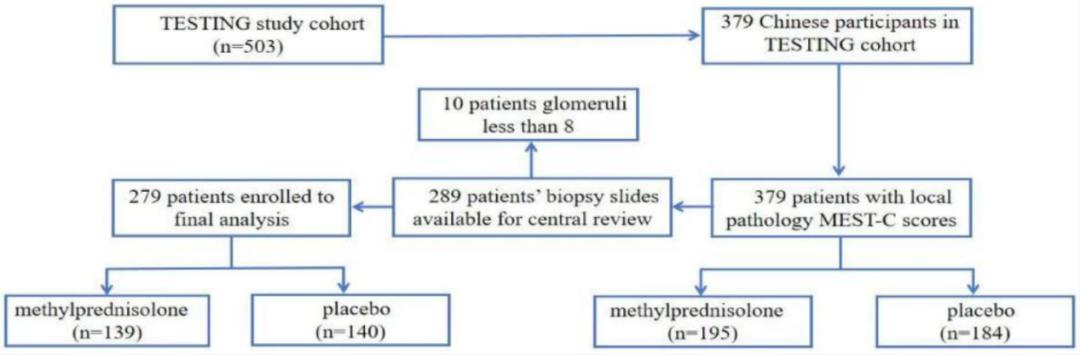
图1 研究受试者入选流程图
依据牛津分型标准,对受试者系膜细胞增生(M)、毛细血管内增生(E)、节段性硬化(S)、肾小管萎缩/间质纤维化(T)及新月体(C)进行评分。其中,S1病变进一步根据以下组织学特征进行亚分类:
-细胞性节段性硬化(CSS):节段硬化病灶内存在炎症/细胞增生(图2)。需注意,毛细血管腔因基质沉积闭塞伴硬化病灶内炎症浸润的CSS病变,虽不符合E病变(定义为“毛细血管腔内细胞增多导致管腔狭窄或闭塞”)的诊断标准,但仍单独归类;
-足细胞病性节段性硬化(PSS);
-纤维性节段性硬化(FSS):节段性硬化伴鲍曼囊破裂和/或纤维性新月体形成,但无细胞增生。
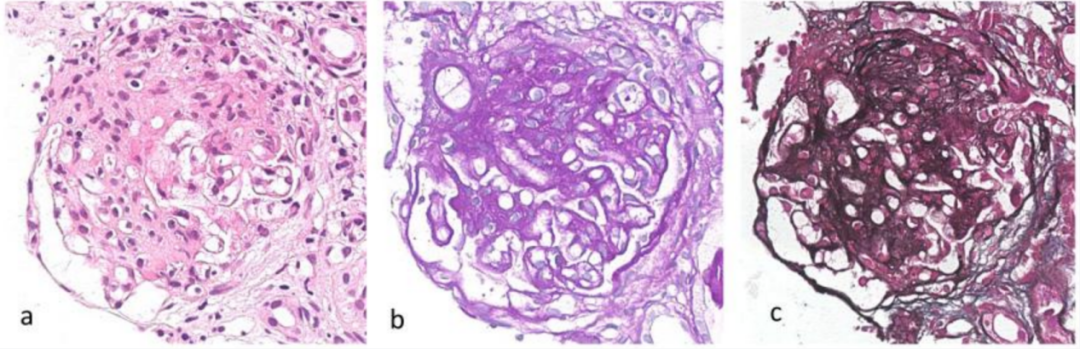
图2. 细胞性节段性硬化(CSS):同一肾小球切片的H&E染色(a)、PAS染色(b)和Jones银染(c)
H&E染色显示节段性硬化病变内的炎症反应,该节段在PAS染色中可见毛细血管腔消失。银染切片中可见鲍曼囊(Bowman's capsule)的破坏。
研究结果
279例患者的基线特征显示:平均eGFR为61±23ml/min/1.73m²,24小时尿蛋白定量为2.4±1.5g/d。当地病理报告显示的牛津分型病变发生率分别为:M1(59%)、E1(29%)、S1(74%)、T1(40%)、T2(18%)、C1(46%)及C2(16%)。本亚组研究中279例患者的基线临床与病理学特征,与TESTING试验全部379例中国受试者及整体试验人群具有可比性(表1)。
表1. 本亚组研究、TESTING试验全部中国受试者及TESTING试验全部受试者的基线临床与病理学特征
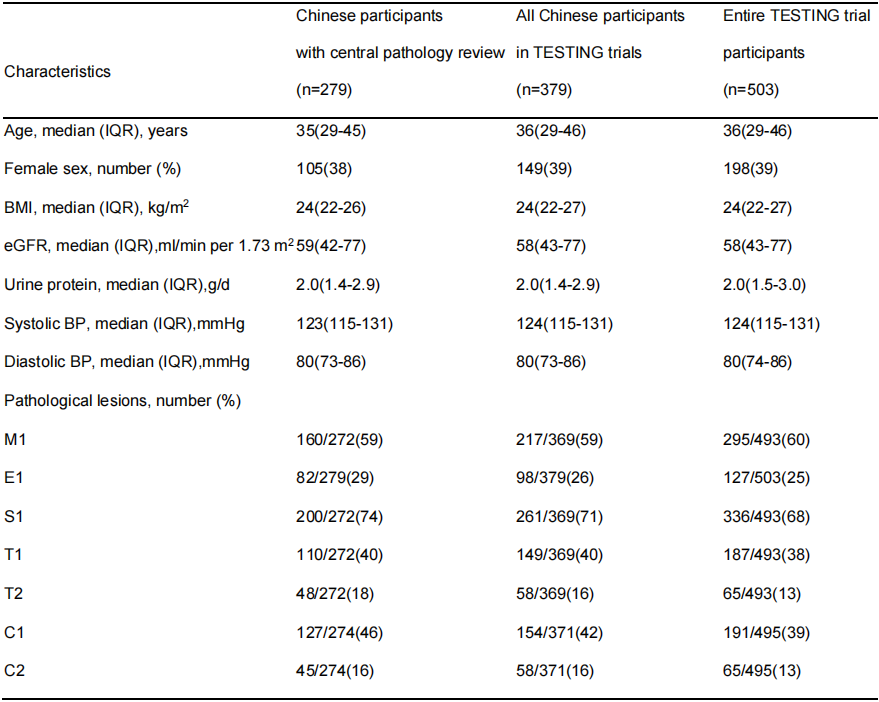
eGFR:估算肾小球滤过率;systolic BP:收缩压;diastolic BP:舒张压;BMI:身体质量指数(体重指数)
收集全国各地方中心的病理切片,对279例受试者进行集中病理复核,肾活检至随机分组的中位时间为4(3-7)个月。集中复核判定的牛津分型病变发生率分别为:M1(32%)、E1(27%)、S1(86%)、T1(30%)、T2(8%)、C1(17%)及C2(0.4%)。由于仅1例活检标本评为C2,后续分析将C1与C2合并统计。
受试者随机分配至安慰剂组(n=140,50%)和甲基强的松龙治疗组(n=139,50%)。两组间临床指标及牛津分型无显著差异,但安慰剂组新月体病变(C1+C2)发生率显著高于治疗组(22% [31/140] vs 13% [18/139],P=0.04)。中位随访时间分别为安慰剂组4.7(3.0-6.4)年与治疗组5.1(3.1-6.8)年。安慰剂组进展至肾脏终点的受试者比例显著高于治疗组(46% [65/140] vs 35% [48/138],P=0.04)(表2)。
表2. 集中病理复核的279例中国受试者基线临床与病理学特征
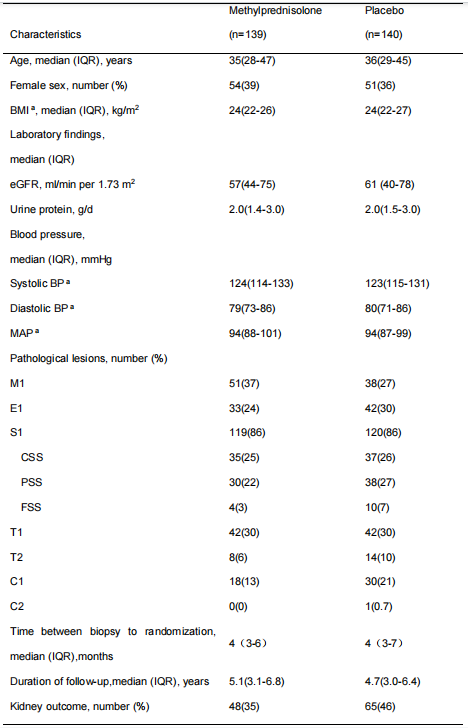
eGFR:估算肾小球滤过率;systolic BP:收缩压;diastolic BP:舒张压;MAP:平均动脉压 ;舒张压+1/3(收缩压-舒张压);BMI:身体质量指数(体重指数);M:系膜细胞增生;E:内皮细胞增生;S:节段性硬化;T:肾小管萎缩/间质纤维化;C:细胞性/纤维细胞性新月体;CSS:细胞性节段性硬化;PSS:足细胞节段性硬化;FSS:纤维性新月体节段性硬化
a:基线数据缺失(n=1)
b:由于T2或C2病变的受试者数量有限,分析时将T1与T2病变、C1与C2病变合并
合并T1/T2病变、CSS及PSS的受试者,其基线eGFR水平显著低于未合并这些病变的患者(T1/T2病变组:48±19 vs T0组:69±22;CSS组:55±20 vs 无CSS组:64±24;PSS组:53±19 vs 无PSS组:64±24)。值得注意的是,PSS病变患者的24小时尿蛋白定量显著高于非PSS患者(PSS组:2.5[1.5-3.7]g vs 非PSS组:2.0[1.4-2.7]g)(表3)。集中病理复核与全国各地方病理中心的牛津分型比较显示,所有指标的Kappa值(范围为–1到+1,kappa值越高代表一致性越强)均<0.40(M:0.1,E:0.2,S:0.1,T:0.3,C:0.1),专业病理医师间的一致性分析对特殊S病变亚型具有中高度判读一致性。
表3. 集中病理复核的牛津分型与临床指标的相关性
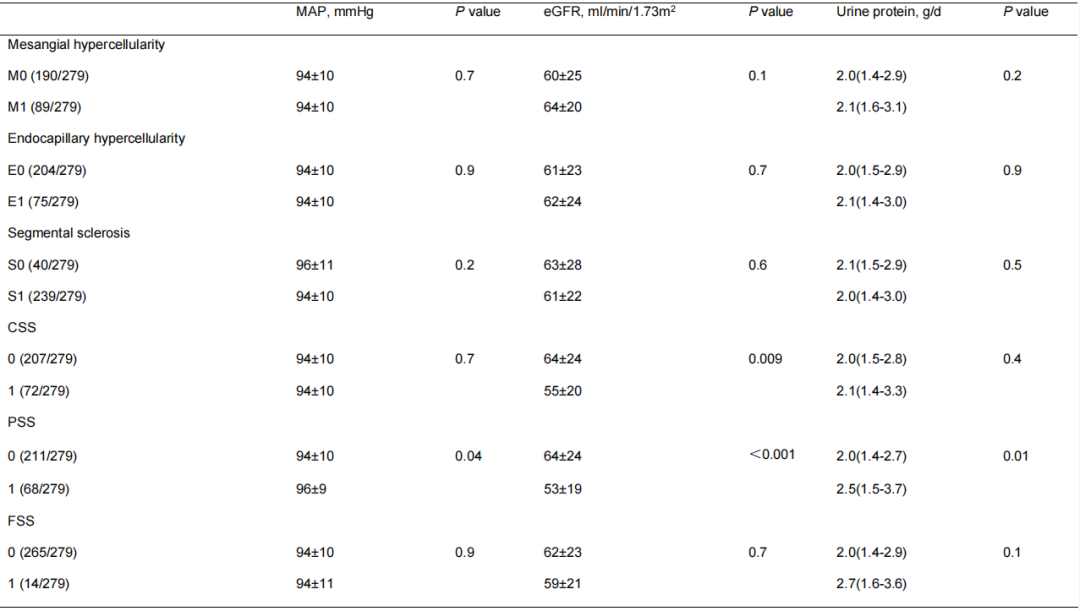
eGFR:估算肾小球滤过率;MAP:平均动脉压;M:系膜细胞增生;E:内皮细胞增生;S:节段性硬化;T:肾小管萎缩/间质纤维化;C:细胞性/纤维细胞性新月体;CSS:细胞性节段性硬化;PSS:足细胞病性节段性硬化;FSS:纤维性新月体节段性硬化
a:由于T2或C2病变的受试者数量有限,分析时将T1与T2病变、C1与C2病变合并计算
对279例受试者进行集中病理复核后,根据不同的牛津分型进行亚组分析,评估甲基强的松龙相对于安慰剂的疗效差异。结果显示:
-M、E、S、T病变亚组:M0与M1、E0与E1、S0与S1、以及T0与T1/2亚组间,糖皮质激素治疗组与安慰剂组的肾脏终点事件风险均未呈现显著差异;
-C病变亚组:虽P值未达统计学意义(P=0.4),但观察到C1/2病变患者可能从糖皮质激素治疗中获益更显著(C0组HR=0.6[95%CI:0.4-0.9];C1/2组HR=0.05[95%CI:0.008-0.3])。值得注意的是,C1/2病变治疗组的95%Cl与C0组完全无重叠,提示可能存在显著临床差异(图3)。多变量分析显示,甲基强的松龙治疗组中C1/2病变患者的风险虽低于C0病变患者(HR=0.3[95%CI:0.08-1.3],P=0.1),但差异无统计学意义。
-评估三种S病变亚型的糖皮质激素疗效,结果显示(图4):
1. CSS病变:该亚型患者从糖皮质激素治疗中获益显著(CSS组HR=0.2[95%CI:0.07-0.4];非CSS组HR=0.6[95%CI:0.4-1.0])(P=0.03)
2. PSS病变:虽然PSS组患者显示更低的肾功能衰竭风险(PSS组HR=0.2[95%CI:0.07-0.4];非PSS组HR=0.6[95%CI:0.4-1.0]),但组间差异无统计学意义(P=0.3)
3. FSS病变:因样本量不足未进行统计分析。
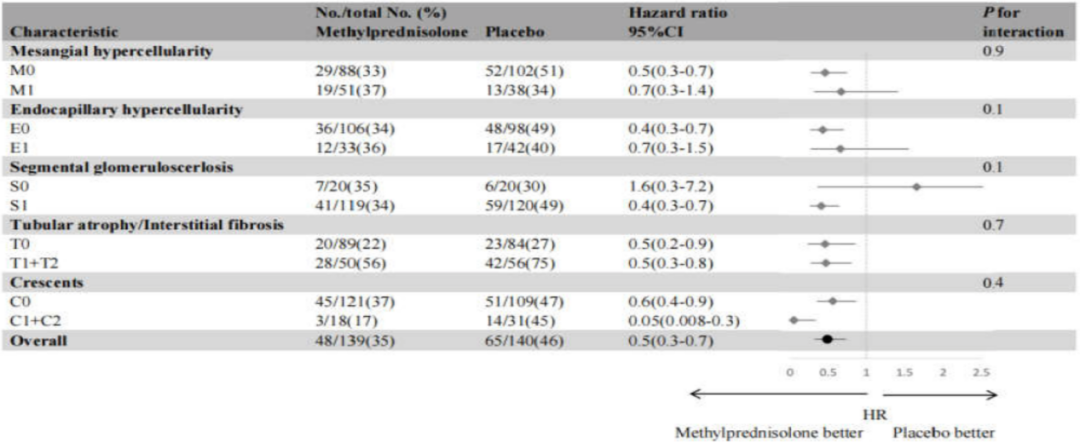
图3. 甲基强的松龙治疗对TESTING研究中279例中国受试者基于集中病理复核牛津分型分层结局的影响
校正因素:年龄、性别、基线估算肾小球滤过率、尿蛋白水平及除待检验变量外的其他中央病理复核MEST-C评分
M:系膜细胞增生;E:内皮细胞增生;S:节段性硬化;T:肾小管萎缩/间质纤维化;C:细胞性/纤维细胞性新月体;CI:置信区间
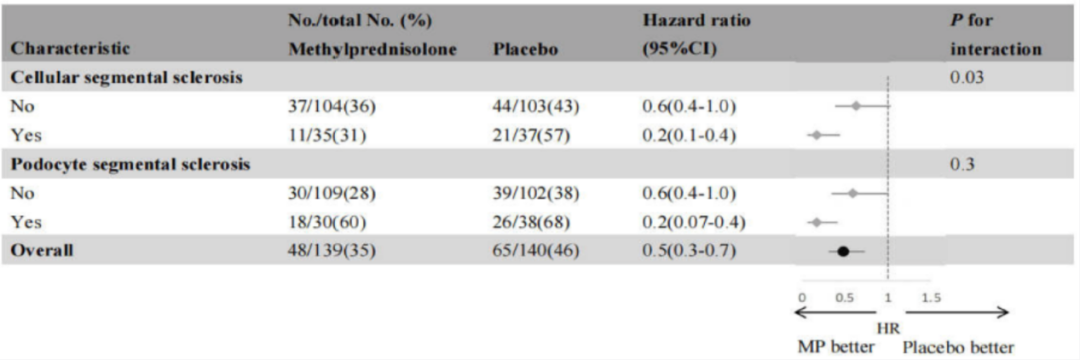
图4. 甲基强的松龙治疗对基于集中病理复核CSS和PSS病变分层的复合肾脏结局的影响
校正因素:年龄、性别、基线估算肾小球滤过率(eGFR)、尿蛋白水平,以及当地病理报告中除待检验变量外的M、E、T、C评分和CSS、PSS、FSS病变
M:系膜细胞增生;E:内皮细胞增生;S:节段性硬化;T:肾小管萎缩/间质纤维化;C:细胞性/纤维细胞性新月体;CSS:细胞性节段性硬化;PSS:足细胞节段性硬化;CI:置信区间;MP:甲基强的松龙
在TESTING试验的全部379例中国受试者中,195例治疗组与184例安慰剂组的临床指标及牛津分型均无显著差异。研究根据当地病理牛津分型进行亚组分析,评估甲基强的松龙在不同亚组中的疗效差异。结果显示,在M0与M1、E0与E1、S0与S1以及T0与T1/2亚组间,糖皮质激素治疗组与安慰剂组的肾脏终点事件风险均无显著差异。然而,在379例中国受试者的当地病理牛津分型分析中,新月体病变亚组存在显著差异(C0组:HR=0.7[95%CI:0.4-1.2];C1组:HR=0.3[95%CI:0.2-0.6];C2组:HR=0.2[95%CI:0.08-0.7];P值=0.05)(图5)。多变量分析进一步表明,甲基强的松龙治疗组的复合终点风险显著降低,尤其在C2亚组中更为明显(C1组:HR=0.9[95%CI:0.6-1.6];C2组:HR=0.3[95%CI:0.1-0.8];趋势P值=0.04)。
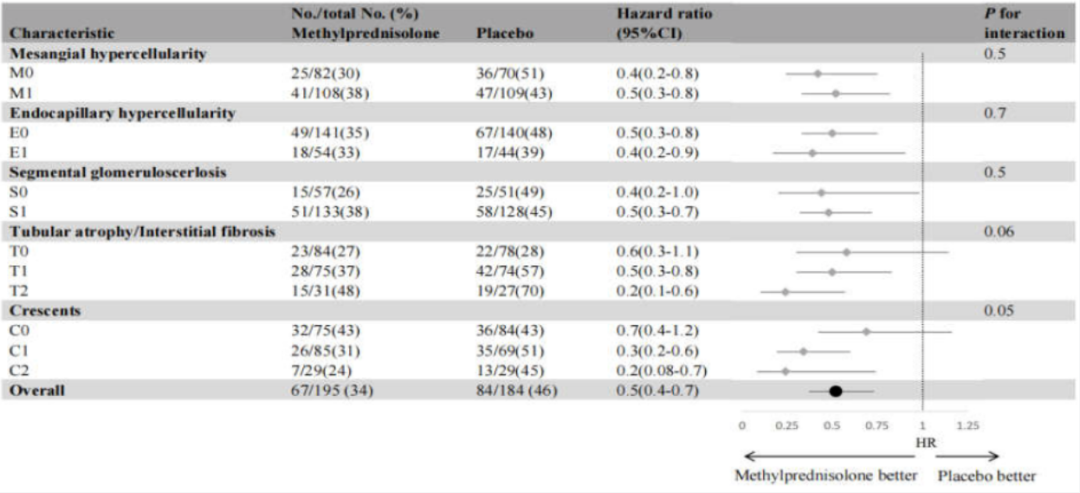
图5. 甲基强的松龙治疗对TESTING研究中379例中国受试者基于当地病理评估牛津分型分层结局的影响
校正因素:年龄、性别、基线估算肾小球滤过率(eGFR)、尿蛋白水平,以及当地病理报告中除待检验变量外的其他MEST-C评分
M:系膜细胞增生;E:内皮细胞增生;S:节段性硬化;T:肾小管萎缩/间质纤维化;C:细胞性/纤维细胞性新月体;CI:置信区间
本研究是首个评估IgAN牛津分型与糖皮质激素治疗疗效差异的前瞻性随机对照试验,且首次报道了节段性硬化的新亚型分类,发现经集中病理复核确认的细胞性节段性硬化(CSS)患者接受糖皮质激素治疗后肾脏结局显著优于非CSS患者,同时新月体病变患者也显示出更好的疗效。虽然足细胞病性节段性硬化(PSS)患者在糖皮质激素治疗组中也显示出较低的风险比,但这一差异无统计学意义,可能与样本量较小有关。
研究最重要的发现是:节段性硬化病灶内的炎症/细胞增生与糖皮质激素治疗的显著获益相关。这一结果提示肾活检可能区分两类患者:进展性炎症性肾小球病变患者——可从激素治疗中获得显著获益,与自限性肾小球炎症患者——病变不会进展至硬化,激素治疗必要性可能较低。
本研究仍存在以下局限性:作为中国人群亚组分析,结果需在其他人群验证;排除了快速进展性肾炎患者且C1/C2病例有限;病理报告的时代差异可能影响评分一致性。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)