前言
近期,《Nephrol Dial Transplant》杂志发布了一篇综述“The Gut Microbiome as a potential therapeutic target in IgA Nephropathy”(IF=5.6),基于IgA肾病的病理生理机制,系统阐述人类肠道微生物组在IgA肾病发病机制中的研究进展,并探讨其作为未来治疗干预靶点的潜在价值。
IgA肾病的病理生理机制尚未完全阐明,多数病例仍属于特发性。值得注意的是,该病常继发于上呼吸道或胃肠道感染,并与多种自身免疫性疾病相关,包括
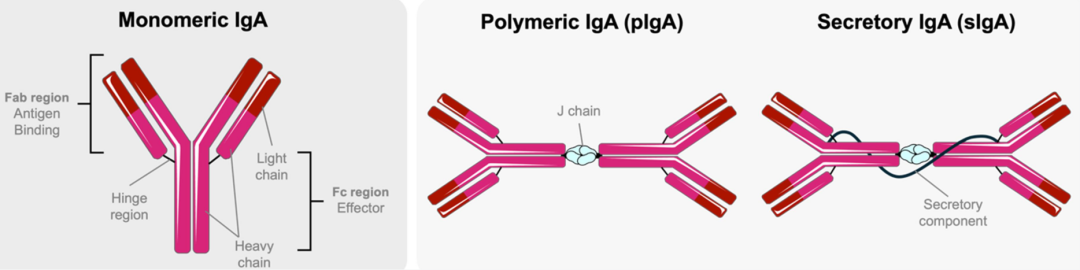
图1. 人类免疫球蛋白A(IgA)结构示意图
单体IgA由两条重链和两条轻链组成,铰链区连接抗原结合区(Fab)和效应区(Fc)。多聚体IgA(pIgA)通常由两个IgA单体通过J链连接而成。当pIgA转运至黏膜表面时,与分泌成分结合形成分泌型IgA(sIgA),可抵抗酶降解作用。
最新研究表明,IgA肾病的病理生理机制是一个复杂的多步骤致病过程,可理解为“多重打击”模型(图2):
第一重打击是lgA肾病患者循环中存在高水平的半乳糖缺失的IgA1(Gd-IgA1);
第二重打击是Gd-IgA1作为自身抗原诱发自身抗体的产生(抗糖抗体);
第三重打击为抗糖抗体和半乳糖缺失的IgA1二者形成循环免疫复合物在肾脏沉积;
第四重打击则是通过激活补体、诱发炎症因子等途径致肾组织损伤,导致IgA肾病的发病和进展。其中,循环中Gd-IgA1的产生增加是IgA肾病的始动因素。
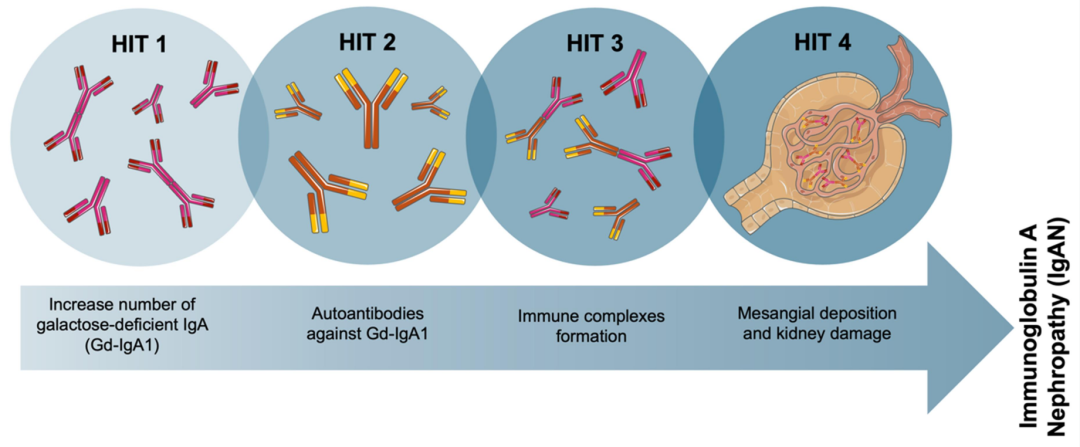
图2. IgA肾病发病机制的"四重打击"理论
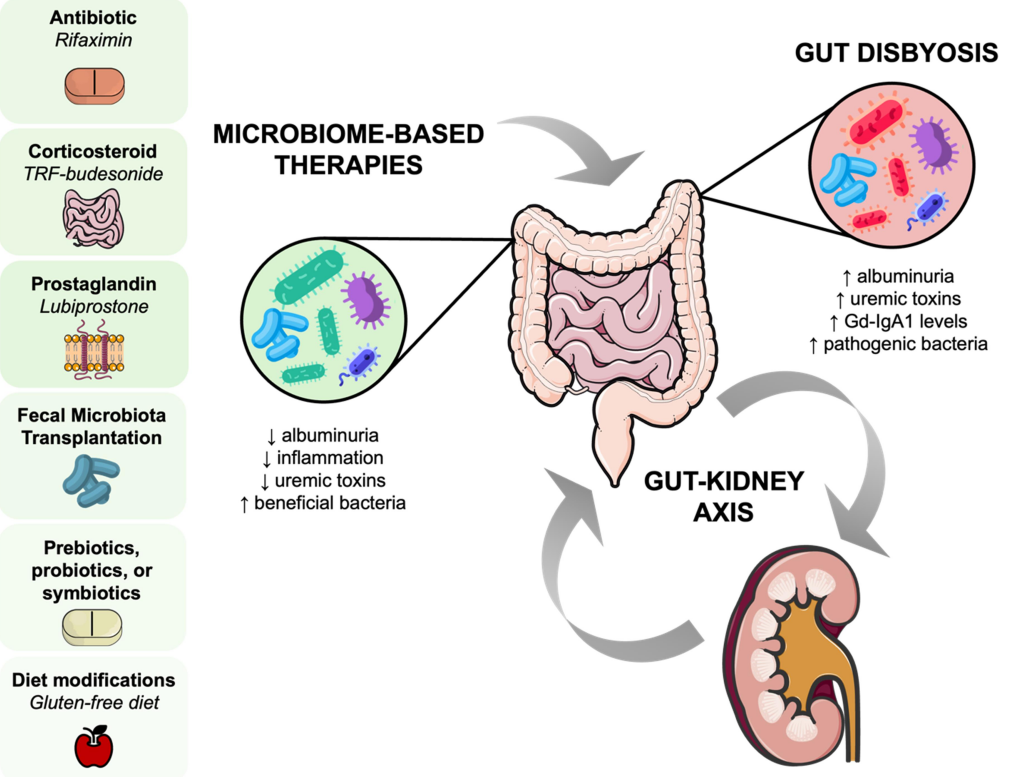
近期研究表明,微生物组与肾脏之间的相互作用是IgA肾病发病机制的关键环节。人体共生微生物组主要由拟杆菌门(Bacteroidetes)、厚壁菌门(Firmicutes)和放线菌门(Actinobacteria)构成,总数约10^14个细菌。这一复杂的动态生态系统不仅参与营养代谢,还调控免疫平衡。当
于2011年提出的"肠-肾轴"理论揭示了肠道与肾脏的双向联系:肾功能不全可导致菌群失调,产生
多聚体IgA(pIgA)是黏膜相关淋巴组织(MALT)产生的最丰富的抗体亚型,作为人体黏膜防御的第一道防线,既能中和病原体和毒素,又能维持对共生菌的免疫耐受。派尔集合淋巴结是肠道重要的淋巴组织,通过分泌型IgA(sIgA)介导黏膜免疫应答,其内的
前文提到,上呼吸道或胃肠道感染常先于IgA肾病发作,其机制可能涉及病原体直接作用于肾小球。例如,在儿童IgA肾病患者中,化脓性链球菌的毒力蛋白(M蛋白)可与系膜区IgA沉积共定位。
2014年De Angelis团队首次证实肠道菌群失调与IgA肾病的关联,发现疾病进展患者存在特定的菌群特征:瘤胃菌科、毛螺菌科等比例升高。最新研究还发现IgA肾病患者肠道中阿克曼菌显著增多,该菌能促进IgA1去糖基化并产生新抗原表位,进而通过IL-10和sIgA等促炎因子加剧疾病进展。此外,相关研究还发现放线菌丰度与蛋白尿程度及预后相关;IgA肾病患者埃希菌-
2017年Fellström团队开展的临床试验为证实IgA肾病与肠道黏膜菌群及免疫的内在联系提供了关键证据。研究者采用新型靶向释放制剂
抗生素
1. 广谱抗生素
研究团队在IgA肾病人源化小鼠模型中发现,广谱抗生素治疗能显著减少系膜区IgA1沉积、肾小球炎症和蛋白尿发生,这些疗效与粪便菌群负荷降低显著相关,研究证实了肠道菌群对IgA1-IgG免疫复合物形成及IgAN发病的关键作用。但广谱抗生素导致的抗生素耐药性等副作用可能限制了其临床应用。
2. 靶向抗生素
肠道调节剂
1. 前列腺素类药物
鲁比前列酮作为2型氯通道激活剂,在治疗IgA肾病患者慢性便秘时意外发现可降低尿蛋白排泄和镜下血尿。这一效应已在慢性肾脏病小鼠模型中得到验证,提示其可能通过调节肠道-肾脏轴发挥治疗作用。
2. 免疫调节药物
羟氯喹(HCQ)通过抑制黏膜及肾脏TLRs信号通路显示潜在疗效。一项随机对照试验表明,HCQ联合RAAS抑制剂治疗6个月可显著减少IgA肾病患者蛋白尿。动物研究进一步证实,HCQ能降低Gd-IgA1水平、改善菌群紊乱和免疫功能障碍,为难治性病例提供了附加治疗选择。
3. BAFF/APRIL靶向治疗
针对BAFF/APRIL系统的生物制剂取得突破性进展:
BRIGHT-SC试验中,BAFF抑制剂blisibimod联合标准治疗显著降低蛋白尿;靶向APRIL的单抗sibeprenlimab、zigakibart相关研究证实其可显著降低蛋白尿;双靶点抑制剂atacicept在IIb期试验中显示可降低Gd-IgA1、稳定肾功能,目前正开展III期研究。
4. 粪菌移植(FMT)
FMT在重建肠道菌群多样性方面展现独特优势:
人源化IgA肾病小鼠接受健康供体FMT后,炎症浸润和蛋白尿显著减轻;2例难治性IgAN患者经FMT治疗后24小时尿蛋白下降、血清白蛋白升高且肾功能稳定;目前正在开展FMT治疗难治性IgA肾病的干预性研究。
5. 微生态制剂
益生菌/元通过调节肠-肾轴发挥治疗潜力:
双歧杆菌水平与IgA肾病严重程度负相关,补充益生菌可改善菌群构成并降低尿蛋白/肌酐比值;布拉氏酵母菌能减少系统性IgA产生,预防疫苗诱导的IgA肾病。
6. 饮食干预
无麸质饮食在继发于乳糜泻的IgA肾病患者中显示疗效:
原发性IgA肾病患者采用无麸质饮食6个月后,循环免疫复合物减少,蛋白尿和镜下血尿显著改善。
其他药物
上文提到,靶向释放布地奈德能显著改善IgA肾病患者预后,已获美国FDA批准用于减少原发性IgA肾病患者肾功能下降。目前我国正在开展布地奈德肠溶胶囊联合益生菌的随机对照试验,这种创新组合疗法值得期待。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)