
2025年6月4-7日在奥地利维也纳举办的第62届欧洲肾脏协会大会-欧洲肾脏病年会,由欧洲肾脏协会(ERA)主办,以“肾脏学的变革者”为核心主题,邀请了国际专家及知名关键意见领袖共襄盛会。
2024年KDIGO

战略压制:扑灭APRIL级联,减少肾小球免疫复合物,快速打击持久抑制
Zigakibart是一种结合并阻断增殖诱导配体(APRIL)的新型人源化单克隆抗体,通过阻断APRIL与其受体的作用,耗竭降低致病性半乳糖缺陷型IgA1(Gd-IgA1)的产生,并阻断致病性免疫复合物的生成,进而改变IgAN病程。
ADU-CL-19是一项正在进行中的Zigakibart I/II期试验。2025年欧洲肾脏协会(ERA)会议展示了IgAN患者治疗100周的疗效数据,这是目前抗APRIL类药物治疗周期最长的报道1。研究发现,Zigakibart持续抑制IgA(治疗第100周下降74%)、IgM(治疗第100周下降80%)、和Gd-lgA1(治疗第76周下降74%)(图1A),其中Gd-lgA1为同类已发表药物中降幅最大;IgG下降不明显(治疗第100周降低39%),尿蛋白较基线降低60.4%(图1B),55.2%的患者尿蛋白排泄量(UPE)降至严格阈值<500毫克/24小时以下1。研究观察到估算的肾小球滤过率(eGFR)持续稳定(图1C)。Zigakibart耐受性良好,治疗100周后无导致研究药物停用或死亡的不良事件1。
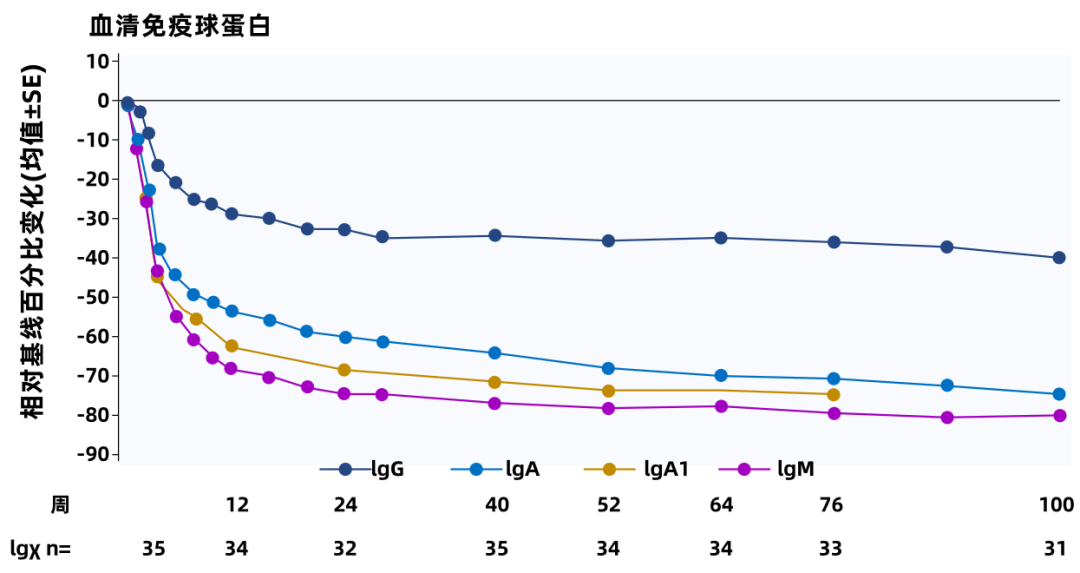
图1A. 血清免疫球蛋白随时间变化
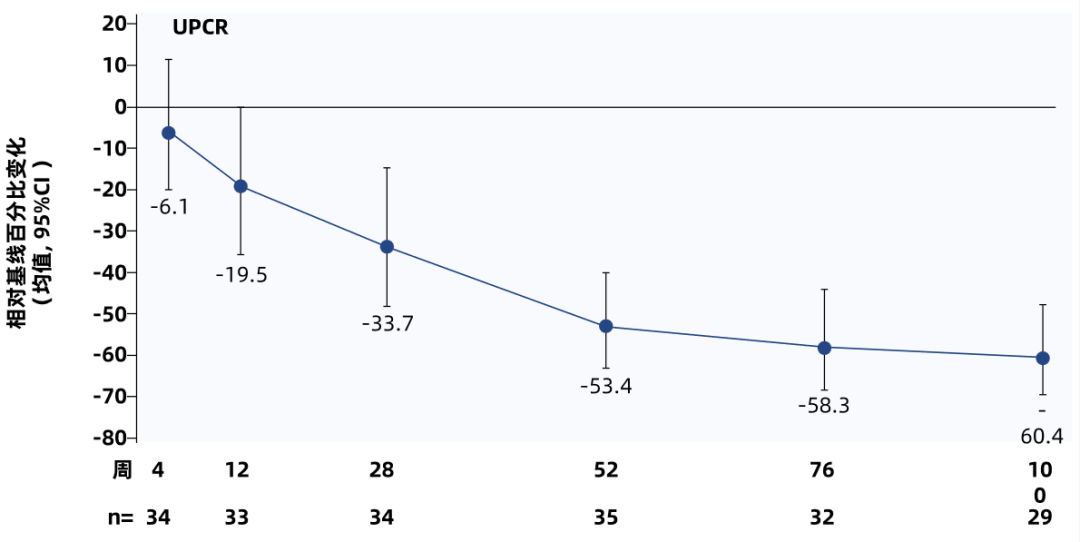
图1B. UPCR随时间变化
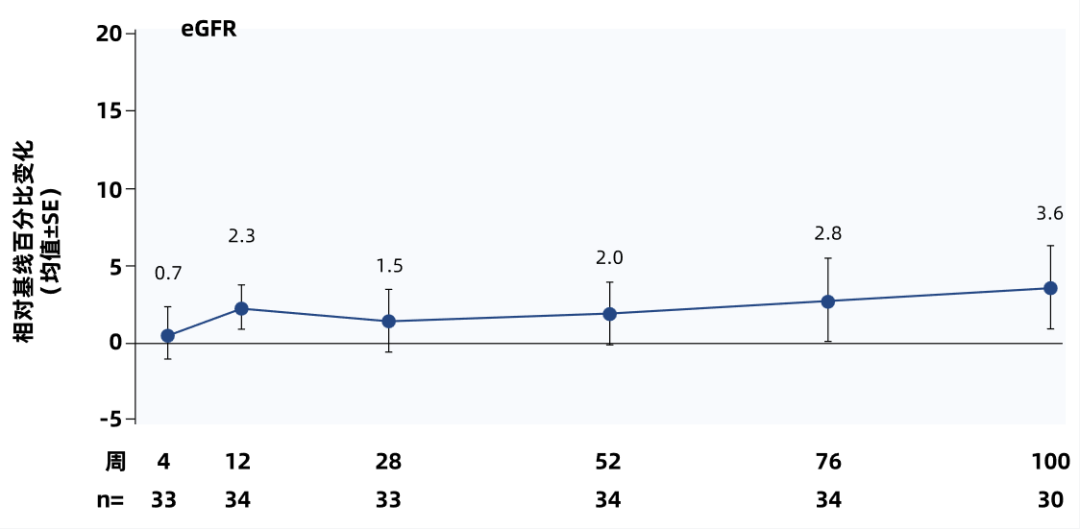
图1C. eGFR随时间变化
大会公布了一项系统性分析与Meta分析结果,通过系统检索PubMed、Cochrane Central和Embase数据库建库至2024年12月25日的相关文献,纳入比较
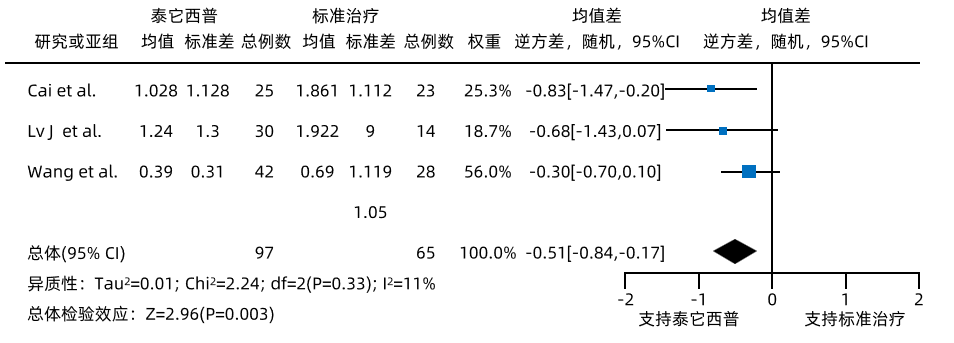
图2A. 泰它西普组与标准治疗组24小时尿蛋白差异森林图

图2B. 泰它西普组与标准治疗组eGFR差异森林图

梦幻联动:遏制补体旁路强效抗炎,长期调控精准治疗
补体旁路途径(AP)过度激活是引起肾小球炎症的重要关键因素,并进一步导致肾小管间质损伤。强效口服
这项II期研究分为两个部分:第一部分治疗90天,第二部分治疗180天3。研究发现,研究第一部分伊普可泮治疗90天组的尿蛋白/肌酐比(UPCR)较基线(BL)降低30%(95%CI: 13.5%-43.4%),停药30天内恢复至BL水平;而第二部分伊普可泮治疗180天的UPCR较BL降低35.4%(95%CI: 17.5%-49.5%),停药30天后UPCR仍低于BL,但高于治疗结束(EoT)时水平。OLE研究中重启伊普可泮治疗后,两部分患者的UPCR均再次下降(图3A、图3B)3。
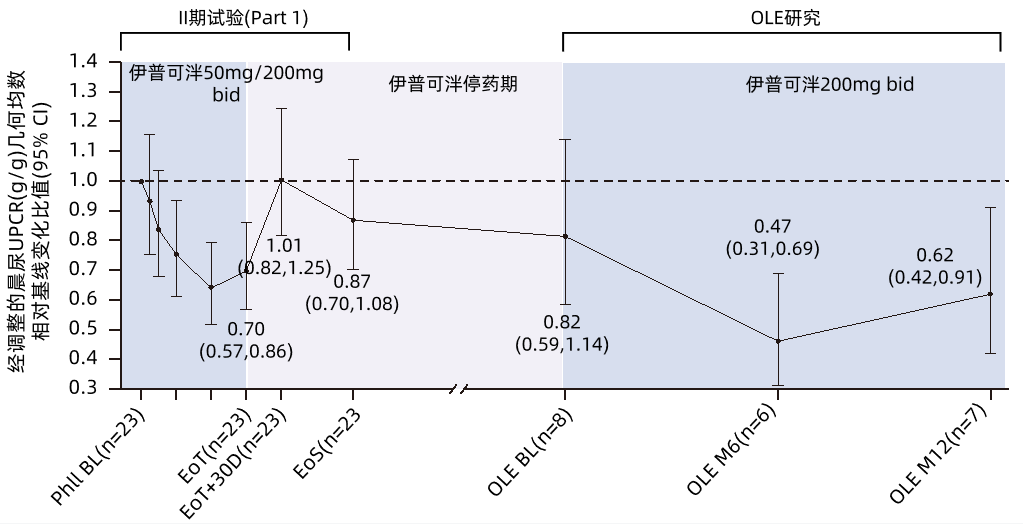
图3A.II期研究Part 1至OLE第12月(M12)伊普可泮50/200mg治疗组UPCR变化值
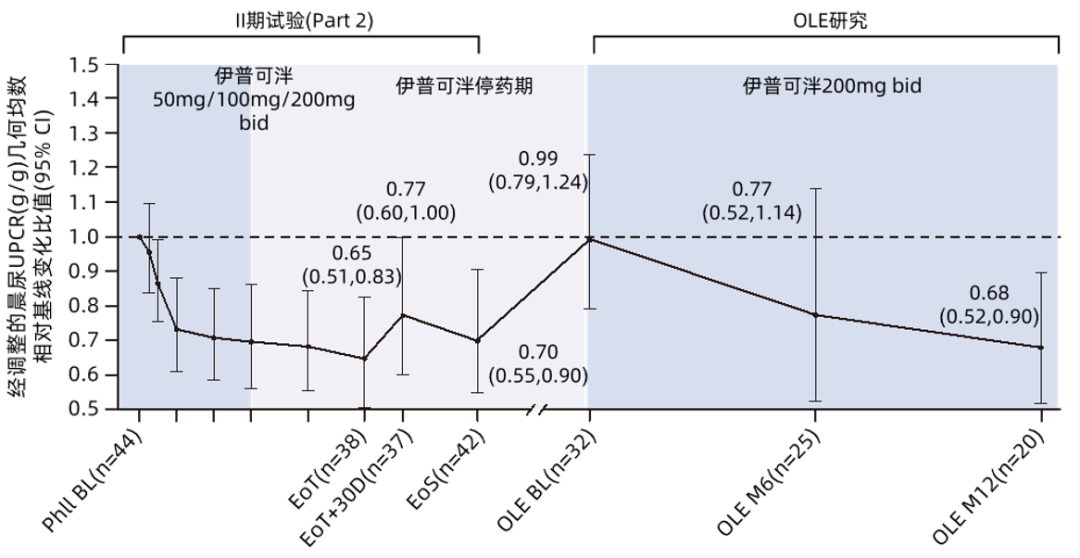
图3B. II期研究Part 2至OLE第12月(M12)伊普可泮50/100/200mg治疗组UPCR变化值
此外,在200mg bid治疗组患者中发现,D90相对基线AP标志物(从基线到D90的中位数[四分位距(IQR)]降低:尿sC5b-9 97.2%[89.3%, 98.4%];血浆Bb:24.5%[13.6%, 40.6%])下降,首次停药随访时AP标志物升高(较基线中位数[IQR]: 尿sC5b-9升高18.3%[-77.8%, 168.8%];血浆Bb升高3.3%[-12.7%, 11.2%])3。
值得注意的是,研究中停药后重新启动伊普可泮治疗,观察到UPCR再次下降,提示患者对补体抑制持续敏感,应持续应用补体抑制剂控制蛋白尿水平。
大会还公布了一款靶向AP关键蛋白因子B(FB)mRNA的反义核苷酸(ASO)药物Sefaxersen的II期研究数据(NCT04014335)4。FB在IgAN患者中表达升高,与蛋白尿及肾功能恶化显著相关。研究发现该疗法支持Q4W皮下给药的理想药代动力学特征,持久降低血液和尿液中AP成分。达稳态时患者血浆FB平均降低69%、Bb降低79%,尿液Ba降低78%,治疗9周后AP活性降低39%,而经典通路活性保持稳定。

实力破局:围剿内皮素受体,稳定肾小球滤过,跨越分型兼容优选
内皮素(ET-1)通过激活内皮素A受体参与IgAN的蛋白尿、炎症及纤维化进程。阿曲生坦是一种强效且高选择性的内皮素A受体拮抗剂,2025年4月已获FDA加速批准,用于降低有疾病进展风险的原发性IgAN成人患者的蛋白尿。本次ERA大会发布了ALIGN研究的事后分析结果。ALIGN是一项随机、双盲、安慰剂对照的全球III期临床试验,旨在评估阿曲生坦对比安慰剂在有肾功能进行性丧失风险的IgAN成人患者中的疗效和安全性5。
研究主要队列纳入经肾活检确诊、接受最大耐受剂量肾素-血管紧张素抑制剂治疗且蛋白尿≥1g/天的IgAN患者。在预设的36周中期分析中,对于接受支持治疗的IgAN患者,阿曲生坦对比安慰剂在降低蛋白尿(主要终点)方面已显示出有临床意义的优势:治疗36周后,与安慰剂相比,阿曲生坦蛋白尿显著降低(36.1%;95% CI:26.4%,44.6%;p<0.0001)。中期分析中的160例IgAN患者纳入此次基于MEST-C评分的事后分析。基线UPCR<1g/g和≥1g/g的患者中,蛋白尿降低幅度(36周时相对于安慰剂的UPCR变化最小二乘均数百分比)分别为-28.7(95% CI:-47.5,-3.2)和-38.3(95% CI:-47.4,-27.5)(图4)。此外,无论MEST-C评分、基线血尿水平及基线24小时UPCR水平如何,阿曲生坦均显著降低蛋白尿水平(图4)5。此次更新的数据进一步支持阿曲生坦在不同蛋白尿水平以及不同肾损伤程度的IgA肾病患者中的疗效。
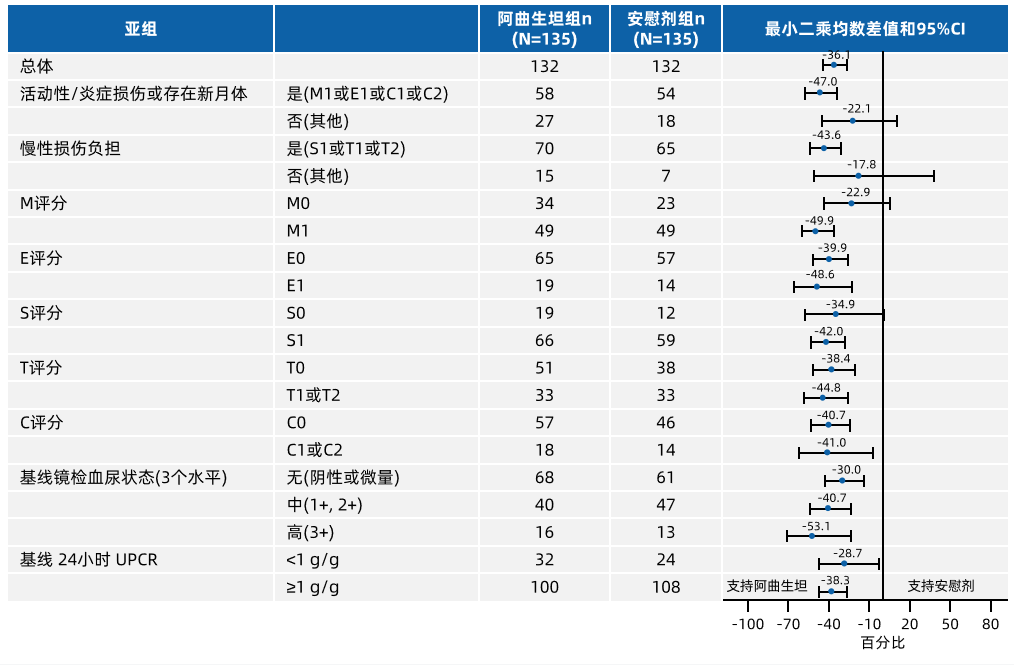
图4. 根据MEST-C评分、基线血尿和蛋白尿水平,第36周UPCR相对基线的最小二乘均值变化百分比:混合效应回归模型(MMRM)分析(意向性分析集,IA ITT分析集)
一款非免疫抑制性双重内皮素和血管紧张素II受体阻滞剂司帕生坦III期研究的OLE研究结果也亮相于ERA大会6。在III期随机对照研究中完成2年双盲期的IgAN患者进入OLE研究接受司帕生坦治疗,治疗48周后UPCR中位数(四分位距)从1.30(0.71-2.13)g/g降至0.60(0.29-1.09)g/g,降幅达54%(图5)。OLE期估算肾小球滤过率eGFR变化斜率与双盲期一致。不良事件发生率低,未出现新的安全性信号或肝毒性问题。研究结果表明,对于既往2年曾接受最大耐受剂量血管紧张素受体阻滞剂(ARB)治疗的IgAN患者,司帕生坦的应用表现出显著疗效和良好耐受性。
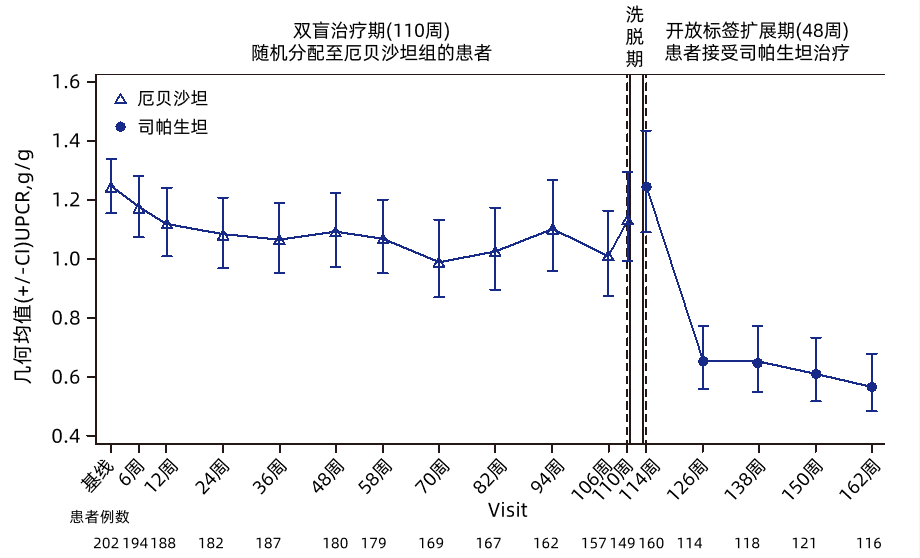
图5. 随机分配至厄贝沙坦组的患者UPCR几何均值随时间变化
2025 ERA大会报告了Zigakibart、伊普可泮、阿曲生坦、泰它西普等创新药的最新临床证据,这些创新药物从不同作用机制出发,在IgAN治疗中展现出良好疗效与安全性,有望为IgAN的疾病管理提供新选择,也预示着IgAN治疗正迈向充满前景的新阶段。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)