慢性乙型肝炎(CHB)患者长期接受核苷(酸)类似物(Nuc)治疗虽可实现HBV抑制、ALT复常、组织学改善及延缓肝病进展,但很少实现
目前,
然而,Nuc对共价闭合环状DNA(cccDNA)及整合HBV DNA(iDNA)无直接作用,而这两者是HBV及其蛋白持续转录的稳定且持久的模板。因此,即使长期维持HBV DNA抑制,HBsAg仍持续产生。值得注意的是,iDNA为HBeAg阴性患者HBsAg的主要来源:其转录的高水平HBsAg可能导致T/B细胞耗竭,而病毒基因整合入肝细胞DNA更可能参与肝癌发生。一项数学建模研究表明,大多数HBeAg阴性患者需要几十年的Nuc治疗才能实现HBsAg清除。一项纳入4769例HBeAg阴性患者的国际真实世界队列研究证实,在ETV/TDF治疗期间,10年HBsAg清除率仅为2.1%。
鉴于当前一线Nuc的良好疗效和安全性,长期维持Nuc治疗下的HBV抑制被视为令人满意的治疗目标。然而相关研究发现,即便长期/终身Nuc治疗无安全性顾虑且HBV抑制率达100%,持续Nuc治疗但HBsAg仍保持阳性者的长期预后仍显著劣于HBsAg清除者。因此,推动HBsAg清除已成为推荐有限疗程治疗或“停药以求治愈”策略的主要依据。
另一方面,若充分知情且依从性良好的HBsAg阳性患者更倾向维持药物控制下的安全状态,而不愿承担停药后HBV复发的风险,持续治疗仍属合理选择。
欧美指南虽将有限疗程策略纳入HBeAg阴性CHB的条件性治疗策略,但仅适用于治疗前非肝硬化患者。鉴于晚期肝病患者的肝功能储备较差,主要顾虑停药后严重肝炎发作、肝失代偿及
APASL与EASL指南在HBeAg阴性CHB患者停药标准上存在差异,包括巩固治疗时长(>1年vs.>3年)及相应总疗程(>2年vs.>4年)。然而,巩固治疗时长对停药后复发率的影响尚未明确。但亚洲和欧洲的研究结果显示,二者的复发率无明显差异。一项系统综述显示,巩固治疗> 2 年的CHB患者,停药后病毒学复发率低于巩固治疗≤2 年的患者;中国台湾地区一项研究显示,ETV停药前巩固治疗< 2 年和≥2 年的患者,临床复发率无明显差异,而TDF停药前巩固治疗≥2 年的患者,复发率更低。
停药决策除考量巩固时长外,更需关注其他降低复发的因素。一项 ETV 研究显示,治疗前 HBV DNA≤2×105IU/mL 的患者,1年复发率显著更低(29% vs. 53%,P=0.036)。近期一项研究显示,治疗前HBV DNA<2×104 IU/mL 的患者,临床复发率更低(22% vs. 60%),HBsAg 清除率更高(17.5% vs. 5%,P<0.001)。此外,治疗结束时定量HBsAg(qHBsAg)、乙肝核心相关抗原(HBcrAg)及HBV RNA水平较高的患者,停药后肝炎发作风险更高。值得注意的是,一项头对头研究证实,qHBsAg在预测患者停药后复发方面优于HBcrAg,其临床复发的风险比为2.4(P<0.001)。
目前治疗结束时的qHBsAg(EOT qHBsAg)已成为预测HBsAg清除与停药复发的最佳指标。多项研究证实,qHBsAg<100 IU/mL为停药后低复发风险的预测指标。治疗结束时qHBsAg <100 IU/mL也是停药后HBsAg清除的预测指标。此外,有研究报道,治疗期间qHBsAg降幅>1 log10 IU/mL可预测停药后HBsAg清除。需注意,这些预测因子虽为医患共同决策提供重要依据,但不可作为Nuc停药的绝对指征或禁忌。
规范监测对保障停药安全以及确保及时再治疗至关重要。停药后监测方案建议:前3个月每1-1.5个月检测ALT,此后每3个月检测;HBV DNA检测于3-12个月间进行,后续每3-6个月复查。若出现HBV DNA和/或ALT升高(尤其ALT>5xULN),需每1-2周检测ALT、胆红素及国际标准化比值(INR),以便及时启动再治疗(图1)。资源有限地区建议采用简化监测方案(图1B),但该方案需进一步验证。
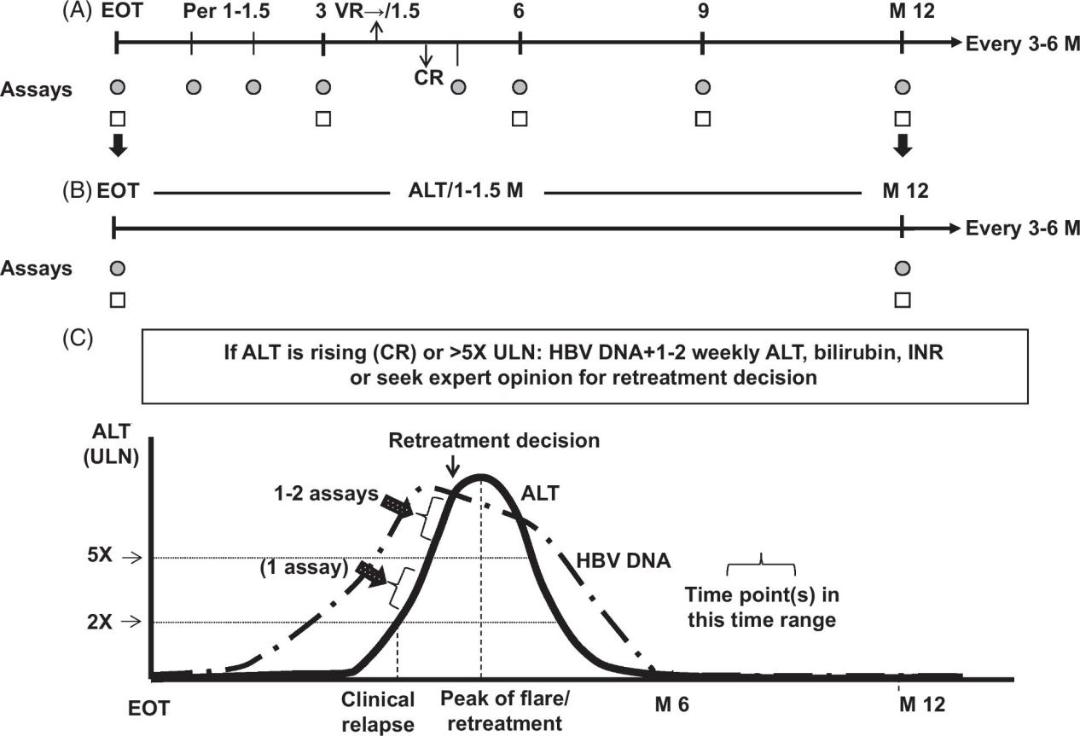
图1 停药后监测方案
注:(A)乙肝专科医师推荐方案;(B)非专科医师简化方案;(C)一旦HBV DNA(□)>2000 IU/mL(病毒学复发)和/或 ALT(●)升高(临床复发),必须加强监测以决定是否再治疗。定量HBsAg(⭣)检测有助于区分肝炎发作类型。若治疗结束后第1年内情况平稳无异常,可每3~6个月随访一次。
一般来说,停药后再治疗的适应症应与Nuc初治患者相似,即肝炎活动>3个月或出现肝炎发作时立即重启治疗。但具体实施中,是否所有ALT和/或HBV DNA超过某一阈值的肝炎发作患者均需再治疗,抑或仅当血清胆红素与INR升高或出现明显肝失代偿时才启动治疗,目前尚未明确。真实世界中,出于肝失代偿风险的安全考量,确诊肝炎发作者通常立即接受治疗(尤其ALT>10×ULN)。值得注意的是,多数肝炎发作为良性且可自行缓解,因此并非所有患者均需立即再治疗。已有研究提示,“不进行再治疗”可能成为后续HBsAg清除的重要影响因素,尽管接受再治疗与未接受再治疗的患者可能不具有可比性。HBeAg阴性患者临床复发或肝炎发作的理想再治疗指征及时机仍有待明确。
肝炎发作患者的再治疗时机需精准把握:既不能过晚以确保安全,也不可过早以保留充分的宿主免疫应答时间,促进HBsAg进一步下降甚至清除。qHBsAg被视为肝细胞内cccDNA与iDNA的替代标志物。因此,肝炎发作期间qHBsAg下降,可能是有效免疫应答减少iDNA的结果。
HBeAg阴性患者在ALT升高伴qHBsAg下降的发作,可能反映有效免疫反应相对于HBV/抗原的主导地位,可称为“宿主主导型发作”。此类患者若血清胆红素与INR正常,通常可自行消退(图2A),故可暂缓甚至无需抗病毒治疗。反之,若肝炎发作时ALT升高伴qHBsAg持续上升或维持高位(>2000 IU/mL),可能反映HBV和/或抗原相对于无效免疫反应的主导地位,新的iDNA形成伴随着免疫介导的炎症持续存在(图2B),此类“病毒主导型发作”常导致持续性/间歇性肝炎或肝失代偿,需启动Nuc治疗。通过ALT升高时检测qHBsAg,并在ALT>5xULN上限后复测1-2次,或有助于鉴别两种肝炎的发作(图1C)。若上述结果能得到其他研究证实,将充分证实联合监测 HBsAg/ALT动力学的临床价值,同时也支持“宿主主导型发作”患者无需接受 Nuc 治疗或可暂缓治疗以待进一步观察/评估的观点。
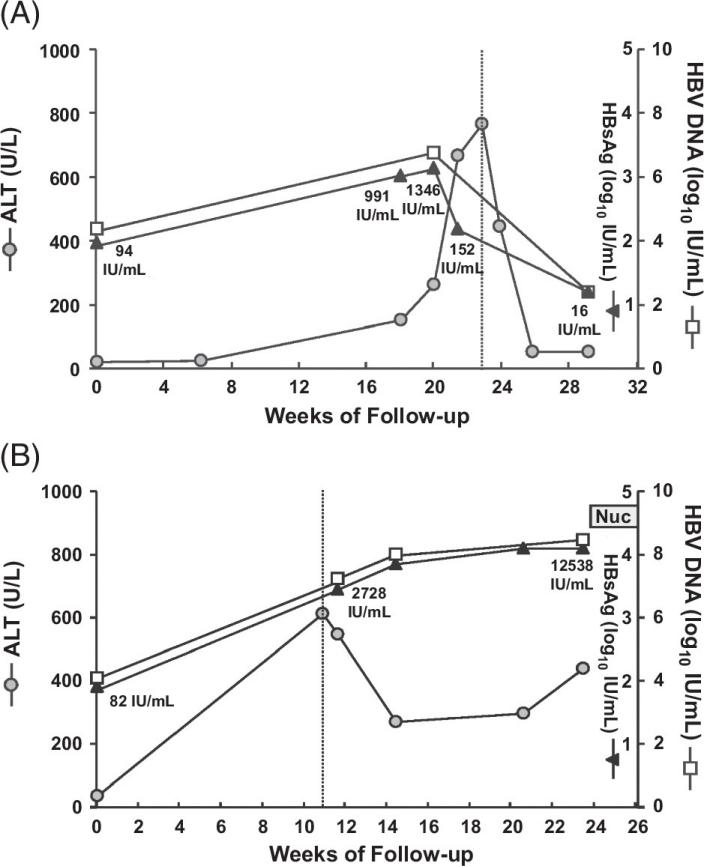
图2 乙型肝炎发作期间的HBsAg/ALT联合动力学
另一方面,也可根据HBV DNA而非qHBsAg变化,对停药后发作患者采取更简化的方法。近期一项停药后病毒动力学研究显示,HBV DNA 每月升高> 1 log10 IU/mL,可预测严重肝炎发作,阴性预测值为 87%;并且在停用ETV后的肝炎发作中,HBV DNA水平>6.6 log10 IU/mL也可预测需要立即Nuc再治疗以防止肝功能失代偿的严重发作。
Nuc药物(ETV/TDF/TAF)可使>95%的HBeAg阴性患者实现血清HBV DNA不可测、ALT复常、肝脏炎症缓解,并预防肝病进展及肝失代偿。但长期治疗期间qHBsAg降幅小,HBsAg清除率低。除消除长期治疗顾虑外,对持续HBV抑制者实施计划性停药可恢复免疫应答以促进HBsAg下降,使HBsAg清除概率逐步提升。停药后监测与再治疗决策对保障安全、避免中断充分免疫应答以促进HBsAg清除至关重要。
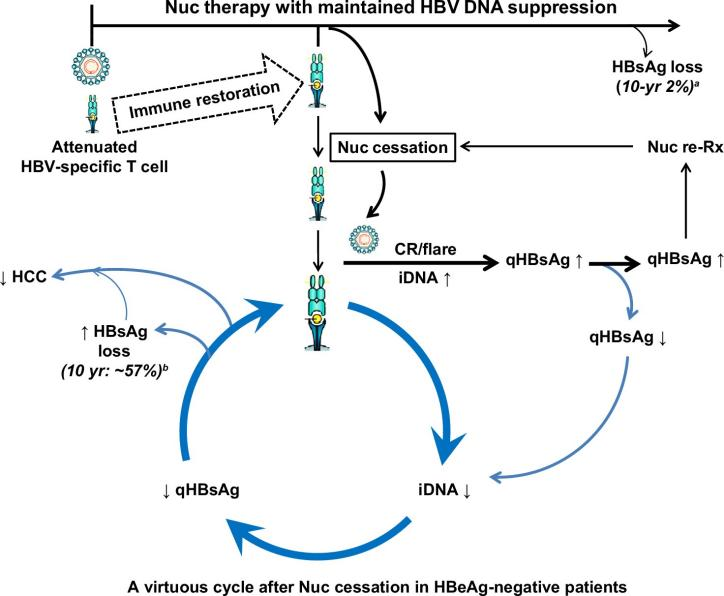
图3 HBeAg阴性患者有限疗程Nuc治疗以实现功能性治愈:停药后的良性循环
治疗期间严格遵医嘱用药与停药后坚持监测计划至关重要。建立医患信任与合作,并在共同决策前明确告知潜在获益与风险,是实现安全、成功的有限疗程策略的关键。
近数十年来,针对功能性治愈的新药研发进展未达预期,有限疗程策略目前仍是HBeAg阴性患者实现HBsAg清除及改善预后的更佳策略。该策略仍需进一步优化,同时亟待开发免疫学或更优病毒学生物标志物,以更好地预测复发和功能性治愈。
信源:Liaw YF, Papatheodoridis G. Finite nucleos(t)ide analog therapy for functional cure in HBeAg-negative chronic hepatitis B: Recent development in the paradigm shift. Hepatology. 2026 Mar 1;83(3):679-692.
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)