导语
➤Efimosfermin alfa的2a期临床试验结果于柳叶刀子刊发布;
➤国家药品监督管理局药品审评中心(NMPA)批准乙型肝炎病毒(HBV)特异性T细胞受体(TCR)工程化T细胞治疗——SCG101V新药1/2期临床试验(IND)申请,用于治疗慢性乙型肝炎。
在研MASH新药Efimosfermin alfa的2a期临床试验结果于柳叶刀子刊发布
代谢相关脂肪性肝炎(Metabolic dysfunction-associated steatohepatitis,MASH)是一种进行性疾病,其特征为脂肪变性、炎症和肝纤维化。成纤维细胞生长因子21(FGF21)被认为是治疗代谢相关脂肪性肝病(MASLD)及MASH的潜在靶点。FGF21通过调节脂质代谢、糖代谢及能量消耗,对代谢异常引起的损伤具有保护作用。然而,天然FGF21半衰期较短(约2小时),限制了其临床应用。Efimosfermin alfa(前称BOS-580、LLF580)是一种经工程化改造的长效人类FGF21变体,其半衰期延长至21天,可实现每4周给药一次。
近期,发表于Lancet Gastroenterol Hepatol(IF:38.6)的研究评估了多种剂量的efimosfermin和给药方案相较于安慰剂的安全性和耐受性,并评估其在表型 MASH 患者中疗效的探索性生物标志物。
这项多中心、随机、双盲、安慰剂对照2a期试验在美国12家医学中心进行,共纳入年龄18~75岁、体重指数(BMI)在30~45 kg/m²的MASH患者102例。将参与者随机分配至不同剂量及给药频率的efimosfermin组(图1):efimosfermin 75 mg每4周一次、75 mg每2周一次、150 mg每4周一次、150 mg每2周一次或300 mg每4周一次;或安慰剂组,均为皮下注射,治疗为期12周。
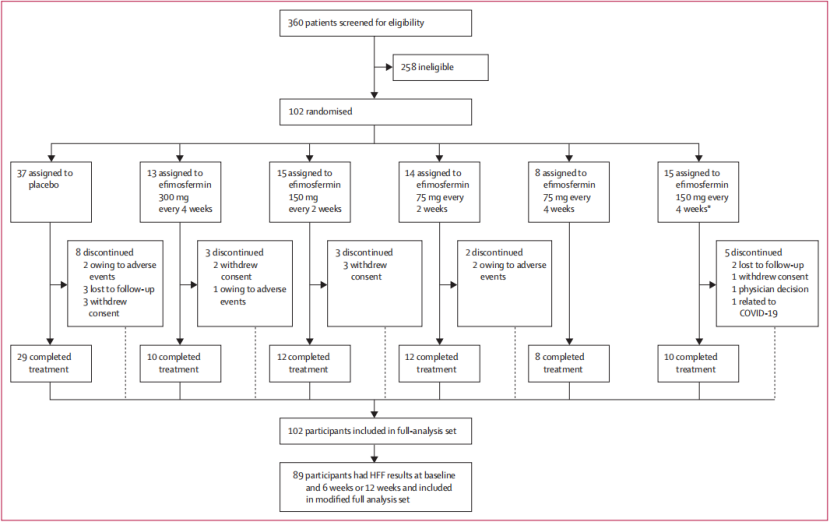
图1 参与者分布流程
结果显示12周时,53例可评估数据的接受efimosfermin治疗患者中47例(89%)肝脏脂肪分数(hepatic fat fraction,HFF)至少降低30%(图2):300mg 每4周一次组全部患者达到该降幅,75mg 每2周一次组和150mg每2周一次组均为92%,150mg每4周一次组90%,75mg每4周一次组63%;而安慰剂组30例中仅2例(7%)达到该降幅。
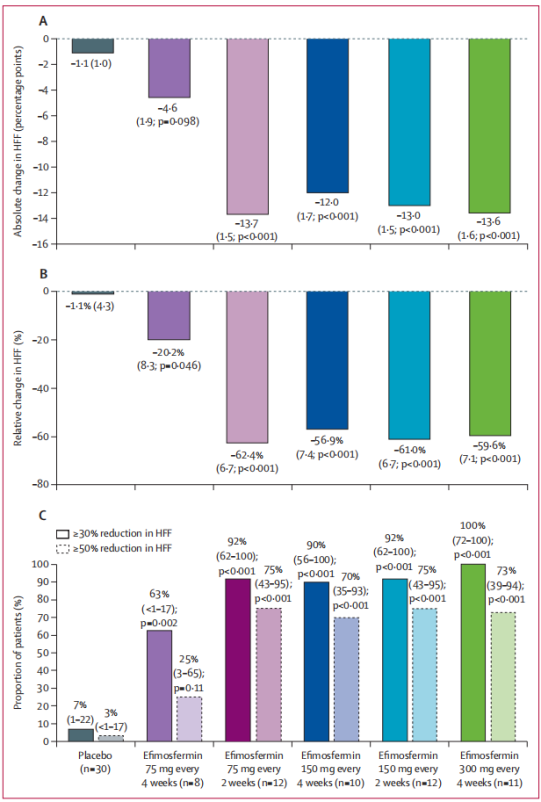
图2 HFF从基线至第12周的变化
安全性方面,65例接受 efimosfermin的患者中,43例(66%)出现治疗期间不良事件(TEAEs);安慰剂组37例中18例(49%)出现TEAEs。TEAEs多为轻至中度,可自行缓解。最常见的是胃肠道事件,包括恶心、呕吐、腹泻,无治疗相关死亡。
研究结果表明,efimosfermin具有良好的安全性并改善肝脂肪变性指标,结果为其后续治疗MASH的研究提供了重要支持。
NMPA批准SCG101V细胞疗法进入I/II期临床试验,用于治疗慢性乙型肝炎
7 月4日,NMPA批准星汉德生物自主研发的HBV特异性T细胞受体(TCR)工程化T细胞治疗——SCG101V新药1/2期临床试验(IND)申请,用于治疗慢性乙型肝炎。作为首个获得监管批准进入1/2期临床试验的研究性细胞疗法,SCG101旨在通过清除HBV感染肝细胞内的HBV共价闭合环状DNA(cccDNA)和整合HBV-DNA,从而治愈慢性乙型肝炎,这些是持续性感染和抗原产生的根本来源,受感染的肝细胞则是当前抗病毒治疗无法清除的长期病毒库。
此前,SCG101在HBV相关肝细胞癌患者中的1期临床试验显示,SCG101具有良好的安全性,并可实现血清乙型肝炎表面抗原(HBsAg)的持续清除,即使在既往接受过多种治疗的患者中也是如此。在接受治疗的患者中,94%的患者既往接受过核苷(酸)类似物(NA)的抗病毒治疗,72%基线时存在肝硬化。单次输注SCG101后,所有患者的HBsAg水平均快速下降,94%的患者在28天内降幅达到1.0-4.6 log10,HBsAg水平维持在100 IU/mL以下长达1年未反弹。此外,23%的患者达到HBsAg完全清除。
参考资料
1. Loomba R, Kowdley KV, Rodriguez J,et al. Efimosfermin alfa (BOS-580), a long-acting FGF21 analogue, in participants with phenotypic metabolic dysfunction-associated steatohepatitis: a multicentre, randomised, double-blind, placebo-controlled, phase 2a trial. Lancet Gastroenterol Hepatol. 2025 Aug;10(8):734-745.
2. https://www.scgcell.com/newsinfo/8509965.html
3. https://www.cde.org.cn/
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)