Metadata Card
文献题目:A cooperative release of mitochondrial DNA from platelets and neutrophils drives an interferon signature in systemic sclerosis
发表期刊:Arthritis & Rheumatology
发表时间:25.12.20 online
影响因子:10.9
通讯作者/单位:Ulrich A. Walker @ epartment of Rheumatology, University Hospital Basel
一句话总结:研究发现
Graphical Abstract
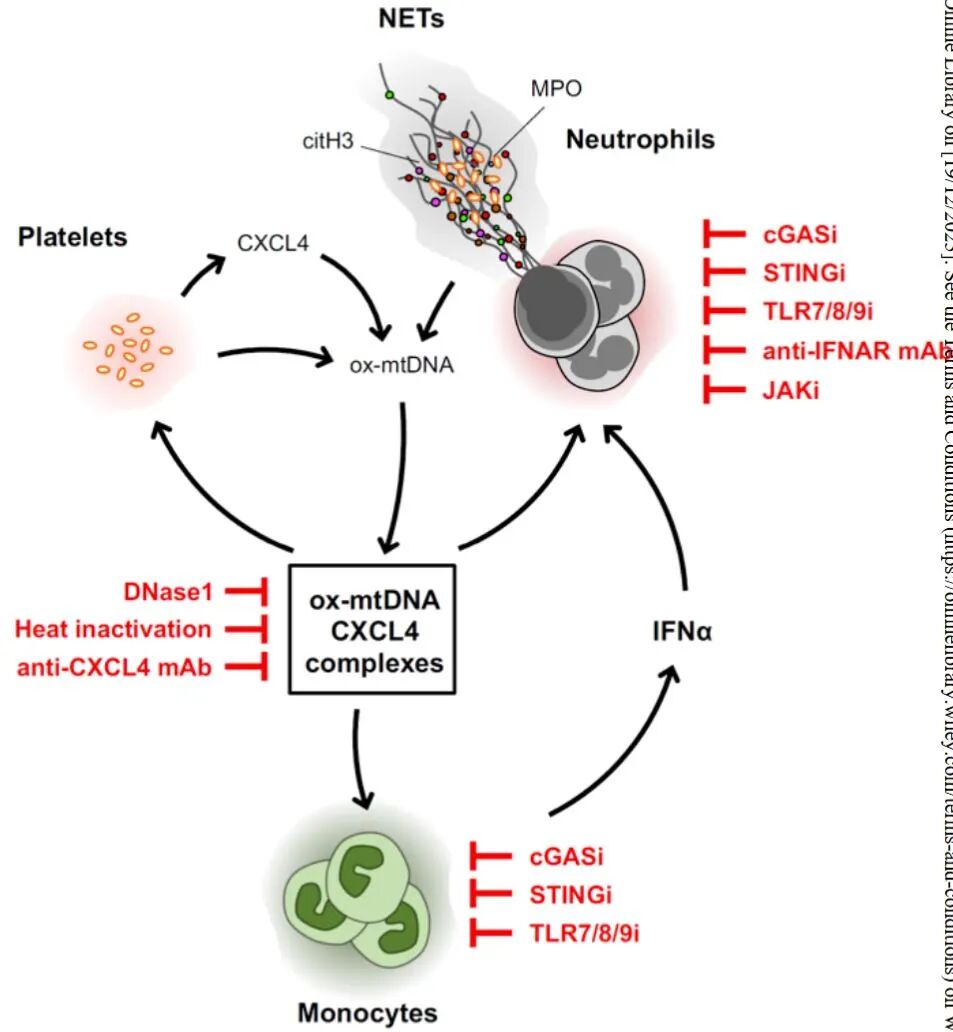
Abstract
目的:线粒体是一种含有低甲基化环状基因组的细胞器。已有研究表明,系统性循环中的线粒体DNA(mtDNA)与炎症反应相关。本研究旨在探讨系统性硬化症(SSc)中循环DNA的作用及其释放的细胞机制。
方法:从健康对照者和SSc患者的血浆中提取总DNA,通过qPCR分析mtDNA(ATP-6)和核DNA(GAPDH)的拷贝数。将中性粒细胞和血小板与SSc患者血浆及mtDNA共孵育,采用SytoxGreen染色和免疫染色评估中性粒细胞胞外诱捕网(NET)形成。检测血小板释放mtDNA的倾向。通过MitoSOX Red染色和8-OHdG ELISA评估DNA氧化情况。采用ELISA检测血浆中I型干扰素(IFN)和CXCL4水平。利用THP1报告细胞系评估IFN信号激活能力,并通过全血RNA转录组分析进行验证。
结果:SSc患者血浆中mtDNA水平中位数较健康对照者高152倍,而核DNA水平无显著差异。SSc来源的mtDNA高度氧化。SSc来源的mtDNA能有效诱导NET形成,尤其在SSc患者的中性粒细胞中作用最强,并能激活血小板释放mtDNA。SSc血小板释放的氧化mtDNA与CXCL4形成复合物,进一步刺激中性粒细胞和血小板释放mtDNA。血浆中mtDNA浓度与SSc患者血液中I型IFN浓度相关,SSc血液表现出干扰素刺激基因(ISG)表达升高。SSc血浆来源的mtDNA通过内体TLR、cGAS/STING和JAK/STAT通路诱导IFN信号和NET形成。I型IFN通路进一步促进NET形成和mtDNA释放,IFN受体(IFNAR)和JAK抑制剂可拮抗这一促NET效应。
结论:SSc血浆中以大量mtDNA为特征,该mtDNA通过正反馈机制促进其自身从中性粒细胞和血小板中释放。因此,mtDNA在SSc的炎症和组织损伤中发挥重要作用。
Background & Problem
背景:SSc以慢性自身免疫紊乱、广泛微血管损伤及纤维化为特征。虽然已知存在“干扰素签名”,但驱动这一现象的内源性DAMP分子来源尚不明确。mtDNA因其细菌样低甲基化结构,被视为强效的免疫激活剂。
研究空白:
1、SSc血浆mtDNA是否显著升高及其疾病表型的关联缺乏定量证据。
2、mtDNA释放的细胞来源及其与血小板/中性粒细胞的协同机制不明。
3、驱动I型IFN信号的具体胞内感受通路(如cGAS-STING)尚未完全确立。
Methodology
研究设计:病例-对照横断面实验研究,纳入33例SSc患者及33例健康对照。
实验设计:
定量与表征:qPCR检测mtDNA/nDNA拷贝数;ELISA与MitoSOX检测氧化程度(8-OHdG)。
功能实验:机械剪切模拟血小板释放;SytoxGreen实时监测NETs形成;THP1-Dual报告细胞评估IFN活性 。
干预策略:使用针对cGAS(PZ038)、STING(H151)、TLR、IFNAR(anifrolumab)及JAK(tofacitinib)的抑制剂。
组学验证:全血Bulk RNA-seq检测ISG。
逻辑:通过定量比较 SSc 与 HC 血浆 mtDNA 水平并实施体外刺激-抑制实验,建立“氧化 mtDNA-CXCL4 复合物 → TLR/cGAS-STING/IFNAR-JAK-STAT 轴 → Ⅰ 型 IFN 信号放大 → NETosis 与血小板进一步释放 mtDNA”的正反馈因果链。
Key Results & Interpretation
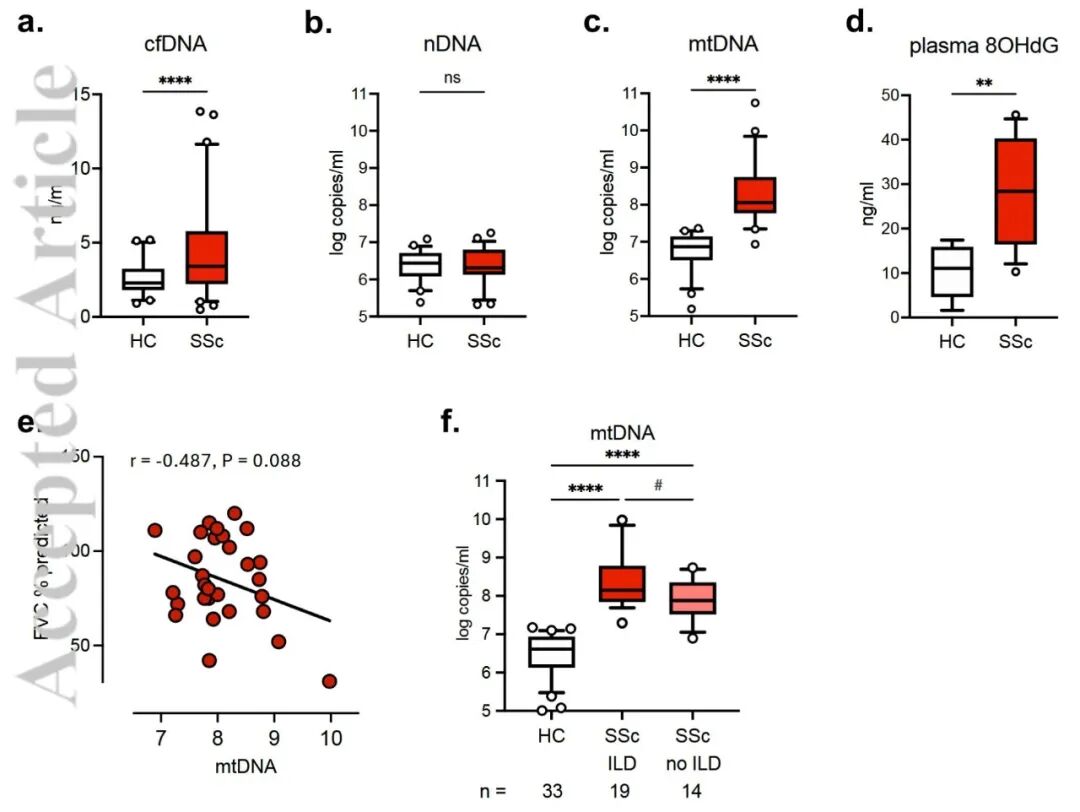
Figure1:SSc患者血浆mtDNA水平(1c)、氧化标志物8-OHdG(1d)及与肺功能的相关性(1e-f)
结果解读:SSc患者血浆mtDNA拷贝数中位数是健康对照的152倍,而nDNA无显著差异。
临床意义:mtDNA水平在ILD患者中更高,且与FVC(用力肺活量)预测值呈显著负相关,提示其参与
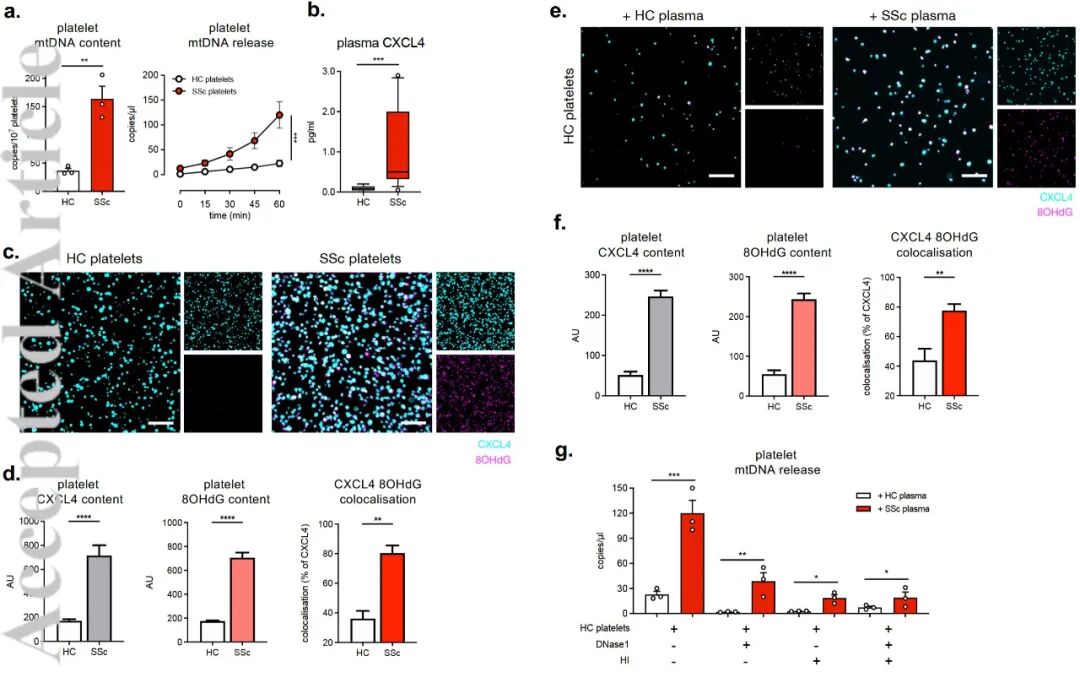
Figure2:血小板机械释放实验(2a)与CXCL4/8-OHdG免疫荧光共定位(2c-d)
结果解读:机械剪切诱导下,SSc血小板释放mtDNA显著高于HC。
机制发现:免疫共定位证明SSc血小板内存在CXCL4-ox-mtDNA复合物,两者协同释放进入循环。
发现点3:SSc血浆诱导中性粒细胞发生NETosis并释放mtDNA
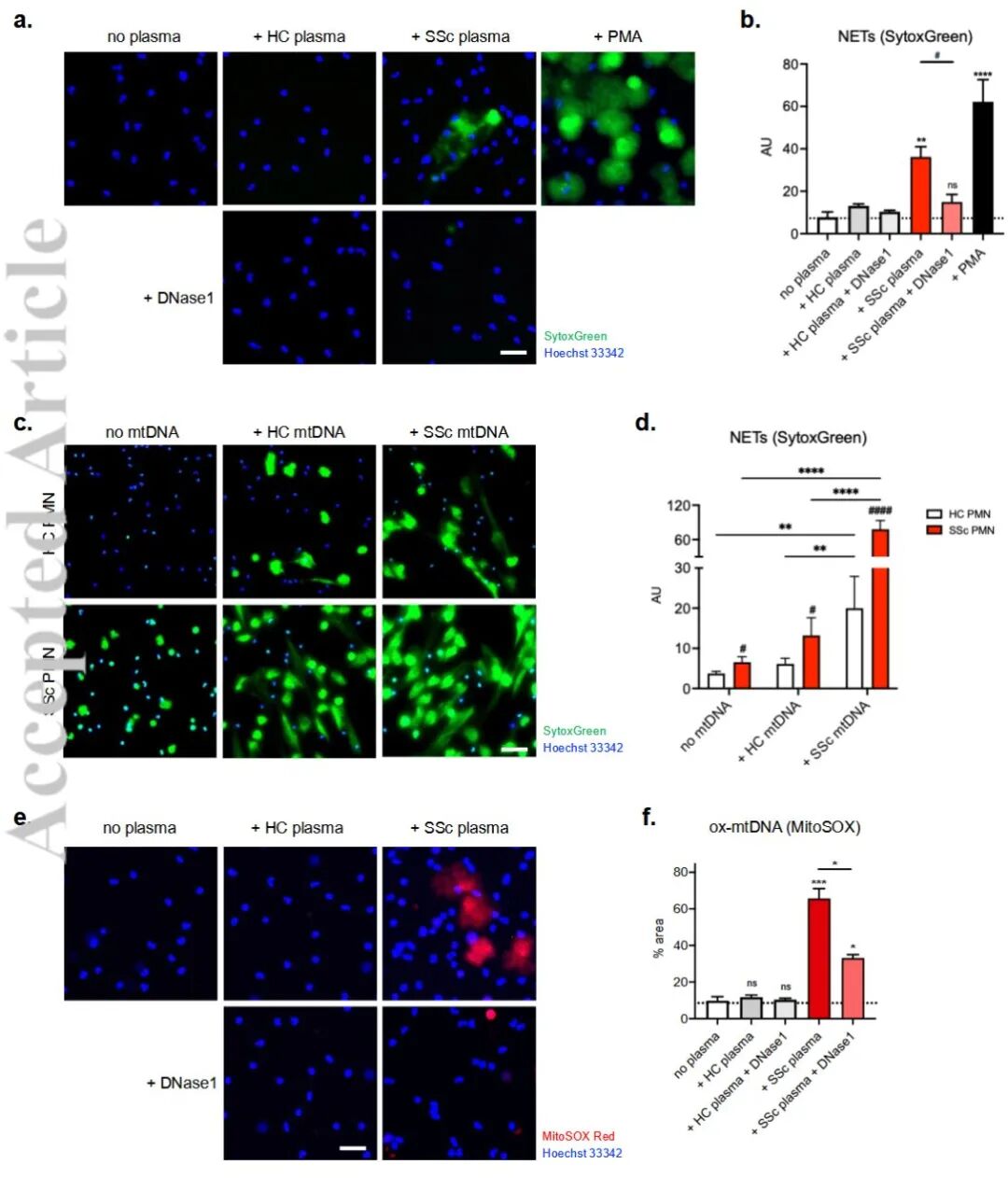
Figure3:SSc血浆诱导的NET形成(3a-b)及释放过程中的氧化型mtDNA(3e-f)
结果解读:SSc血浆可强效诱导健康中性粒细胞发生NETosis,且这一过程可被DNase1抑制,说明DNA成分是诱导关键。
关键点:实时成像证实中性粒细胞在形成NETs的同时排出了氧化的mtDNA。
发现点4:“血小板-中性粒细胞”协同放大效应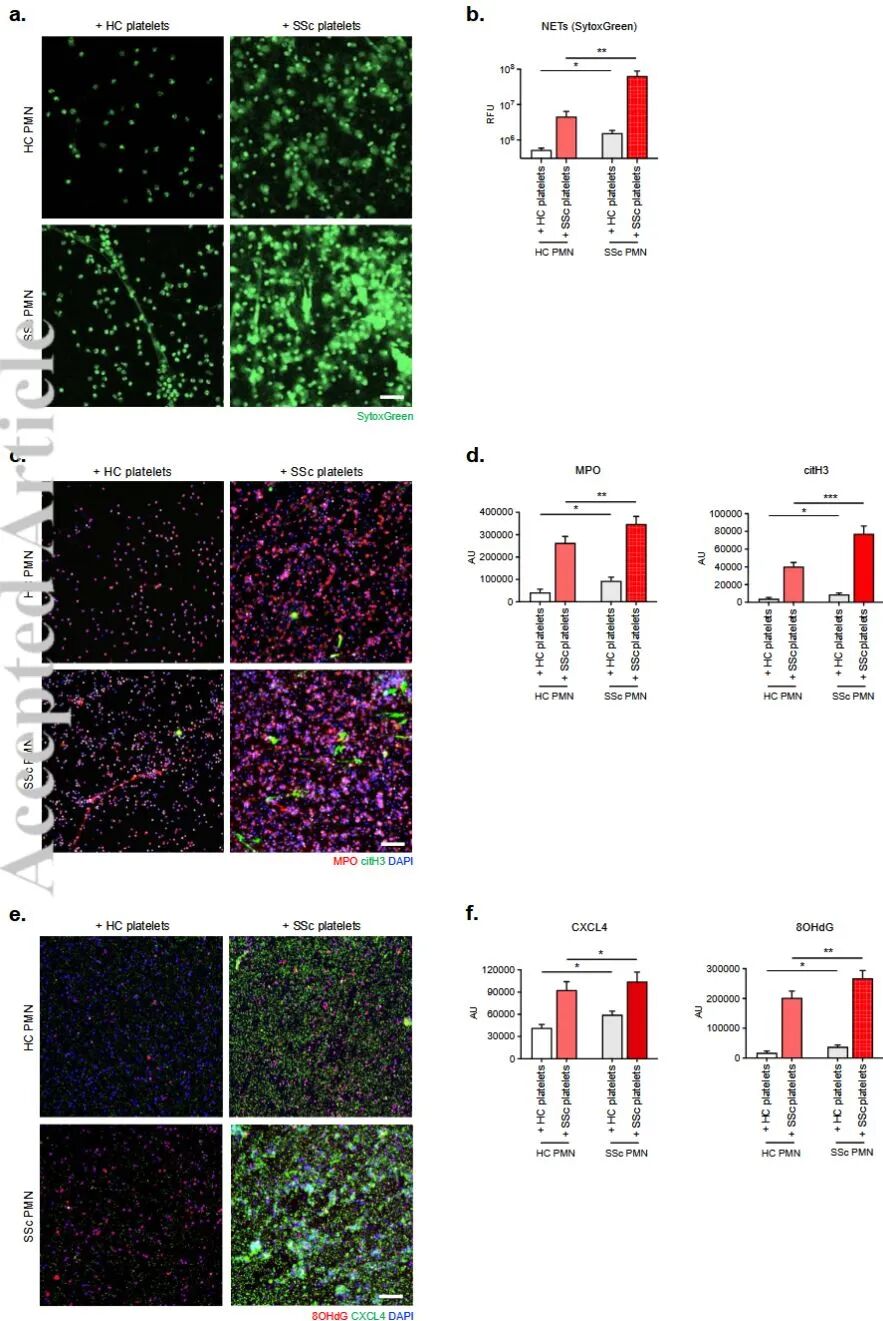
Figure4:细胞共培养实验展示SSc血小板诱导中性粒细胞产生含CXCL4的NETs(4e-f)
结果解读:SSc血小板与中性粒细胞共培养时,NETs形成量显著增加。
形态学证据:免疫荧光显示生成的NETs结构内嵌有CXCL4与氧化型mtDNA,形成了自我放大的闭环。
发现点5:信号通路解析:复合物如何激活干扰素通路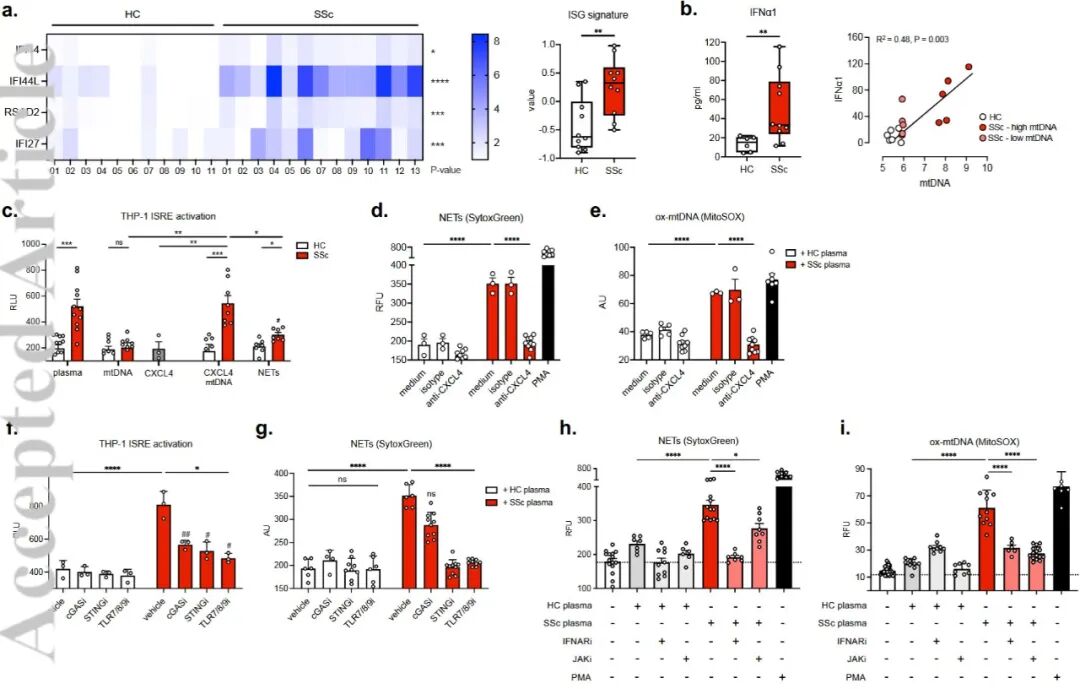
Figure5:THP1报告系统实验(5c)与多通路药理学阻断结果(5f-i)
核心发现:只有CXCL4-mtDNA复合物能激活IFN信号,单用任一成分均无效。
通路闭环:阻断cGAS-STING或TLR可抑制ISRE激活;阻断JAK通路不仅抑制IFN,还能反过来减少NETosis及mtDNA释放,证实了双重正反馈环路。
发现点6:转录组学与临床亚组验证
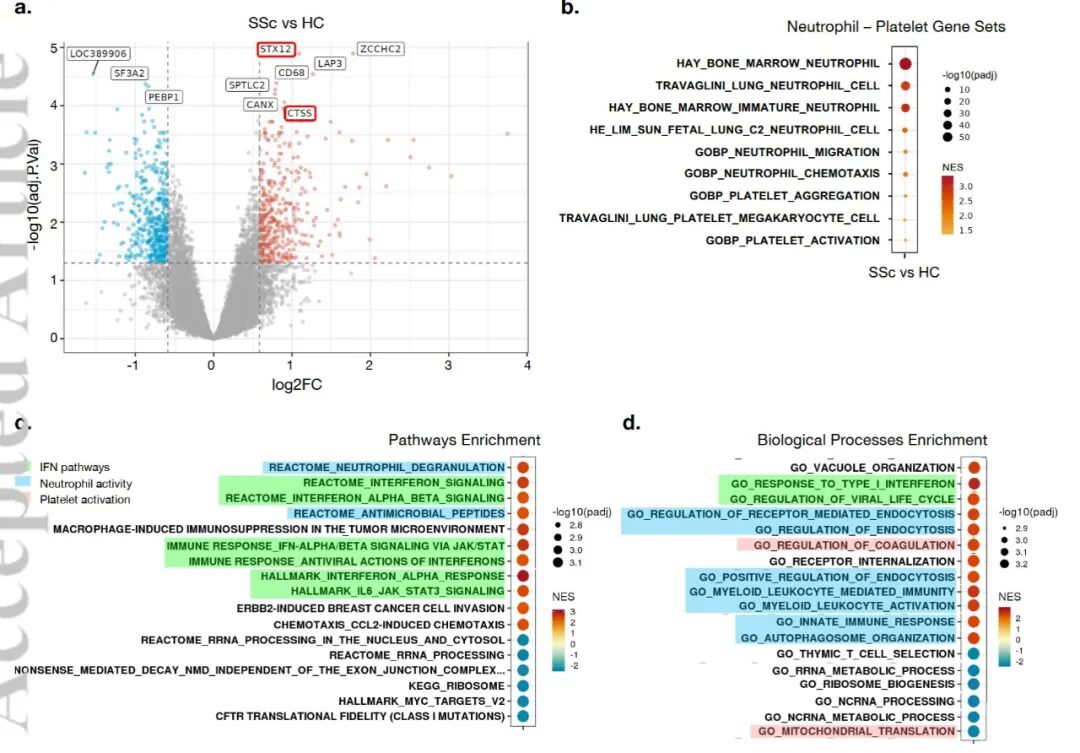
Figure6:全血转录组差异基因(6a)与ISG/血小板/中性粒细胞激活通路富集(6b-d)
结果解读:RNA-seq显示SSc患者外周血中ISG与中性粒/血小板激活基因同步高表达,与体外实验高度吻合
Innovation & Takeaway
✨ 创新点
1、首次揭示血小板-中性粒细胞协同释放ox-mtDNA是SSc炎症的核心驱动轴。
2、发现CXCL4-ox-mtDNA复合物作为新型DAMP激活干扰素信号。
3、确立了“DNA感受→IFN信号→促进释放”的闭合环路,解释了SSc炎症的持续性。
✨ 科研启示
该研究将mtDNA从单纯的“细胞损伤标志”提升到了“疾病驱动因子”的高度。对于其他伴有干扰素通路的疾病(如SLE、
✨ 临床/应用价值
诊断标志物:循环氧化mtDNA及CXCL4水平可辅助评估ILD风险及疾病活动度。
精准治疗:靶向mtDNA释放、促进降解(DNase I)或阻断感应通路(JAKi、anifrolumab、cGAS抑制剂)是极具前景的新策略。
临床课题+基础的思路借鉴
本研究问题可概括为:“SSc 中异常 mtDNA 从何而来、如何放大、是否驱动 I 型干扰素反应及组织损伤?”
第一步(图1)确认“有”——血浆 mtDNA 显著升高且氧化。
第二步(图2-3)明确“从哪来”——血小板与中性粒细胞各自释放,且 SSc 来源细胞更活跃。
第三步(图4)展示“如何放大”——血小板CXCL4-ox-mtDNA 复合物诱导 NET,NET 再释放更多 ox-mtDNA,形成正反馈。
第四步(图5)揭示“如何信号”——复合物经TLR/cGAS-STING 激活 I 型干扰素,干扰素经 JAK-STAT 再促进 NET,构成第二重正反馈。
第五步(图6+临床数据)验证“有何意义”——外周血基因表达与体外机制吻合,且 mtDNA 水平与肺纤维化指标关联,提示其可能参与疾病进展。
通过“现象→来源→交互→信号→临床”五级阶梯,作者把“mtDNA 升高”这一表象逐层拆解,最终完整论证了“血小板-中性粒细胞协同释放氧化 mtDNA-CXCL4 复合物,经I型干扰素通路激活炎症风暴并助推SSc炎症与ILD”的核心结论
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)