Metadata Card
文献题目:Lipid droplet-induced T cell death sustains autoimmune tissue inflammation
发表期刊:Cell Metabolism
发表时间:26.2.18 Online
影响因子:30.9(中科院1区)
通讯作者/单位: Cornelia M. Weyand @ 斯坦福大学/梅奥医学中心
一句话总结:类风湿关节炎中的CD4+ T细胞在脂质压力下,将脂滴转化为携带GSDMD及其活化因子的“杀手武器”,通过诱导T细胞焦亡并释放促炎DAMPs来持续驱动关节炎症。
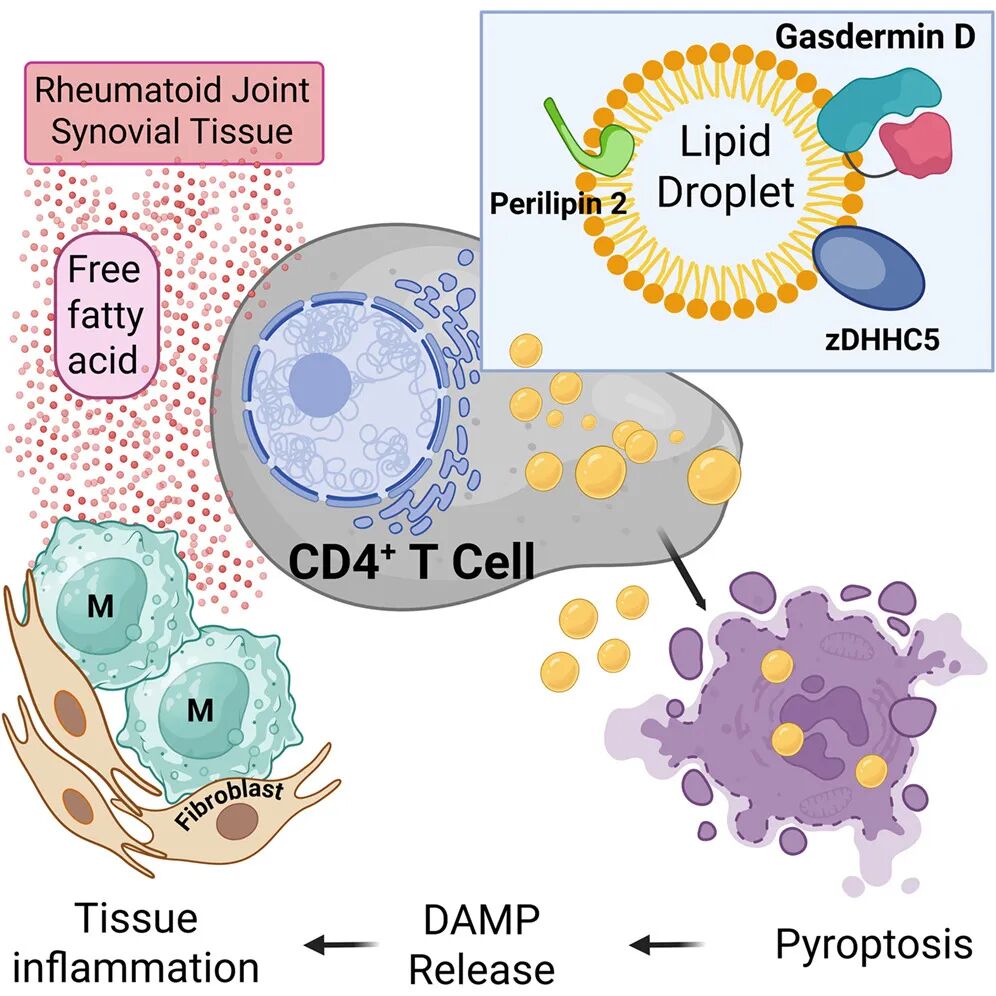
Graphical Abstract
Abstract
中文摘要:
导致
英文摘要:
Autoimmunity leading to rheumatoid arthritis (RA) involves CD4+T cell recruitment into synovial tissue. However, metabolic conditions supporting the survival and pro-inflammatory effector functions of these tissue-invading T cells remain poorly understood. Lipidomic analysis identified the inflamed synovium as a lipid-rich environment. In functional studies, administration of the free fatty acid oleic acid exacerbated synovitis. Tissue-invading CD4+T cells responded to fatty acid with rapid cell lysis, releasing cytoplasmic and nuclear content into the extracellular space. This T cell lytic death required sequestration of the pore-forming molecule gasdermin D and the acyltransferase zDHHC5 to lipid droplets, which translocated to the plasma membrane to trigger membrane rupture and pyroptotic cell death. Targeting lipid droplet formation in CD4+T cells through perilipin-2 knockdown or inhibiting gasdermin activation by blocking protein acylation proved highly effective in suppressing synovitis. Thus, autoimmune CD4+T cells lack metabolic resilience, are primed to undergo pyroptosis in lipid-rich environments, and deliver pro-inflammatory cargo to surrounding tissue.
Background & Problem
背景:传统的自身免疫研究多聚焦于自抗原识别。然而,近期研究发现代谢重构在维持炎症反应中至关重要。RA患者的CD4+ T细胞存在线粒体DNA修复缺陷,导致其进入一种“伪饥饿”状态,被迫在
痛点:尽管已知RA T细胞存在代谢功能障碍,但它们如何在恶劣的组织微环境中生存并发挥促炎作用仍不明确。特别是滑膜组织中极高浓度的游离脂肪酸 (FFA) 如何影响T细胞的命运及其与慢性炎症的关系,一直是该领域的空白点。
Methodology
策略:本研究采用了“人体组织-小鼠”嵌合模型(NSG小鼠植入人类滑膜并重建人类免疫系统)。
技术:
1. 脂质组学与蛋白质组学:分析滑膜组织液及T细胞内脂滴的成分。
2. 活细胞成像与电镜:实时追踪脂滴易位至质膜并触发细胞裂解的过程。
3. 基因干预:利用siRNA或质粒过表达靶向PLIN2和zDHHC5,验证脂滴和酰化在炎症中的作用。
4. 临床样本关联:结合RA患者临床疾病活动度指数 (CDAI) 进行相关性分析。
Key Results & Interpretation
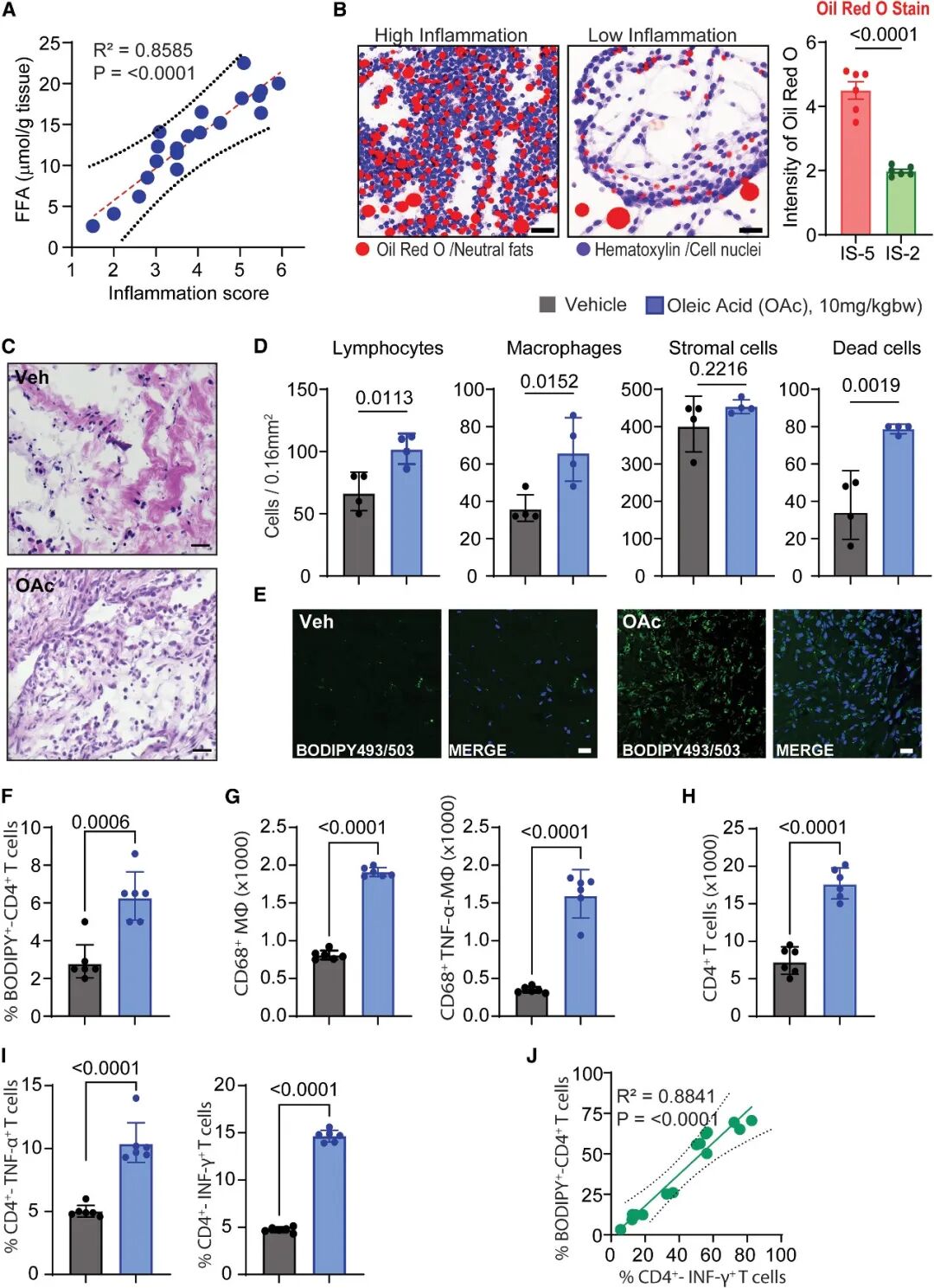
[1A-B]:通过对新鲜滑膜活检样本的定量分析发现,组织内游离脂肪酸 (FFA) 浓度比血浆高约100倍。FFA 浓度以及油红 O 染色强度均与组织炎症评分 (IS) 呈显著正相关 (P<0.0001) 。
[1C-D]:在人源化 NSG 小鼠模型中,注射外源性油酸 (OAc) 显著加剧了滑膜炎症,导致滑膜组织中淋巴细胞、巨噬细胞以及死细胞的数量大幅增加。
[1E-F]:BODIPY 染色结果显示,OAc 处理诱导了组织浸润的 CD4+ T 细胞内脂滴 (LD) 的大量积累。
[1G-I]:流量细胞术分析证实,OAc 暴露不仅增加了促炎性 CD68+ 巨噬细胞的比例,还显著提升了 CD4+ T 细胞产生 TNF-α 和 IFN-γ 的能力。
[1J]:相关性分析揭示,CD4+ T 细胞内脂滴形成频率与其 IFN-γ 的分泌水平以及细胞死亡率高度同步。
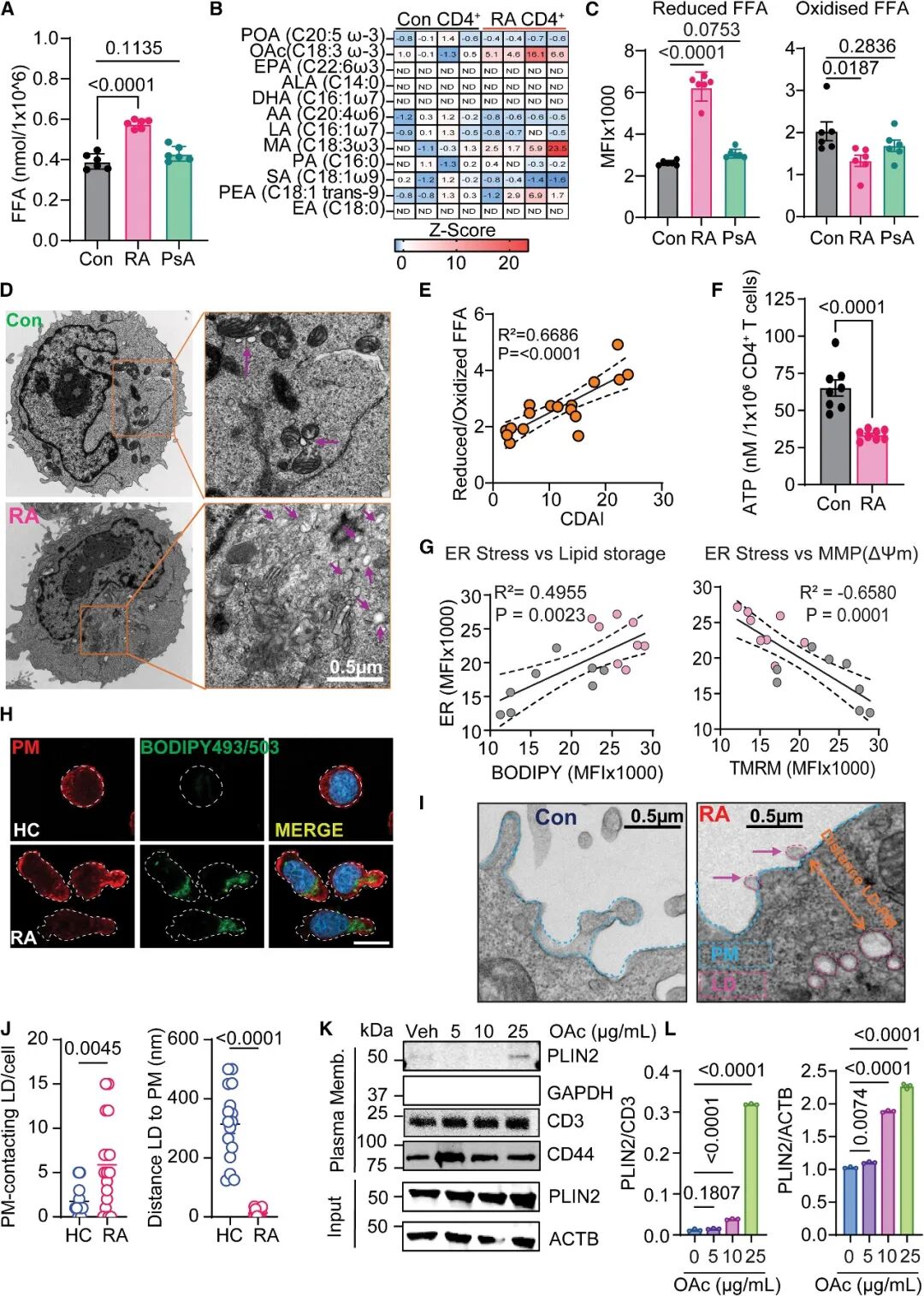
[2A-B]:脂质组学分析显示,RA 患者 CD4+ T细胞内的 FFA 含量比对照组高出约 40%,且分离出的脂滴中特别富集了油酸 (OAc) 和肉豆蔻酸。
[2C-E]:RA T细胞主要积累还原型而非氧化型 FFA。这种还原型/氧化型 FFA 的比例与患者的临床疾病活动度评分 (CDAI) 呈强正相关。
[2F-G]:由于线粒体适能下降(ATP 产量降低),RA T细胞表现出明显的内质网 (ER) 压力和 ER 膜扩张,这为脂滴的大量生成提供了结构基础。
[2H-J]:电镜与超分辨成像显示,在 RA T 细胞中,脂滴不再均匀分布,而是高度集中在细胞尾足部 (uropod) 。脂滴与质膜 (PM) 的距离从健康细胞的 300-400 nm骤减至 20 nm以内,形成了直接的物理接触。
[2K-L]:质膜成分分离实验证实,脂质压力下 LD 结构蛋白 PLIN2 会直接整合进 T 细胞的质膜中。
发现点3:脂质压力诱发 T 细胞焦亡及其促炎货物的释放
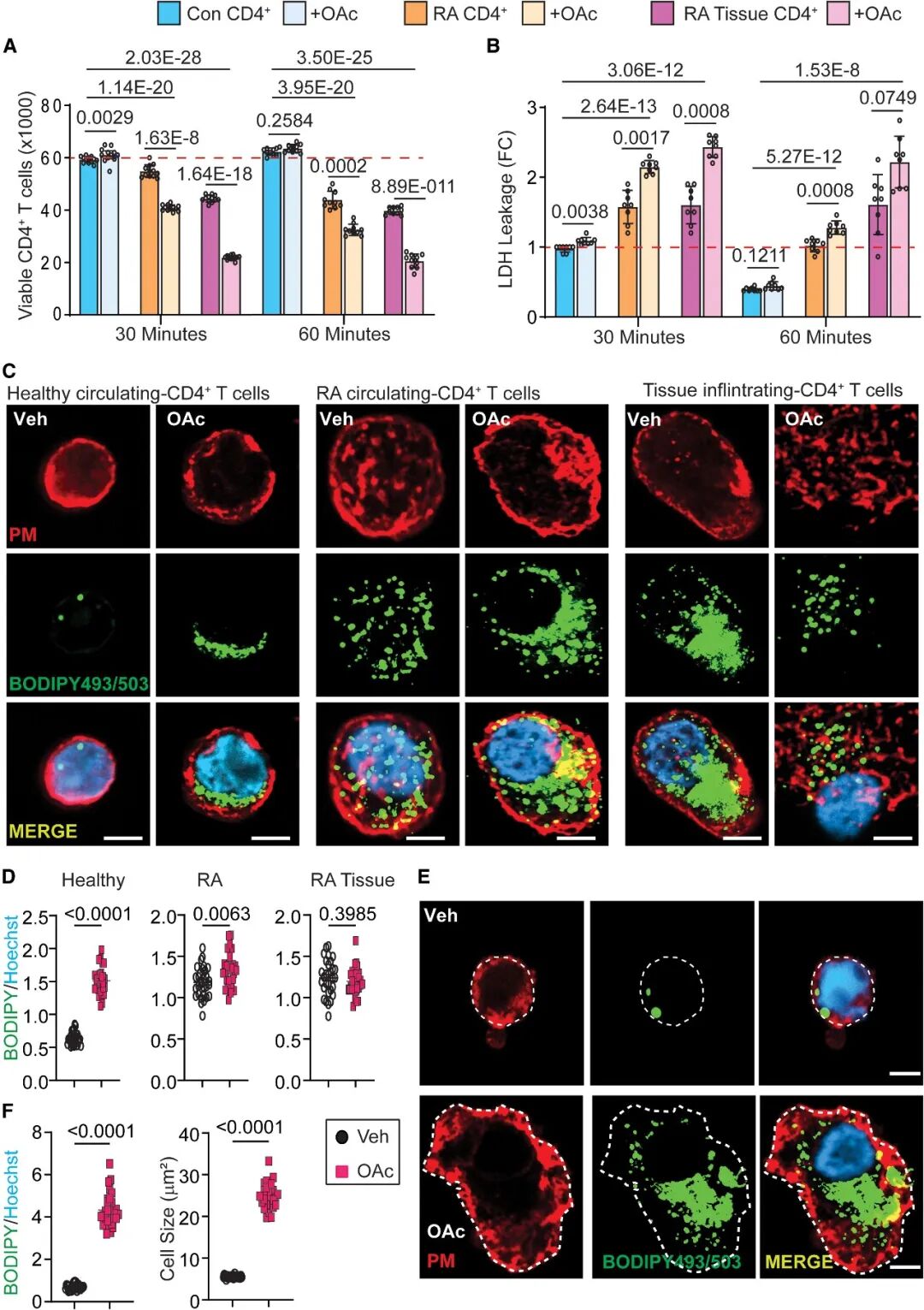
[Fig 3A-C]:生存分析显示,来自 RA 组织和外周血的 CD4+ T细胞在油酸挑战下表现出极高的易感性,在 60 分钟内即出现大规模死亡。
[Fig 3E-F]:活细胞成像捕捉到 T 细胞在脂质诱导下发生细胞肿胀、脂滴弹射以及质膜彻底碎裂的过程。
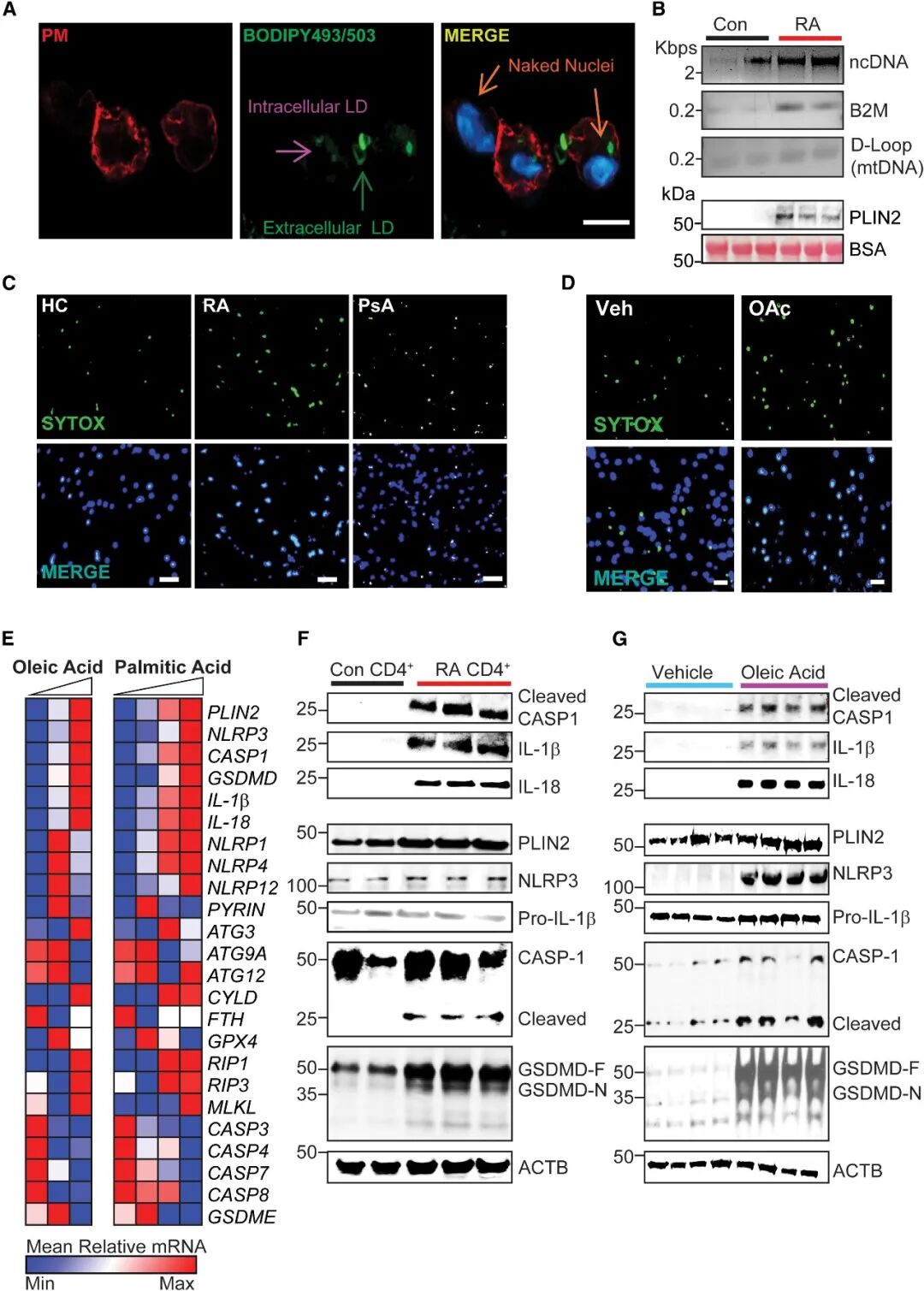
[Fig 5A-D]:受损细胞表现出典型的焦亡特征,包括 SYTOX 绿色荧光染料的快速摄取(代表膜通透)以及“裸核”的形成。
[Fig 5B & G]:上清液检测证实,受损 T细胞释放了大量的核 DNA (ncDNA)、线粒体 DNA (mtDNA) 以及 PLIN2 蛋白。同时,免疫印迹检测到剪切后的活性 CASP1、IL-1β和 GSDMD-N 端片段。
[Fig 5E]:转录本分析显示,油酸处理激活了 NLRP3、GSDMD 以及促炎细胞因子(IL-1β、IL-18)的基因特征谱。
发现点4:脂滴通过隔离 GSDMD 和 zDHHC5 构建“膜孔触发器”
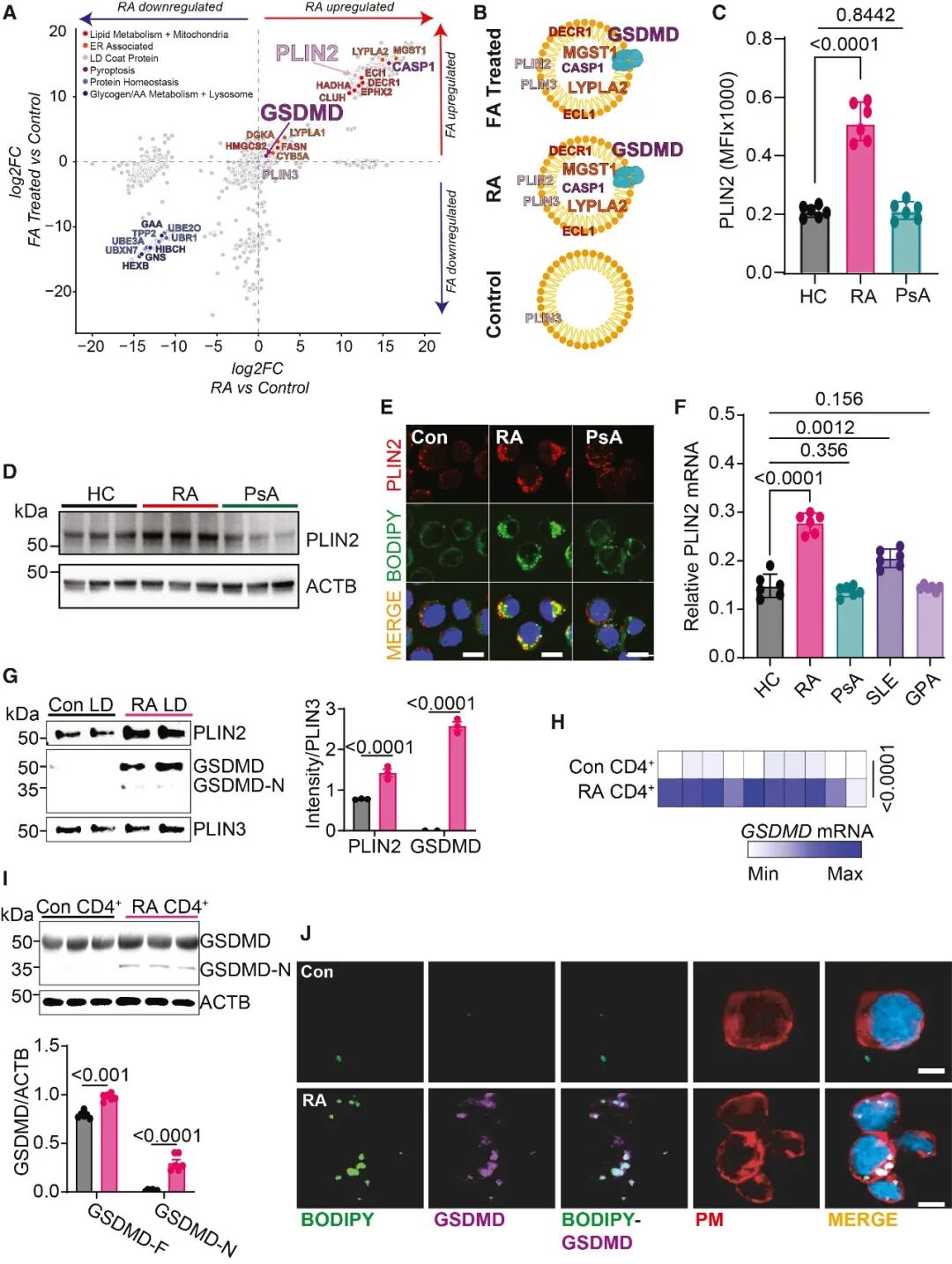
[Fig 4A-B]:脂滴蛋白质组学 scatterplot 揭示,RA 状态和脂质处理共同导致脂滴表面 GSDMD、CASP1 及相关代谢酶(如 LYPLA2)的显著富集。
[Fig 4G-J]:免疫印迹和共聚焦实验确认,GSDMD 蛋白特异性地隔离在 RA T 细胞的脂滴中 ,并与 PLIN2 存在显著的共定位。
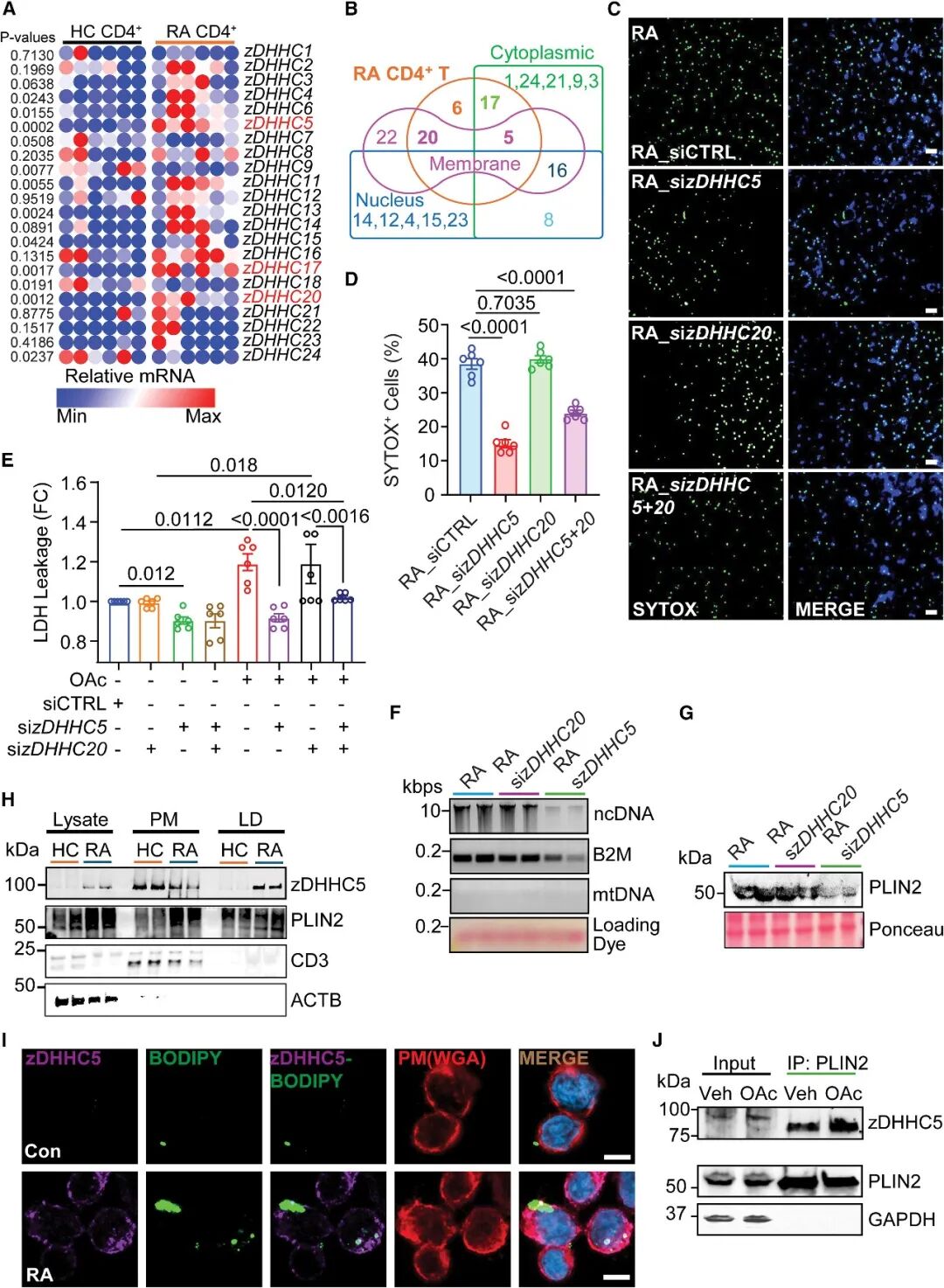
[Fig 6A-B]:酰基转移酶筛选发现 zDHHC5 在 RA T 细胞中异常高表达 ,且其亚细胞定位与质膜和脂滴高度重合。
[Fig 6H-J]:生化实验证实 zDHHC5 能够与 PLIN2 结合并整合至脂滴表面。
[Fig 6C-G]:通过 siRNA 敲低 zDHHC5,能够显著抑制脂质诱导的 SYTOX 摄取、LDH 泄漏以及胞外 DNA 的释放,证明了 zDHHC5 在介导膜孔形成中的关键作用。
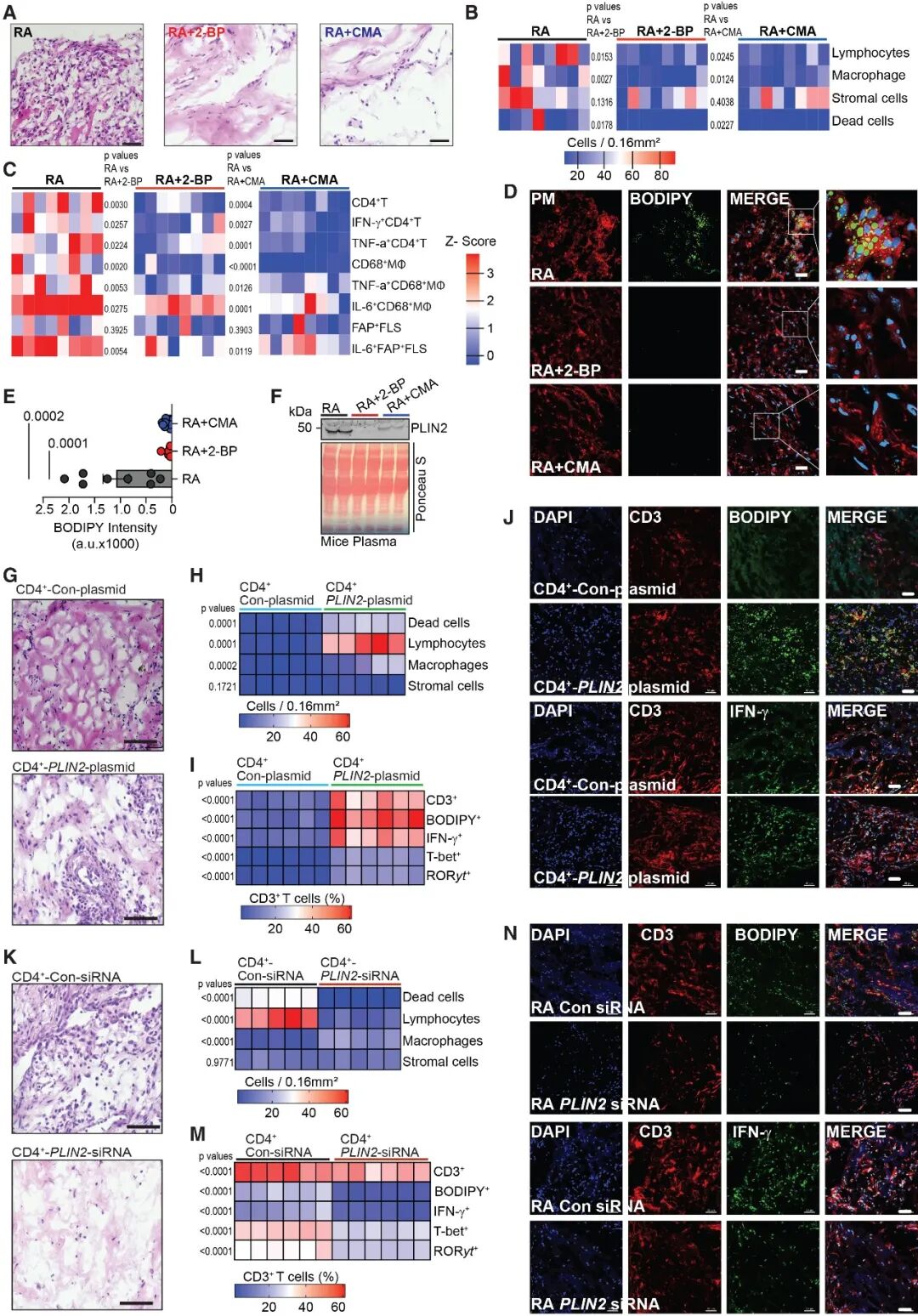
[7A-C]:在人类滑膜移植模型中,使用广谱 S-酰化抑制剂 2-BP 或 CMA 处理,可显著减少滑膜组织的细胞浸润,并大幅降低产生 IFN-γ 和 TNF 的致病性T细胞频率。
[7D-F]:抑制酰化能够减少组织内的脂滴沉积,并降低小鼠血浆中循环的 PLIN2 水平。
[7G-J]:人为在健康 CD4+ T细胞中过表达 PLIN2 (PLIN2-OE),足以使其在进入滑膜后产生大量的死细胞、积累脂滴并分化为 IFN−γ+ 和 T−bet+ 的致病表型。
[7K-N]:反之,在 RA T细胞中敲低 PLIN2 (PLIN2-siRNA) 则能够显著减轻滑膜炎,减少浸润的炎性细胞数量并恢复组织耐受性。
Innovation & Takeaway
✨ 创新点
1. 首次发现脂滴在T细胞中不仅是能量仓库,更是诱导焦亡的“杀手细胞器” 。
2. 鉴定了zDHHC5驱动的GSDMD酰化是脂质诱导细胞死亡的核心环节。
3. 解释了为何在缺乏抗原刺激时,RA炎症仍能通过DAMP释放自我维持。
✨ 科研启示
本研究将“代谢异常”与“细胞死亡方式”联系起来,提示我们在研究慢性炎症时,不仅要看细胞在产生什么,还要看细胞是怎么“死的”。脂滴-质膜的近距离相互作用可能是调控细胞命运的物理新维度。
✨ 临床/应用价值
1. 生物标志物:循环T细胞中PLIN2、zDHHC5的高表达可作为RA病情评估或常规治疗不敏感的新指标。
2. 治疗新方向:通过恢复T细胞的线粒体适能或直接阻断脂滴介导的焦亡,可能为难治性RA提供除细胞因子拮抗剂之外的新选择。
局限性
1. 上调机制不明:导致PLIN2、GSDMD和zDHHC5在进入组织前就初步上调的最初触发因素尚待研究。
2. 广谱抑制剂局限:研究使用的2-BP和CMA是广谱酰化抑制剂,未来需开发针对zDHHC5的特异性小分子。
3. 模型局限:虽然人源化小鼠模型模拟了关键特征,但仍无法完全替代人体复杂的免疫环境。
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)