2026年3月22日~25日,第52届欧洲血液和骨髓移植学会(EBMT)年会于西班牙马德里顺利召开。此次大会,浙江大学医学院附属第一医院
大会主旨报告:P04-5
Armored and in vivo Next-Gen CARs
下一代装甲型与体内CARs
报告人:黄河
本研究围绕CAR-T细胞疗法的前沿研发与临床应用展开深度分享,重点阐释了该领域两大核心发展方向:CAR-T细胞的基因工程改造与体内递送系统优化。在CAR-T细胞基因工程改造板块,黄河教授系统梳理了各类细胞因子武装型CAR-T细胞的设计思路与临床优势,包括低剂量给药、简化治疗流程、优异的体内扩增与存续能力等。针对双特异性T细胞衔接子分泌型CAR-T细胞,他指出这类CAR-T细胞可协同NK细胞发挥协同抗肿瘤效应,在临床前动物模型中展现出卓越的抗白血病及实体瘤活性,为多细胞联合免疫治疗提供了全新策略。在递送系统革新方面,报告重点对比了病毒载体递送与脂质纳米颗粒递送两大技术路径。基于最新临床数据,体内CAR-T细胞疗法已在复发难治性
特邀报告:IS01-4
Chemo-free therapy for Ph+ ALL
Ph+ ALL的去化疗治疗模式
报告人:黄河
本报告系统介绍了Ph+ ALL无化疗治疗策略的发展现状,并重点分享了团队在靶向治疗与CAR-T细胞治疗领域的研究进展。报告首先回顾了Ph+ ALL治疗模式的演变。随着酪氨酸激酶抑制剂(TKI)和免疫治疗的发展,Ph+ ALL正逐渐从传统化疗模式迈向“chemo-free”治疗时代。目前,多项临床研究正在探索TKI联合免疫治疗的新策略。黄河教授重点介绍了团队开展的临床研究——Dasatinib联合CAR-T细胞治疗新诊断Ph+ ALL的临床试验。研究结果显示,在中位随访23.9个月时,大部分患者维持完全缓解并获得持续分子学缓解,2年总体生存率和无白血病生存率均达到92%,且治疗相关毒性可控。该研究提示,TKI联合CAR-T细胞治疗有望成为新诊断Ph+ ALL的一种潜在无化疗治疗新模式。黄河教授最后指出,随着靶向治疗与细胞免疫治疗技术的不断发展,通过优化TKI与CAR-T细胞治疗的联合策略,Ph+ ALL治疗正逐步迈向更加精准化和个体化的新时代。
SS02-1
From page to podium: mastering publication and presentation in Hematology
论文发表与学术汇报进阶:精进血液学研究成果的发表与展示能力
报告人:黄河、Mohamad Mohty

图1 黄河教授作报告
摘要号:OS04-03
ORAL IPTACOPAN DEMONSTRATES EFFICACY AS SALVAGE THERAPY FOR HIGH-RISK TRANSPLANT-ASSOCIATED THROMBOTIC MICROANGIOPATHY: FIRST REAL-WORLD EXPERIENCE
首个真实世界应用经验:口服
报告人:高斐

图2 高斐医生作报告
研究结果:在这项回顾性研究中,2024年7月至2025年5月期间,来自中国7家机构的共27例TA-TMA患者接受了伊普可泮治疗。TA-TMA的诊断时间为
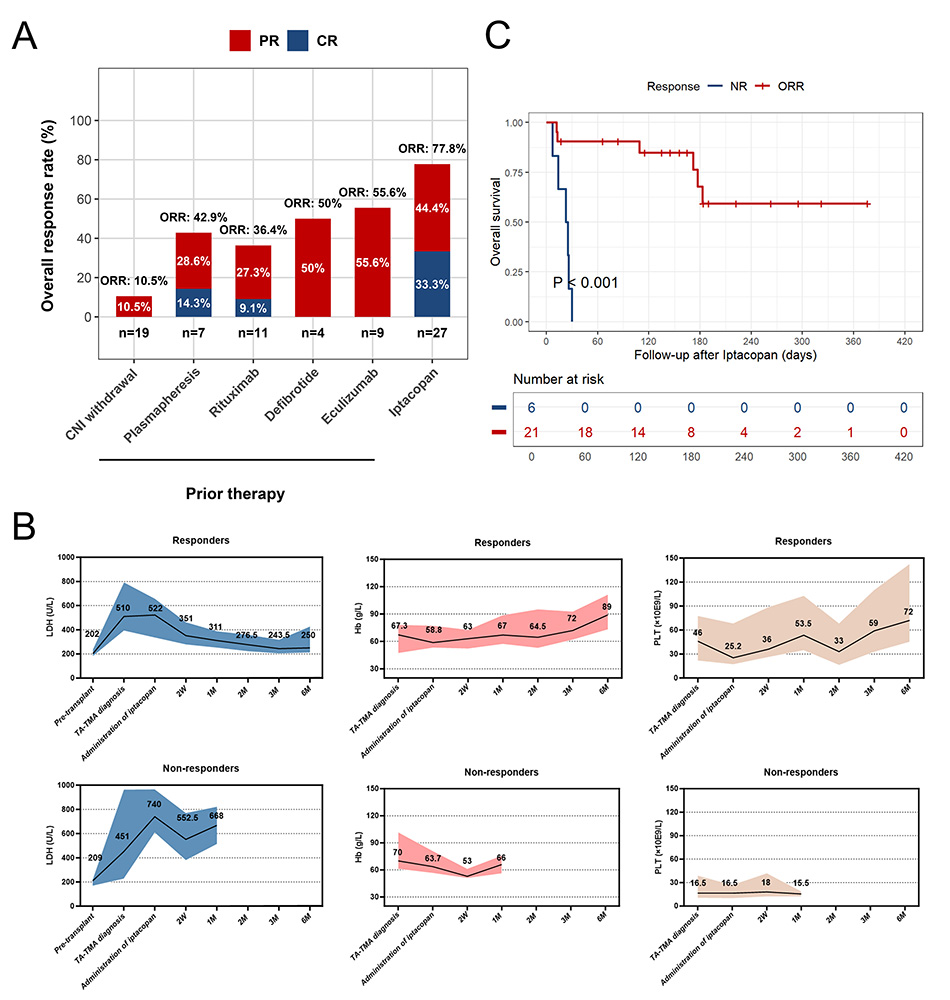
图3 (A)不同治疗手段后ORR;(B)不同治疗手段后LDH、Hb、PLT变化情况;(C)伊普可泮治疗后6个月时OS率
研究结论:口服补体抑制剂伊普可泮作为高危TA-TMA的挽救治疗显示出确切的临床疗效,且不受既往是否接受末端补体抑制剂治疗的影响。
摘要号:OS14-05
BETTER OUTCOMES WITH HAPLOIDENTICAL THAN MATCHED SIBLING DONORS FOR AML PATIENTS TRANSPLANTED IN MRD+ CR: A STUDY FROM GLOBAL COMMITTEE AND ALWP OF THE EBMT
一项来自EBMT全球委员会与ALWP的研究:对于以完全缓解伴MRD+状态接受移植的AML患者,单倍体相合供者(Haplo)较同胞全相合供者(MSD)可获得更优结局
报告人:

图4 叶逸山教授作报告
研究结果:研究共分析3385例移植患者,包括609例(18%)Haplo、1057例(31%)MSD和1719例(51%)10/10人类白细胞抗原(HLA)全相合无关供者(MUD)。全队列患者中位年龄为55岁(范围18-83岁)。Haplo组中第二次完全缓解(CR2)期移植患者比例(22%)高于MSD组(15%)和MUD组(18%)(p<0.001)。外周血是主要移植物来源(91%),约一半(49%)患者采用减低强度预处理。在三组中,原发病复发均是最主要的死亡原因。
多变量分析显示,以Haplo-HSCT为参照组,MSD-HSCT与显著更高的疾病复发风险相关(HR=1.55,95%置信区间[CI] 1.26-1.91;p<0.001),同时非复发死亡(NRM)率更低(HR=0.63,95% CI 0.46-0.86;p=0.004),最终导致其无白血病生存期(LFS)更差(HR=1.19,95% CI 1.01-1.41;p=0.048),GVHD/无复发生存率(GRFS)也更低(HR=1.22,95% CI 1.05-1.41;p=0.01)。值得注意的是,与Haplo-HSCT相比,尽管MUD-HSCT的疾病复发率更高(HR=1.26,95% CI 1.03-1.54;p=0.03),但在LFS、GRFS和OS方面无显著差异。
此外,如预期所示,与第一次完全缓解(CR1)期移植相比,CR2期移植与显著更高的复发发生率相关(HR=1.5,95% CI 1.27-1.78;p<0.001),因此其OS、LFS和GRFS均显著更差。与减低强度预处理相比,清髓性预处理方案与显著更低的复发率相关(HR=0.75,95% CI 0.64-0.87;p<0.001),并且OS、LFS和GRFS均显著更优。最后,年龄较大的患者(按10年间隔)与较高的NRM(HR=1.23, 95% CI 1.12-1.36; p<0.001)和较差的OS(HR=1.10, 95% CI 1.04-1.17; p<0.001)相关。
研究结论:对于在完全缓解伴MRD+状态下接受移植的AML患者,Haplo-HSCT较MSD-HSCT可获得更好的LFS和GRFS,主要归因于其更优的复发预防效果。
摘要号:OS17-02
TP53 VARIANT ALLELE FREQUENCY AS A GENETIC MRD MARKER PREDICTS RELAPSE AND GUIDES SUBTYPE-SPECIFIC THERAPY IN TP53-MUTATED AML/MDS UNDERGOING ALLOGENEIC STEM CELL TRANSPLANTATION
TP53变异等位基因频率(VAF)作为遗传学MRD标志物,可预测接受异基因造血干细胞移植(allo-HSCT)的TP53突变型AML/骨髓增生异常肿瘤(MDS)患者的复发,并指导亚型特异性治疗
报告人:

图5 赵妍敏教授作报告
研究结果:如图6所示,根据移植前遗传学MRD分为三组(VAF≤0.01%、0.01-0.1%和>0.1%)后发现,与其余两组相比,VAF>0.1%的患者结局明显更差(2年OS率:55.4% vs. 76.7% vs. 75.0%,p=0.240;2年无事件生存[EFS]率:40.3% vs. 69.7% vs. 75.0%,p=0.028;2年累积复发[CIR]率:52.0% vs. 13.3% vs. 0%,p=0.001)。在校正变量后,移植前TP53 VAF>0.1%仍是较差结局的独立预测因素(EFS:校正风险比[aHR] 3.3,95%CI 1.5-7.2;CIR:aHR 8.2,95%CI 2.6-26.2;OS:aHR 2.5,95%CI 1.0-6.1)。移植后VAF>0.01%同样可独立预测较差的OS(aHR 2.7,95%CI 1.2-6.0)、EFS(aHR 2.7,95%CI 1.4-5.0)和CIR(aHR 4.1,95%CI 2.1-8.2)。围移植期MRD动态监测显示出更优的预后区分能力。将遗传学MRD与多参数流式细胞术(MFC)联合,可提高移植前风险分层效能,其中双阳性患者生存最差(EFS:aHR 7.0,95%CI 2.6-18.9;CIR:aHR 30.3,95%CI 4.5-205.0;OS:aHR 4.5,95%CI 1.5-13.6)。
移植前TP53突变克隆清除可改善AML和MDS/AML患者的生存(2年OS率:77.2% vs. 47.2%,p=0.025;2年CIR率:12.8% vs. 62.3%,p<0.001),但在MDS患者中无显著影响。关于预处理方案,无论MRD状态如何,清髓性预处理与减低强度预处理之间的生存差异均无统计学意义。对于移植前VAF>0.1%的患者,
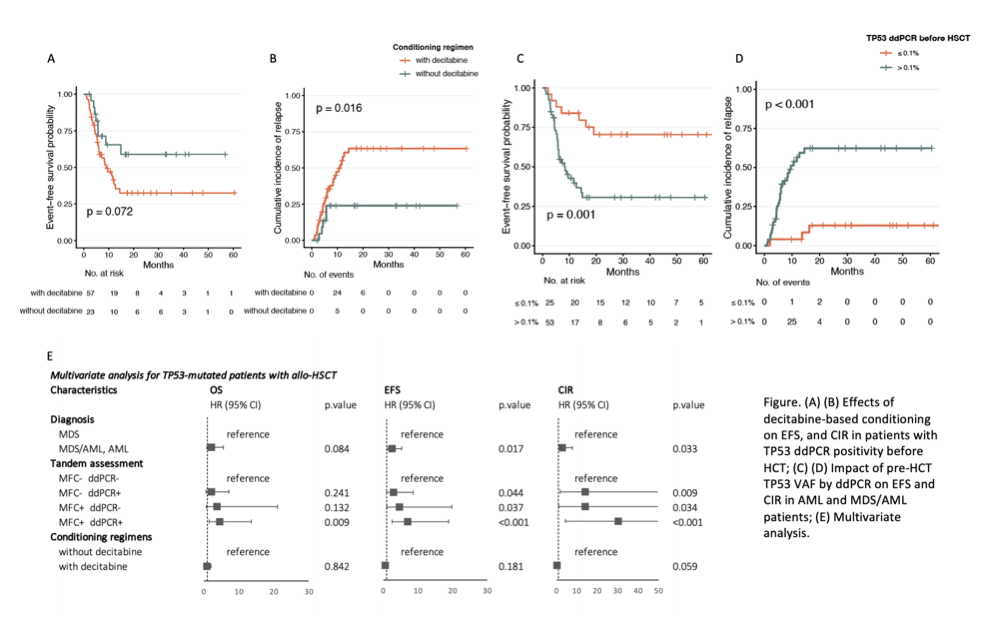
图6 (A)(B)地西他滨对移植前TP53 ddPCR阳性患者EFS和CIR的影响;(C)(D)通过ddPCR检测移植前TP53 VAF对AML和MDS/AML患者EFS和CIR的影响;(E)多变量分析
研究结论:移植前遗传学MRD监测可有效优化TP53突变型AML/MDS的风险分层。对于AML和MDS/AML患者,移植前强化治疗以实现MRD清除可带来生存获益;而对于MDS患者,无论是否达到深度MRD清除,尽早进行allo-HSCT可能已足够。对于移植前MRD水平较高的患者,地西他滨联合预处理可降低复发风险,突显了基于MRD指导预处理方案选择的价值。对于这一高危人群,移植后清除TP53突变克隆对于改善生存至关重要。
摘要号:OS17-04
PROGNOSTIC VALUE OF PERI-TRANSPLANT MOLECULAR MRD MONITORING BY TARGETED NGS FOR ALLO-HCT RECIPIENTS WITH FLT3-ITD MUTATED ACUTE MYELOID LEUKEMIA: A MULTICENTER STUDY OF TROPHY GROUP
围移植期采用靶向二代测序(NGS)进行分子学MRD监测对接受allo-HSCT的FLT3-ITD突变AML患者的预后价值:TROPHY研究组多中心研究
报告人:赵叶千

图7 赵叶千博士研究生作报告
研究结果:基于二代测序技术的聚合酶链反应(PCR-NGS)检测,移植前MRD+(>0.001%)患者较MRD-患者结局显著更差,具体表现为2年无复发生存(RFS)率更低(56.8% vs. 86.5%)、CIR率更高(30.0% vs. 6.9%)以及OS率更低(65.9% vs. 88.4%),差异均具有统计学意义(所有p<0.001)。值得注意的是,低水平FLT3-ITD(0.001%–0.1%)分子学MRD(M)即便低于毛细管电泳(CE)的检测阈值,仍提示移植后复发风险显著升高(CE-/M- vs. CE-/M+:8% vs. 25%,p<0.001)。
进一步分析显示,纳入移植前及移植后MRD状态的围移植期动态评估,较单一时间点的静态检测具有更优的风险分层能力(RFS的C指数:0.76 vs. 0.66 vs. 0.67;OS的C指数:0.73 vs. 0.64 vs. 0.67)。鉴于FLT3-ITD克隆具有动态演变特征,本研究进一步采用PCR-NGS与MFC联合进行串联MRD评估。结果显示,MFC-MRD阴性而分子学MRD阳性(F-/M+)组患者预后最佳,其2年CIR率、RFS率和OS率分别为6.4%、92.9%和92.9%;而MFC与分子学MRD双阳性(F+/M+)组患者预后最差,相应指标分别为45.0%、34.3%和43.1%,差异均具有统计学意义(所有p<0.001)。
在流式MRD-患者中,分子学MRD可进一步实现风险分层:在F-/M-组与F-/M+组中,CIR率分别为6.4%和23.0%(p=0.024),RFS率分别为88.3%和66.0%(p=0.003),OS率分别为89.8%和73.6%(p=0.024);而在分子学MRD-患者中,流式MRD并未显示出显著的预后区分作用。联合评估可提高阴性预测值(PPV 0.48;NPV 0.89),在假阳性略有增加的情况下,增强了对复发风险的排除能力。
在移植前分子学MRD+患者中,清髓性预处理较减低强度预处理可显著改善结局,2年RFS率分别为61.3%和20.0%(p=0.002),OS率分别为72.1%和40.0%(p=0.002)。移植后酪氨酸激酶抑制剂(TKI)维持治疗可独立改善移植前分子学MRD-患者的生存结局(OS:aHR 0.3,p=0.029;RFS:aHR0.3,p=0.019)。
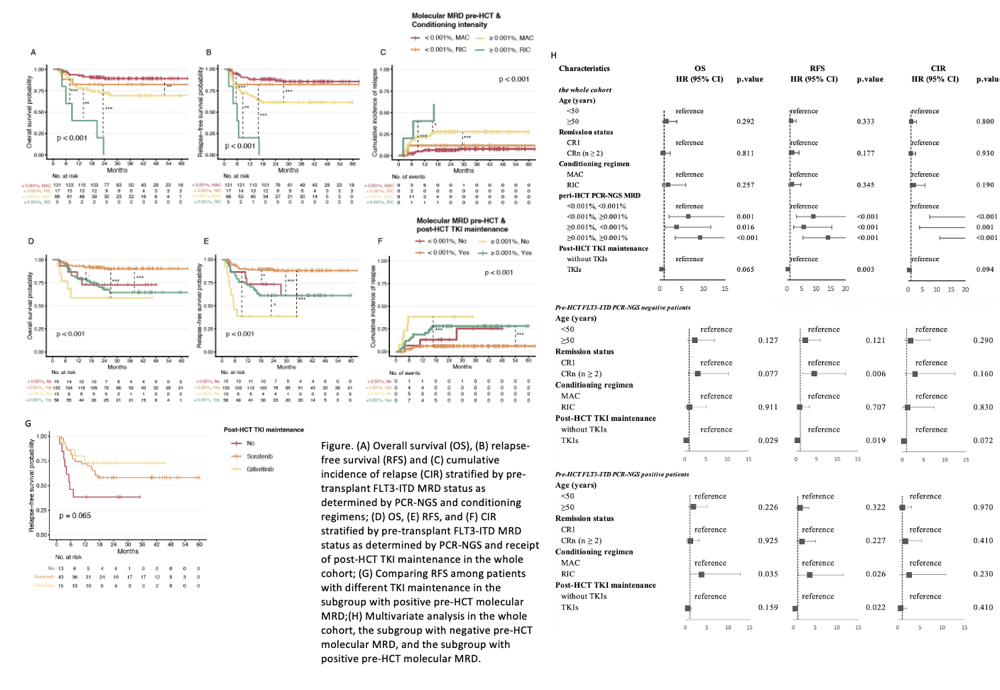
图8 (A)OS,(B)RFS,(C)由移植前FLT3-ITD MRD状态分层的CIR率,该状态由HSCT后NGS确定。(D)OS,(E)RFS,(F)CIR,由移植前FLT3-ITD MRD状态(由PCR-NGS确定)和接受HSCT后TKI维持的整个队列分层;(G)HSCT前分子学MRD+亚组不同TKI维持方式患者的RFS比较;(H)全队列多变量分析;HSCT前分子学MRD-亚组和HSCT前分子学MRD+亚组
研究结论:基于PCR-NGS的分子学MRD监测可实现动态风险分层,并可为FLT3-ITD突变AML患者的个体化移植策略提供依据,包括预处理强度选择及移植后TKI维持治疗方案优化,从而改善患者临床结局。
摘要号:OS18-01
ULTRA-LOW-DOSE IL-10-EXPRESSING CAR-T CELLS ACHIEVE ROBUST COMPLETE REMISSION IN R/R DLBCL: RESULTS UPDATE OF A PHASE I TRIAL
表达IL-10的超低剂量CAR-T细胞在复发/难治性(R/R)
报告人:付珊
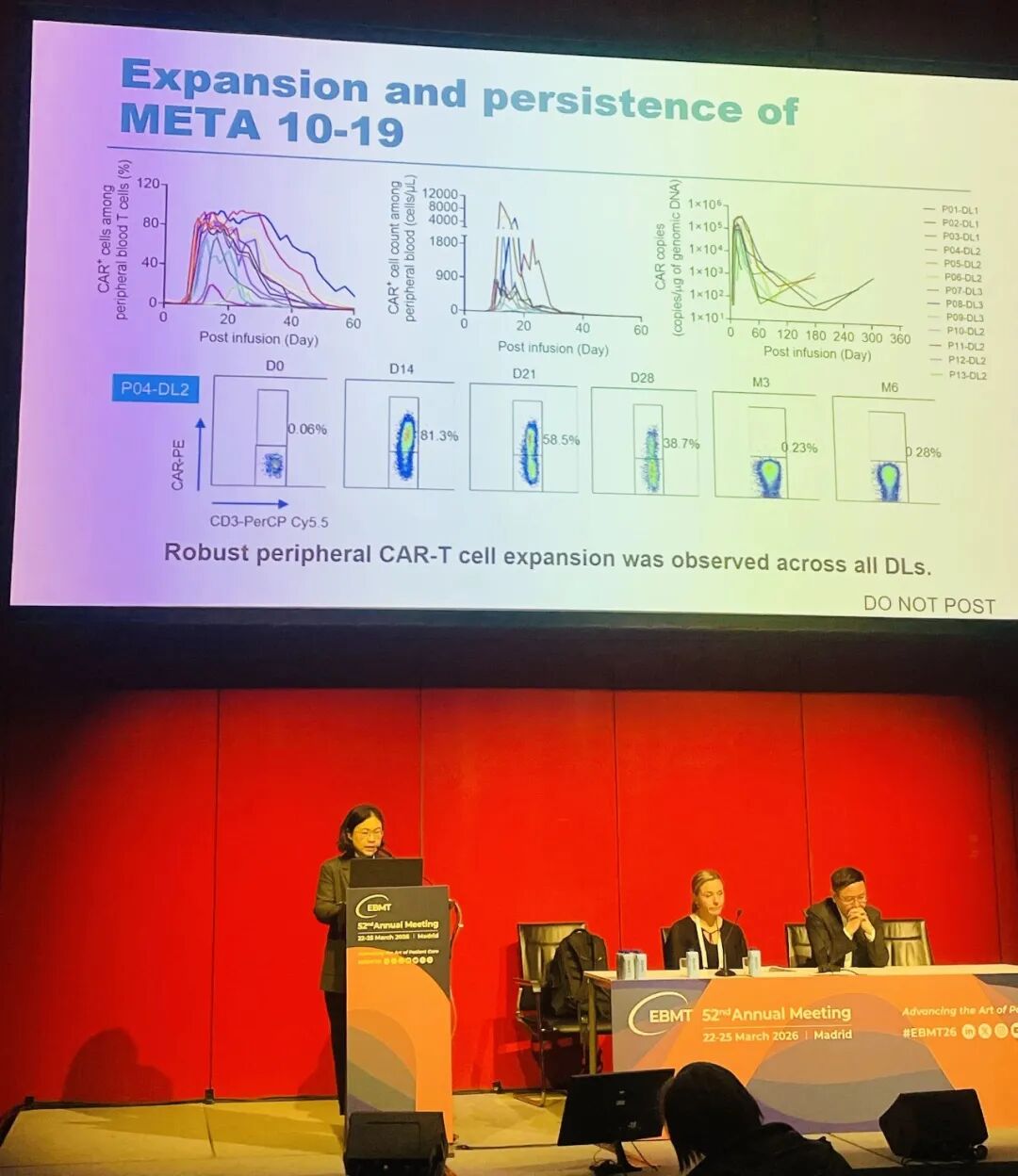
图9 付珊教授作报告
研究结果:截至2025年11月15日,ORR为100%,其中11例患者达CR(91.7%),1例达PR(8.3%)。12例患者发生细胞因子释放综合征(CRS),其中1级8例、2级3例、3级1例;2例患者发生免疫效应细胞相关的神经毒性综合征(ICANS),其中1级1例、2级1例。所有患者均表现出META 10-19在体内的强劲扩增能力,其峰值中位数为660.7个细胞/μL,同时伴随血清IL-10水平显著升高,峰值中位数为1,221.59 pg/mL。单细胞RNA测序(scRNA-Seq)显示,与IL-10⁻ CD8⁺ CAR-T细胞相比,IL-10⁺ CD8⁺ CAR-T细胞呈现出更强的增殖、活化、2型免疫反应及IL-10信号通路相关转录程序。
研究结论:超低剂量META 10-19在R/R DLBCL中表现出强效抗肿瘤活性、可控的安全性以及卓越的体内增殖能力。本研究采用的剂量范围(2×10³-2×10⁴ CAR-T细胞/kg)为迄今临床CAR-T治疗报道中的最低剂量,树立了疗效强度和临床可扩展性的新标杆。作为最早在R/R DLBCL患者中评估的细胞因子工程化CAR-T产品之一,META 10-19为侵袭性B细胞恶性肿瘤提供了一种新的治疗范式。未来仍需开展更大样本量、随访时间更长的研究,以验证其长期疗效持久性及其在血液系统肿瘤和实体瘤中的广泛应用前景。
摘要号:OS20-01
CO-INFUSION OF ANTI-CD19 AND ANTI-BCMA CAR-T CELLS FOR RELAPSED OR REFRACTORY NMOSD: A PHASE 1 CLINICAL TRIAL AND MECHANISTIC INSIGHTS
抗CD19与抗BCMA CAR-T细胞联合输注治疗R/R视神经脊髓炎谱系疾病(NMOSD):一项I期临床试验及机制研究
报告人:冯晶晶

图10 冯晶晶医生作报告
研究结果:2023年4月4日至2024年3月28日期间,共有9例患者接受治疗(中位年龄45岁,范围23-65岁;女性8例)。8例患者(89%)发生1级CRS;未观察到ICANS。≥3级细胞减少为一过性且可逆。所有患者均进入临床缓解;在中位随访505天(291-687天)后,7例患者(77.8%)仍保持无复发状态,且未再接受任何NMOSD治疗。所有受试者的血清AQP4-IgG均在3个月内降至检测限以下。1例患者于8个月时复发,并检测到新生的致病性B细胞克隆;单细胞分析显示,其CD16⁺非经典单核细胞缺失、调节性CD4⁺ T细胞减少、CD8⁺效应T细胞扩增并呈耗竭状态,同时干扰素-γ和淋巴毒素信号通路富集。
研究结论:同步输注抗CD19和抗BCMA CAR-T细胞治疗安全性良好,可诱导深度分子缓解,并使大多数高度难治性NMOSD患者实现无药物疾病控制。复发来源于促炎性免疫微环境中新生的自身反应性克隆,提示长期疗效可能依赖于以免疫调节为目标的辅助策略。未来仍需开展对照试验进一步验证。
在2026年EBMT年会上,浙江大学医学院附属第一医院黄河教授团队多项研究成功入选,展现了该团队在血液疾病治疗领域的持续研究进展。期待相关领域出现更多来自国内外中心的研究结果,共同推动血液疾病治疗证据体系的不断完善!

图11 黄河教授团队
编辑:Echo
审校:Vera,Julia
排版:Baa
执行:Baa
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)