转甲状腺蛋白淀粉样变性
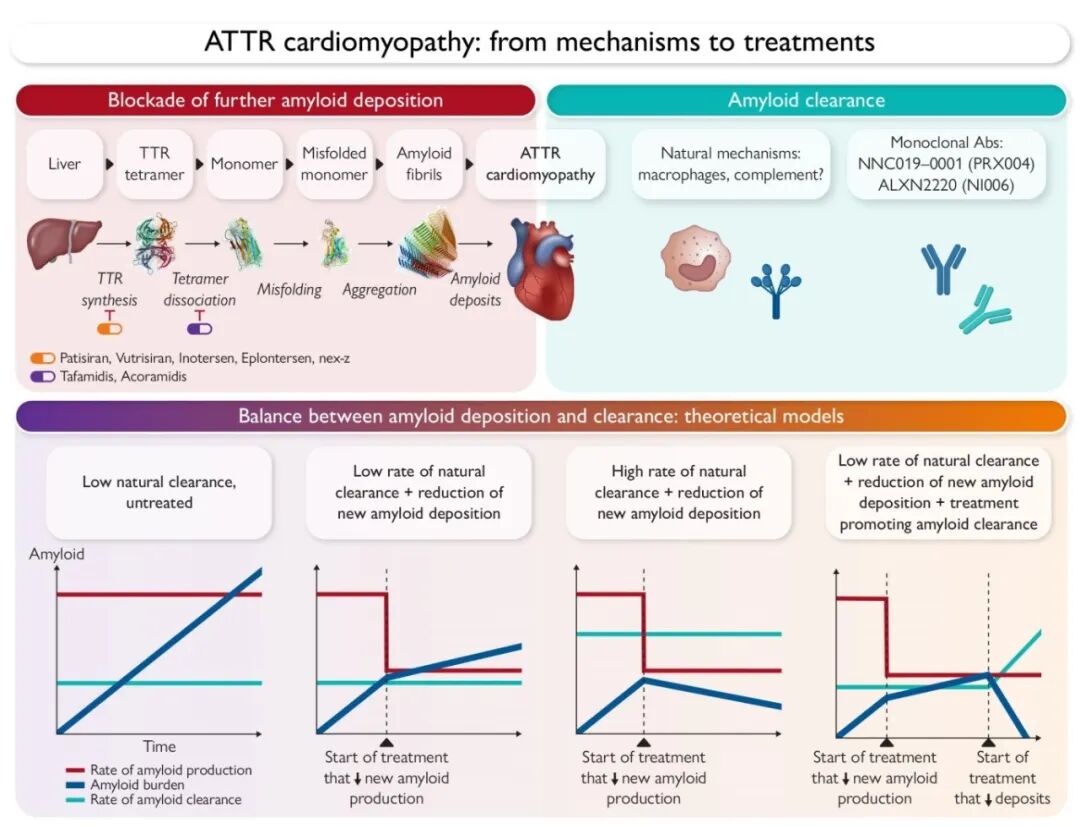
中心图
血清淀粉样蛋白P成分(SAP)闪烁扫描(内脏淀粉样沉积的定量诊断和监测工具)及心脏
淀粉样蛋白清除速率缓慢的原因和机制尚未明确。患者活检组织学评估显示,淀粉样蛋白沉积通常(但并非总是)会引发非常有限的炎症反应。实验性AA淀粉样变性小鼠模型及不同类型系统性淀粉样变性患者的研究证实,靶向淀粉样沉积的特异性抗体可显著加速内脏淀粉样蛋白清除。
小鼠模型证据表明,抗体加速清除涉及:经典补体途径激活、巨噬细胞募集、以及吞噬周围淀粉样物质的多核巨细胞生成。当补体或巨噬细胞功能缺陷时,该清除过程终止。人类证据进一步支持此机制:使用抗SAP抗体dezamizumab后发生快速内脏淀粉样清除的患者中观察到补体激活。致病性p.Val50Met TTR变异携带者的发病年龄受C1q功能变异影响,亦佐证补体途径在淀粉样病理中的作用。
所有获批疗法的首要目标均为阻止淀粉样蛋白在组织中进一步沉积,以延缓或终止疾病进展。在ATTR淀粉样变性领域,该目标可通过稳定转甲状腺素(TTR)四聚体(图1)或抑制其合成(图2)实现。
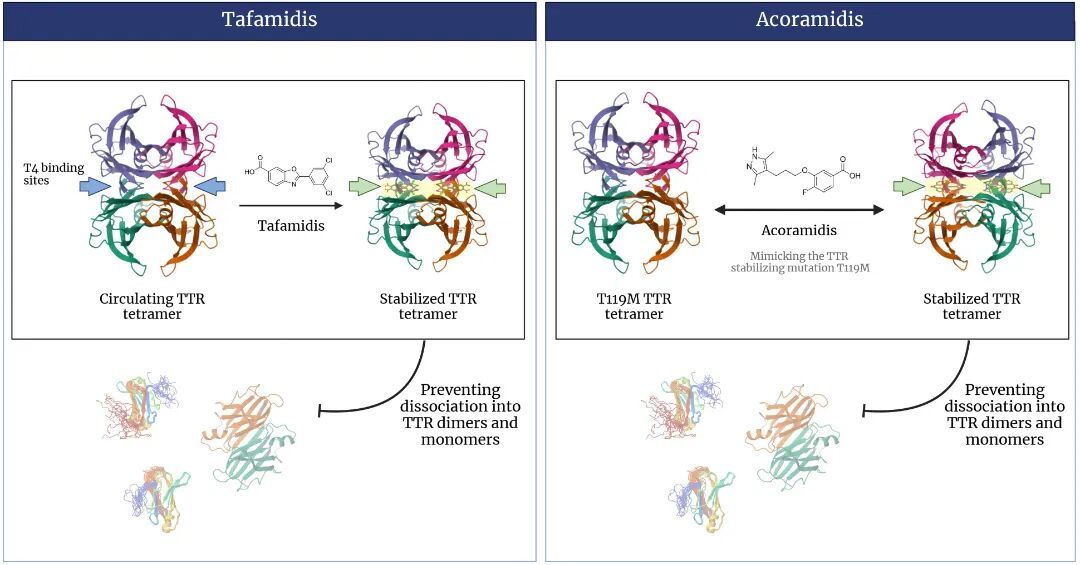
图1 TTR稳定剂的作用机制。
TTR稳定剂(tafamidis和acoramidis)在甲状腺素结合位点与TTR四聚体结合,并延缓四聚体解离为单体,这是淀粉样纤维生成的速率限制步骤
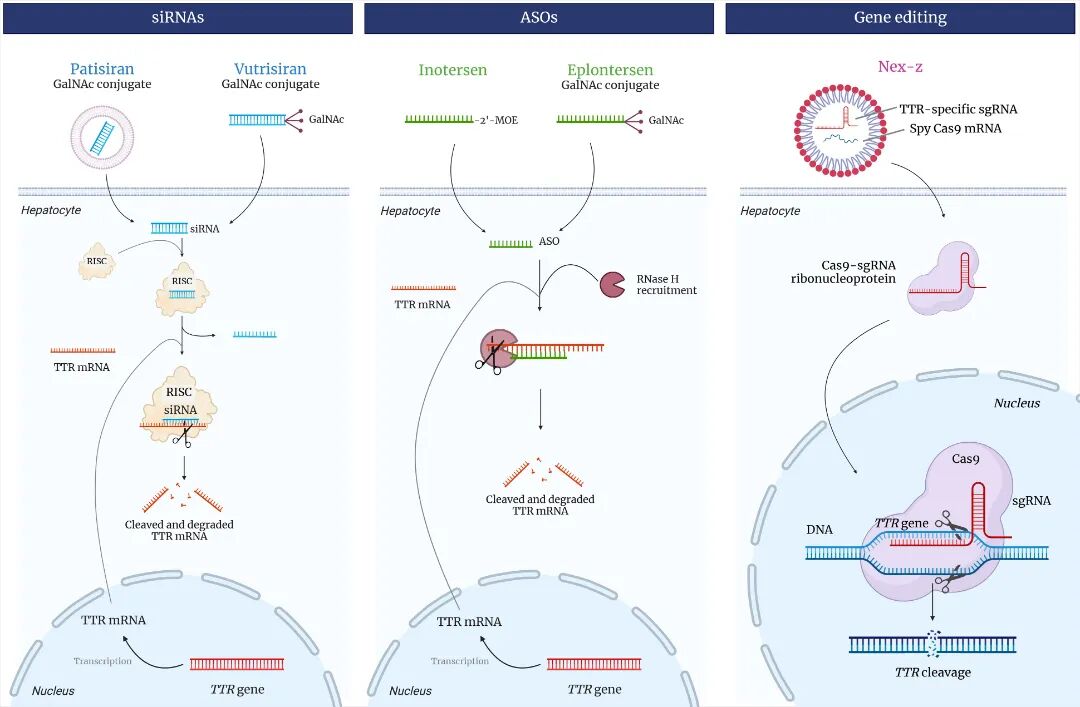
图2 TTR合成抑制剂的作用机制。
siRNA和ASO通过不同的分子机制促进TTR mRNA降解(图示意),最终阻断TTR合成。Cas,caspase;GalNAc,N-乙酰半乳糖胺;RISC,RNA诱导沉默复合体;sgRNA,单链引导RNA
(1)Tafamidis
Tafamidis 是一种小分子口服 TTR 稳定剂,通过结合TTR四聚体上的甲状腺素(T4)结合位点,减少其解离为单体TTR(淀粉样蛋白持续生成的底物)。
3期ATTR-ACT试验显示,相较于安慰剂,Tafamidis治疗可使野生型ATTR-CM(ATTRwt-CM)和变异型 ATTR-CM(ATTRv-CM)相关心衰患者的全因死亡率和心血管住院率降低约30%。纽约心脏协会(NYHA)心功能IV类患者被排除在研究之外,而接受Tafamidis治疗的NYHA心功能III级患者的心血管住院风险较高。与安慰剂相比,该药物减缓了患者功能状态和生活质量下降进程,且安全性和耐受性良好。Tafamidis成为首个获批治疗ATTRwt-CM和ATTRv-CM的疾病修正治疗药物。
ATTR-ACT的长期拓展(LTE)研究显示,基线NYHA心功能III级患者中,在ATTR-ACT期及LTE期持续接受Tafamidis治疗者死亡率较安慰剂交叉治疗者降低36%,提示其对NYHA心功能III级患者仍具预后获益。此外,Tafamidis还可改善运动耐量并逆转心脏重构。
(2)Acoramidis
Acoramidis作为一种新型TTR稳定剂,通过模拟Thr119Met TTR变异体效应,实现近完全的TTR稳定。
3期ATTRibute-CM试验证实其显著临床获益:复合主要终点(涵盖全因死亡、心血管住院、NT-proBNP较基线变化、6分钟步行距离[6MWD]较基线变化)得到改善。亚组分析显示NYHA心功能 III级患者使用Acoramidis未出现心血管住院风险升高。此外,该药治疗组循环TTR浓度显著高于安慰剂组及Tafamidis组,提示TTR浓度可作为反应TTR稳定及疗效的潜在循环生物标志物。但迄今尚无研究阐明循环TTR升高程度与临床状态改善或心血管结局的关联,故无法判定特定TTR升高阈值是否具有临床意义,亦不能据此区分治疗应答者或进行风险分层。
TTR由单一基因编码,几乎完全由肝脏合成。由于其生理功能与其他蛋白重叠,在补充
(1)siRNA
①patisiran
patisiran是一种脂质纳米颗粒包裹的siRNA药物,可抑制肝细胞野生型/变异型TTR生成。
APOLLO-B试验结果显示,治疗12个月时,相较于安慰剂组,patisiran组6MWD下降幅度(P=0.02)及堪萨斯城心肌病问卷总评分(KCCQ-OS)恶化程度(P=0.04)减小,但此统计学显著差异的临床意义尚未明确,故美国FDA未批准其用于ATTR-CM治疗。
②Vutrisiran
Vutrisiran是一种经化学结构优化、稳定性增强的TTR特异性siRNA,每12周皮下给药1次。
基于HELIOS-A试验中Vutrisiran在ATTRv-PN伴心脏受累患者中取得积极结果后,III期HELIOS-B试验(n=655)对其展开进一步研究。结果显示,Vutrisiran较安慰剂显著降低全因死亡率及心血管事件复发风险,并在保留运动耐量与生活质量方面(6MWD、KCCQ-OS评分)展现获益。该获益在总体人群、基线未联用Tafamidis亚组及多数亚组中一致显现,且不良事件发生率与安慰剂相当。近期,FDA已批准Vutrisiran用于ATTR-CM治疗。
③Nucresiran
Nucresiran(前称ALN-TTRsc04)是另一款在研的siRNA药物。
I期研究显示,单次给药≥300mg可快速敲低TTR,抑制效果至少持续至第180天,300mg剂量组在第360天TTR下降幅度仍超过70%。该药物患者间变异性低且耐受性良好。
(2)反义寡核苷酸(ASO)
①inotersen
III期NEURO-TTR试验显示,每周皮下注射inotersen(ASO类药物),持续15个月,可延缓ATTRv-PN患者神经功能衰退与生活质量下降。该研究人群63%合并ATTRv-CM,但该试验未观察到左心室收缩/舒张功能的显著变化。
而一项单中心研究对野生型及变异型ATTR-CM的患者随访24个月后发现,inotersen治疗组经CMR检测平均左心室心肌质量降低8%,6MWD较基线增加20米,提示运动耐量改善。
NEURO-TTR试验中约3%患者报告肾小球肾炎与重度
②eplontersen
新型ASO类药物eplontersen采用差异化结构偶联技术,可实现每月1次皮下给药。当前正在进行的III期CARDIO-TTRansform试验作为迄今最大规模的ATTR-CM研究,纳入超1400例患者,其关键特点还包括大规模CMR与心脏闪烁扫描亚组研究,预期2026年公布结果。
(3)基因编辑疗法
Nex-Z(前称NTLA-2001)作为一次性给药疗法,可通过靶向肝细胞TTR基因实现持久TTR抑制。
I期开放标签试验中,36例ATTR-CM患者接受Nex-Z单次静脉输注治疗。血清TTR呈现快速、显著、持续下降:输注后28天,TTR平均降幅达89%,12个月随访时维持90%抑制率。该效应在所有患者中均显现,部分可持续24个月。Nex-Z安全性良好,未出现非预期不良事件或治疗中断,无脱靶编辑临床证据。输注相关反应可控且短暂。12个月初步疗效分析显示:多数患者病情稳定。功能评估显示研究人群6MWD中位数增加5米,92%患者NYHA心功能分级在研究期间稳定或改善,心肺运动试验核心参数保持稳定。CMR等影像评估证实心脏结构与细胞外容积稳定,与临床表现一致。
仍需长期随访评估持久TTR抑制、基于CRISPR基因编辑的长期安全性及临床结局影响。正在进行的III期MAGNITUDE试验将提供部分关键数据。
基于AL/AA淀粉样变性经验及ATTRv-PN初步数据,作者提出理论框架(图3):血清TTR浓度降幅越大、持续性越强,ATTR-CM患者临床结局可能越好。
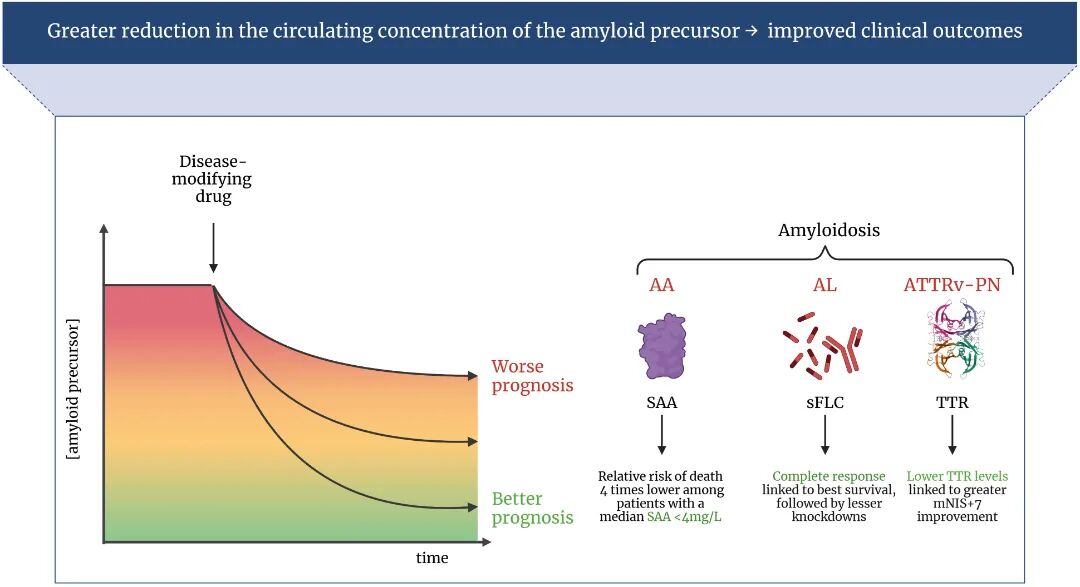
图3淀粉样前体蛋白与临床结局。
AA淀粉样变性的数据源于Lachmann等人;AL淀粉样变性资料来自Palladini等人;ATTRv-PN数据来自APOLLO-A试验。SAA,
尽管淀粉样蛋白清除机制在心脏中的相对作用,以及预防ATTR淀粉样蛋白沉积的具体价值尚不明确,通过靶向免疫应答增强ATTR淀粉样物质清除的策略展现重大潜力。
ALXN2220(前称NI006)是一种人源IgG1单克隆抗体,可特异性结合错误折叠TTR及ATTR沉积物特有的WEPFA线性表位,触发巨噬细胞吞噬ATTR聚集体从而加速纤维清除。
在首次人体、随机双盲、安慰剂对照、I期试验中,40例受试者数据显示:未出现明确药物相关严重不良事件,未检测到抗药抗体。多数不良事件为轻中度,且符合该人群疾病特征,少数报告轻度细胞因子释放综合征或一过性肌肉骨骼症状(如关节痛),经对症处理后缓解。部分患者出现短暂无症状性血小板减少(1例因此退出试验)。药代动力学显示该药半衰期2-3周,符合人IgG抗体特性。
影像学研究证实,随时间推移出现剂量依赖性心脏淀粉样负荷降低。探索性分析提示,高剂量组可能改善NT-proBNP与
目前 ALXN2220 正在开展 Ⅲ 期临床试验。
NNC6019-0001(前称PRX004)作为靶向错误折叠TTR单体及聚集体的新型人源化单抗,同样通过抗体介导吞噬作用促进淀粉样物质清除。2022年启动的II期试验计划纳入99例ATTR-CM患者,在标准治疗基础上比较NNC6019‑0001 30mg/kg、100mg/kg剂量组与安慰剂组治疗的疗效。核心终点包括第52周6MWD与NT-proBNP变化、心脏结构与功能参数演变、心血管住院及紧急心衰就诊发生率,以及患者报告生活质量。
当前多项创新疗法正处于临床探索阶段(图4,表1)。提升疗效的新兴策略聚焦多机制联合疗法。然而,完全阻断沉积能否实现淀粉样物质净清除平衡尚待验证。即将开展的临床试验将阐明深度TTR抑制能否显著降低淀粉样负荷并转化为临床获益。此外,创新疗法也会引发成本、可及性与公平性质疑。关键在于平衡治疗目标与医疗经济现实,保障潜在获益者的公平可及。
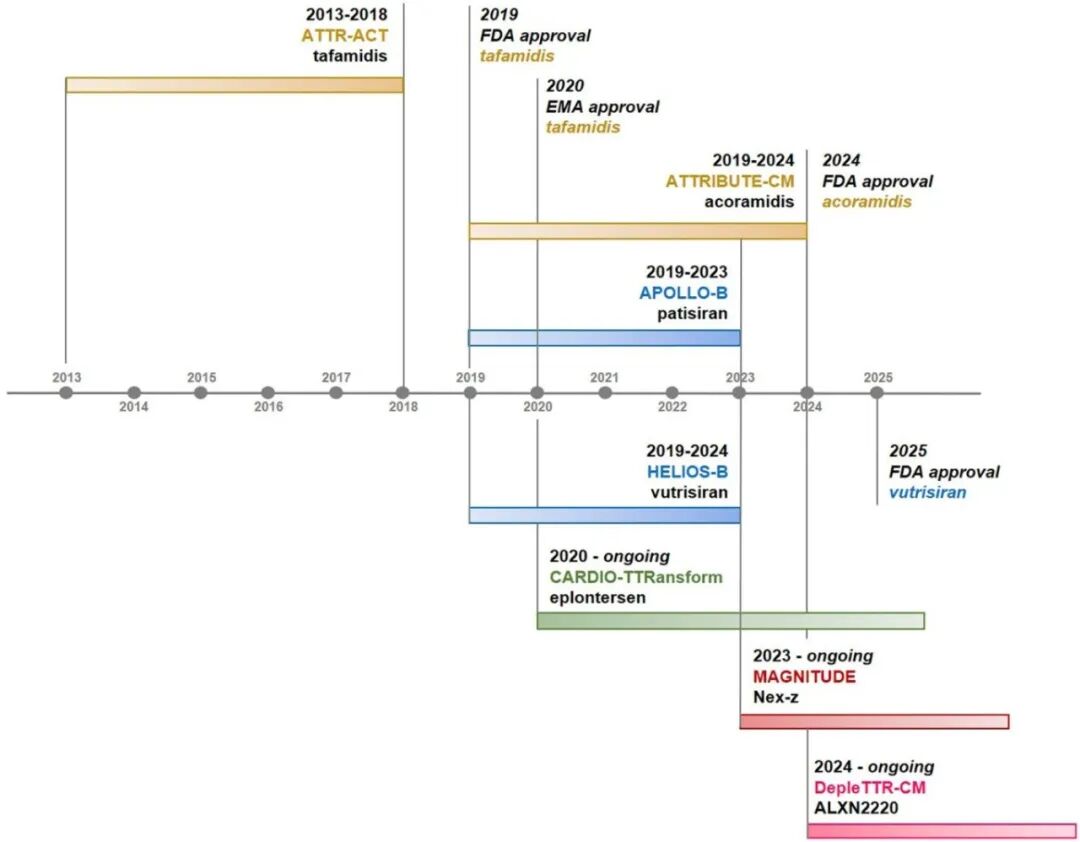
图4 ATTR-CM治疗演变。
图中标注已完成及进行中的III期临床试验,以及获FDA或EMA批准的年份。
表1 经批准或正在研究的疗法

尽管治疗创新显著拓展了ATTR-CM患者的治疗选择,关于最优疗法、患者筛选及疗效评估的迫切问题仍需持续研究。在直接临床对比数据完备前,以患者为中心的个体化多学科管理仍是提供高效诊疗的基石。
信源:Fontana M, Aimo A, Emdin M, Porcari A, Solomon SD, Hawkins PN, Gillmore JD. Transthyretin amyloid cardiomyopathy: from cause to novel treatments. Eur Heart J. 2026 Jan 5;47(1):54-63. doi: 10.1093/eurheartj/ehaf667. PMID: 41030053; PMCID: PMC12765559.
编辑&排版:siqili
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)