2025年,降脂治疗领域迎来多项突破性研究进展,内容涵盖PCSK9抑制剂适应证拓展与剂型更新、新型靶向疗法与基因编辑技术探索、脂蛋白(a)[Lp(a)]风险管控及特殊人群用药安全验证等方向。一系列高质量研究为临床降脂策略优化、高风险人群管理提供了坚实的循证依据,推动
近日,《European Heart Journal》期刊系统梳理了血脂异常领域最具影响力的10大研究进展,本文对此进行了整理,以飨读者。
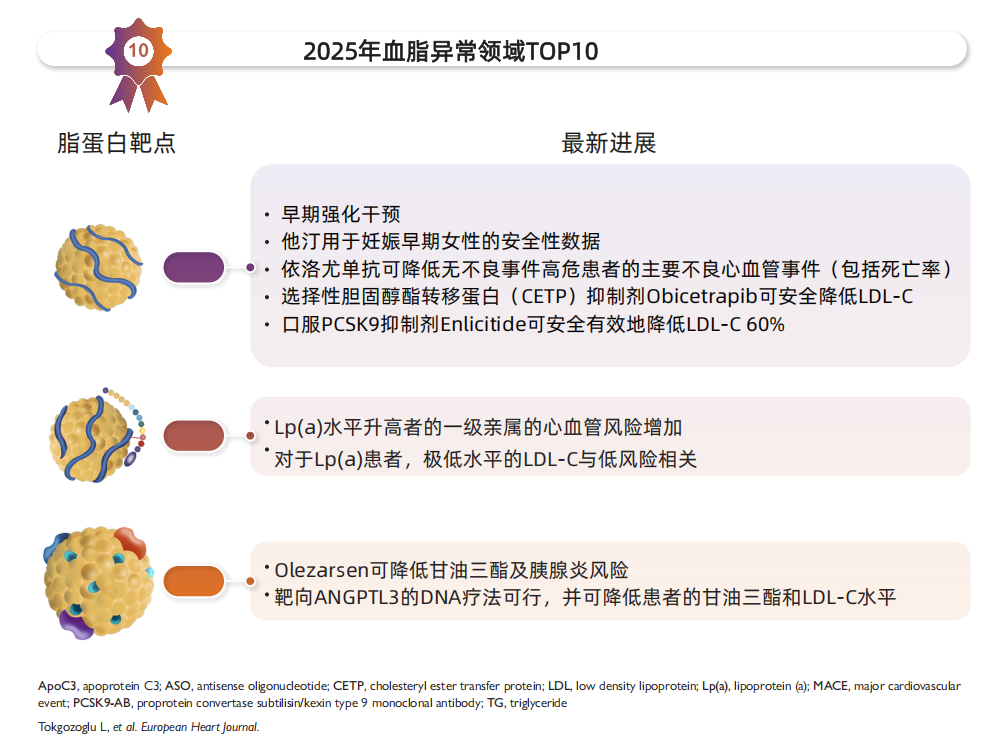
中心图
VESALIUS-CV研究为一项国际双盲安慰剂对照试验,共纳入12257例接受优化降脂治疗后LDL-C仍≥90 mg/dl的受试者。中位随访4.6年显示,PCSK9抑制剂
该研究拓展了强化降低LDL-C的证据基础,挑战了“一级预防”与“二级预防”的传统二分法,凸显了
相关链接
Enlicitide是首个口服PCSK9抑制剂,2025年发表的一项Ⅲ期临床试验证实,其在接受指南指导的药物(GDMT)治疗后血脂仍控制不佳的杂合子型
该研究共纳入303例患者(平均年龄52岁;51%为女性),均接受至少中等强度他汀类药物治疗(82%为高强度他汀;64%联合
患者在基线时的平均LDL-C水平为119 mg/dL。在第24周时,Enlicitide使LDL-C降低了58%,而安慰剂组则增加了3%(组间差异为-59%,P<0.001)。
在第52周时,降脂效应仍持续(Enlicitide组 vs.安慰剂组:-55% vs. +9%组间差异-62%,P<0.001),同时非高密度脂蛋白胆固醇(HDL-C)、载脂蛋白B(apoB)和Lp(a)分别下降52%、48%和25%。不良事件发生率与安慰剂组无显著差异。、
更大规模的CORALreef Lipids研究进一步证实,该药在2912名ASCVD确诊或高危患者中可使LDL-C降低达60%,超三分之二患者在他汀基础上实现了LDL-C<55 mg/dL,为不耐受注射制剂的患者提供了新选择。
值得一提的是,更大规模的CORALreef Outcomes研究仍在进行中,其旨在评估Enlicitide对罹患ASCVD或ASCVD高风险患者结局的影响,该研究结果公布后,有望显著扩大降脂治疗的选择范围。
相关链接
PCSK9在血浆中以游离形式及与LDL结合形式存在,但目前仍未明确这两种形式是否共享肝脏清除途径。
本研究发现,与游离型PCSK9相比,LDL结合型PCSK9的清除速度更慢,多配体聚糖-1(syndecan-1)可通过不依赖低密度脂蛋白受体(LDLR),由肝脏硫酸
这些数据表明,存在一条与脂质代谢和PCSK9 抑制剂药效学相关的次要清除途径,为理解PCSK9代谢稳态提供了新视角,尤其适用于LDLR缺乏或他汀治疗人群。此类替代途径或影响靶向PCSK9 的单克隆抗体或小干扰 RNA(siRNA)疗法的药代动力学及反弹动力学效应。
无论是遗传、药物诱导还是疾病相关(如糖尿病、
这些发现均提示,肝脏细胞外基质或为PCSK9代谢的一个潜在决定因素(此前未被充分认识),或可影响现有PCSK9靶向药物在某些代谢状态下的疗效,但其在人类中的生理相关性仍有待证实。
2025年发表的一项首次人体I期剂量递增试验评估了CRISPR-Cas9 mRNA/脂质纳米颗粒疗法(LNP)CTX310的安全性与有效性。
研究纳入了15例接受最大耐受治疗后,血脂仍控制不佳的血脂异常成人患者,单次静脉注射CTX310(0.1-0.8 mg/kg)进行治疗。主要研究终点为安全性及剂量限制性毒性;循环ANGPTL3蛋白水平作为药效学指标。
研究中,无剂量限制性毒性发生,仅3例患者出现了轻中度输液反应;2例患者出现了严重不良事件(1例椎间盘突出,1例
研究显示,ANGPTL3水平降低呈剂量依赖性,≥0.6 mg/kg剂量组60天内ANGPTL3持续下降≥70%,伴随LDL-C、甘油三酯均降低约50%,证实体内基因编辑的生物学疗效;为血脂异常“单次给药、长期维持”治疗模式提供了概念验证。然而,该研究受限于小样本、短随访,长期安全性与脱靶效应仍需严格监测与评估。
BROADWAY多中心、随机、安慰剂对照研究评估了选择性胆固醇酯转移蛋白(CETP)抑制剂obicetrapib在接受最大耐受降脂治疗的高危患者中的降脂疗效。研究纳入了来自中国、欧洲、日本和美国的多个中心的2530例患者,以2:1比例被随机分入obicetrapib治疗组(1686例,10 mg/d)和安慰剂组(844例,10 mg/d),为期1年。
研究的主要终点为从基线到第84天时,患者LDL-C水平的百分比变化。
基线时的平均LDL-C为98 mg/dL,第84天时Obicetrapib组的LDL-C降低29.9%,安慰剂组升高2.7%(组间差异-32.6%,P<0.001),同时Obicetrapib组的HDL-C升高136.3%,apoB、Lp(a)分别降低18.9%、33.5%,安全性与安慰剂组相当。该研究证实Obicetrapib可为难治性高胆固醇血症患者提供额外降脂获益。
相关链接
两项最新研究结果发布!无论是否联用依折麦布,Obicetrapib均可显著降低LDL-C和lp(a)水平| EAS 2025
严重高甘油三酯血症(sHTG)可增加
Olezarsen是一种靶向APOC3 mRNA的GalNAc偶联反义寡核苷酸(ASO)。两项Ⅲ期试验(CORE-TIMI 72a/72b)纳入1061例sHTG患者,每月注射一次Olezarsen(50 mg、80 mg)或安慰剂治疗12个月。
在第6个月时,经安慰剂效应校正后,72a研究50mg组和80mg组的甘油三酯变化分别为-62.9%和-72.2%,72b试验分别为-49.2%和-54.5%(所有P值均<0.001),且该疗效在12个月时仍持续。
此外,80 mg剂量的ApoC-III水平降低>80%,残余胆固醇水平降低50%-60%,非HDL-C水平降低30%-40%。
急性胰腺炎事件发生率不足安慰剂组的三分之一,安全性良好。研究证实了ApoC-III在甘油三酯代谢中的核心作用,为sHTG患者提供了有效治疗手段,但其长期肝脏、免疫安全性仍需长期随访试验证实。
相关链接
2025年发表的一项基于美国医保数据库的研究评估了Lp(a)是否会增加ASCVD复发风险,以及降LDL-C治疗是否能减轻这种关联。
研究共纳入273770例ASCVD确诊且检测Lp(a)水平的患者,中位随访5.4年显示,15%的患者ASCVD复发。结果提示,Lp(a)水平与复发风险呈连续正相关:与Lp(a)<15 nmol/L的患者相比,Lp(a)15-79 nmol/L、80-179 nmol/L、180-299 nmol/L及≥300 nmol/L组的校正后风险比(HR)分别为1.04、1.15、1.29和1.45。
亚组分析提示,进行高强度降脂治疗(尤其联合PCSK9抑制剂)可降低Lp(a)≥180 nmol/L带来的残余事件风险,为合并ASCVD的高Lp(a)患者的治疗策略提供了方向。
为评估Lp(a)水平升高(≥第80百分位)患者一级亲属的心血管疾病风险是否增加,研究者从瑞典STRIREG 队列中识别出41304例常规检测过血浆Lp(a)水平的个体,以及61715例未检测过Lp(a)的一级亲属,旨在探讨Lp(a)分层与主要不良心血管事件(包括心血管死亡、心肌梗死、缺血性卒中和冠状动脉血运重建)之间的关联。
中位随访19年显示,在Lp(a)<第80百分位和≥第80百分位的配对患者中,Lp(a)水平的一致性分别为86%和53%。一级亲属中MACE累积发病率随患者Lp(a)水平分层的升高而增加(P<0.001)。与最低Lp(a)分层的亲属相比,随患者Lp(a)分层升高,其一级亲属发生MACE的HR依次为1.08、1.30和1.28(趋势P<0.001)。Lp(a)水平升高者的一级亲属MACE 发生率更高,表明级联筛查可能有助于识别高风险一级亲属。
CARDIA队列研究纳入4366例18-40岁的年轻成人,随访22年,旨在探讨青年时期的apoB、LDL颗粒(LDL-P)和富含甘油三酯脂蛋白颗粒(TRL-P)累积暴露(定义为22年随访期内的总暴露量)及年均暴露量(由累积暴露量除以22年计算得出)与后续ASCVD发病的关系。
研究显示,apoB、LDL-P和TRL-P的累积暴露量每增加1个标准差(1 SD),40岁后新发ASCVD的HR分别为1.53(95%CI :1.36-1.72)、1.54(1.36-1.75)和1.48(1.30-1.68)。当18-40岁期间apoB年均暴露量>75 mg/dL时,ASCVD风险显著升高。
该研究提示,青年期累积暴露于致动脉粥样硬化性脂质颗粒,会增加个体中晚年发生ASCVD的风险;强调脂质暴露的“累积效应”,支持血脂异常的全生命周期管理,提示年轻人群早期干预的重要性。
近年来,育龄期女性使用他汀类药物的情况增加,探究其潜在致畸风险的必要性凸显。挪威全国性队列研究(2005-2018年)纳入803830例妊娠数据,旨在探讨孕早期他汀/调脂药物暴露与先天性畸形的关联,并更新2022年发表的一项荟萃分析。
在纳入的803830例受试者中,1255例为停药者,283例为暴露者,其余为非暴露者。校正混杂因素后,结果显示非暴露组、他汀停药组和暴露组的畸形率分别为4.3%、5.9%和6.7%。严重畸形的校正后比值比(aOR)分别为1.15(暴露组vs 未暴露组)和 1.08(暴露组vs 停用组),置信区间较宽。轻微畸形显示出相似的关联模式(aOR=0.94)。
未发现调脂药物暴露与心脏畸形相关(aOR=1.22,95%CI:0.50-3.01)。更新后的荟萃分析同样显示,降脂药物暴露并未增加主要畸形(aOR=1.06,95%CI:0.86-1.31)或心脏畸形(aOR=1.24,95%CI:0.94-1.64)的风险。
这些发现有助于让孕早期意外使用他汀的女性安心——现有证据并未表明应用他汀类药物存在明显的致畸风险。然而,不建议女性在妊娠期启动他汀类药物治疗。对于ASCVD风险极高或罹患纯合子家族性高胆固醇血症的女性,可在专科医生监督下根据具体情况考虑是否继续用药。
尽管暴露病例数较少,可能无法检测到罕见效应,但该研究增强了相关证据基础,或促使重新审视当前的妊娠期他汀类药物使用禁忌。
信源:The year in Cardiovascular Medicine 2025: the top 10 papers in dyslipidaemias. Eur Heart J. 2026 Jan 14:ehaf1045. doi: 10.1093/eurheartj/ehaf1045. Epub ahead of print. PMID: 41529940.
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)