2026年3月2日,艾伯维宣布其III期、随机、安慰剂对照、双盲AFFIRM研究取得了积极结果。该研究旨在评估利生奇珠单抗皮下诱导治疗对比安慰剂,用于中重度活动性
CD是一种慢性全身性疾病,以胃肠道炎症为主要表现,最常累及小肠末端(回肠)与结肠,可导致持续性
利生奇珠单抗是一种白细胞介素(IL)-23抑制剂,通过结合IL-23的p19亚基选择性阻断IL-23。IL-23是参与炎症反应的细胞因子,与多种慢性免疫介导性疾病相关。目前,基于既往研究(CD:ADVANCE和MOTIVATE诱导研究、FORTIFY维持研究;
这些研究主要采用静脉诱导给药后皮下维持的方案,AFFIRM研究评估了利生奇珠单抗皮下注射作为诱导治疗的疗效与安全性,探索了更为便捷的给药方案的可能性。
AFFIRM是一项全球多中心、III期、随机、安慰剂对照、双盲研究,旨在评估利生奇珠单抗皮下给药作为诱导治疗,用于中重度活动性CD成人患者的有效性与安全性。共同主要终点为达到第12周克罗恩病活动指数(CDAI)临床缓解(CDAI<150)患者比例及内镜应答患者比例。
共有289例患者以2:1的比例随机分配接受利生奇珠单抗皮下给药或安慰剂治疗。两组人口统计学与基线特征总体均衡,65%患者既往接受CD先进疗法治疗失败。
研究结果显示,第12周时,接受利生奇珠单抗皮下诱导治疗的患者,达到CDAI临床缓解及内镜应答的比例均显著高于安慰剂组:临床缓解率55% vs 30%(P<0.0001);内镜应答率44% vs 14%(P<0.0001)。
表1 AFFIRM研究第12周共同主要终点结果
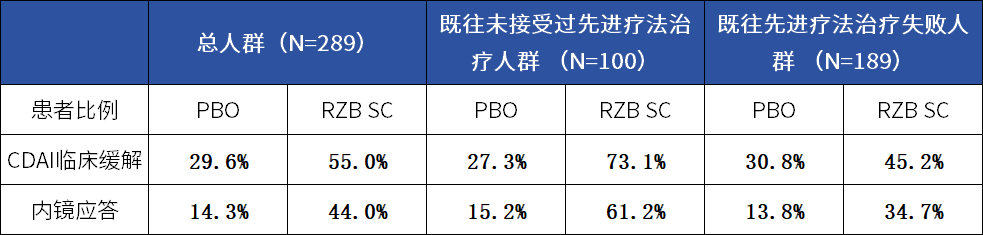
注:RZB:利生奇珠单抗;PBO:安慰剂;SC:皮下注射
在利生奇珠单抗皮下诱导治疗12周获得临床应答、并继续维持治疗12周的患者中,第24周CDAI临床缓解率为67%,内镜应答率为57%。
值得注意的是,这项III期研究入组患者以难治性人群为主(65%),其中50%患者既往≥2种先进疗法治疗失败,23%患者
安全性方面,在12周双盲、安慰剂对照阶段,利生奇珠单抗皮下给药的安全性特征与既往CD研究一致,未出现新的安全风险。利生奇珠单抗组最常见不良事件为
AFFIRM研究主要研究者、北卡罗来纳大学教堂山分校胃肠病学和肝病学系主任Millie D. Long博士指出:“CD是复杂且常致残的疾病,不仅影响消化健康,还会干扰患者工作、社交与日常生活。本研究在各人群中均观察到较高的内镜应答率,尤其在既往未接受过先进疗法治疗的患者中,提示利生奇珠单抗皮下诱导治疗有望成为CD的有效治疗方案。”
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)