适时精准用药是
The right drug at the right time: key to IBD success
Trends in Molecular Medicine
PMID: 41314864 [IF=13.8]
来源:IBD Daily
炎症性肠病 (IBD) 包括
近年来,单细胞和空间转录组学的研究揭示:IBD的免疫表型并非一成不变,而是随着病程进展、炎症部位、甚至既往治疗史而动态演变。这意味着,单一的“标准治疗方案”难以覆盖所有患者,“在合适的疾病阶段,给合适的患者,用合适的药物”,正成为IBD精准治疗的新方向。
本篇综述系统梳理了IBD不同阶段的免疫特征与细胞因子网络演变,提出了一种“阶段匹配治疗”的新思路,并结合现有药物机制,探讨如何在临床实践中实现真正的个体化治疗。
1. IBD的免疫变化
IBD是消化道的慢性复发缓解性炎症性疾病,主要包括CD和UC。CD的特征是透壁性炎症,可影响胃肠道的任何部位,而UC则是局限于结肠黏膜的浅表性炎症。尽管IBD的病因尚不完全清楚,但普遍认为遗传易感个体对肠道微生物的免疫应答失调是驱动疾病发生发展的核心机制。单细胞和空间转录组学的最新进展揭示了IBD亚型之间及内部的独特免疫机理,为理解疾病机制和开发靶向疗法提供了全新视角。
2. 贯穿IBD各阶段的细胞因子动力学
越来越多的证据表明,IBD中的细胞因子网络随着疾病阶段和病变部位动态演变。在IBD早期活动期,上皮屏障功能障碍触发先天性和适应性免疫激活,CD中主要表现为1型T辅助细胞 (TH1) 和TH17在免疫应答中占主导地位,IFN-γ和IL-17介导的信号驱动巨噬细胞活化和黏膜损伤。值得注意的是,IL-17阻断在临床试验中的失败提示该细胞因子可能具有黏膜保护作用,凸显了细胞因子网络的复杂性。在UC中,除TH17扩增外,还观察到IgG+浆细胞显著增加,表明B细胞参与度更高。
随着炎症持续,细胞因子格局转向促进组织重塑和纤维化的通路。IL-23和IL-22信号在回肠中富集,通过促进上皮再生和先天性淋巴细胞活化维持慢性炎症。空间转录组学研究发现,局部IFN-γ反应中心和TREM2+巨噬细胞与非消退性炎症有关,提示这是一种适应不良的修复尝试。此外,先天性淋巴细胞的失调也在IBD进展中发挥积极作用。
3. 细胞因子动力学对治疗药物选择的启示
理解细胞因子动态变化为靶向治疗的选择和排序提供了理论依据。抗TNF药物在细胞因子丰富的活动期仍然有效,而抗IL-12/IL-23疗法或JAK抑制剂可能更好地解决由IL-23依赖性通路驱动的慢性重塑炎症。整合细胞和分子生物标志物,有望识别可能对特定生物制剂或小分子有应答的患者,优化联合治疗策略,降低治疗失败风险。
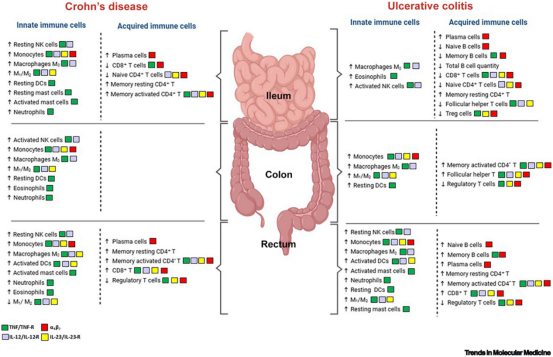
图1 炎症性肠病患者肠黏膜的区域异质性与免疫细胞重分布。
肠道免疫系统在肠道不同部位呈现出显著的异质性,受区域功能差异、部位特异性内在因素及环境因素的影响。在炎症性肠病中,这种有序结构被破坏,不同肠段 (如回肠、结肠、直肠) 出现独特的免疫细胞组成与细胞因子谱。
1. 常规疗法
在常规治疗中,诱导缓解通常依赖于短程中高剂量皮质类固醇,在6-12周内逐渐减量并停用,同时UC患者继续使用治疗剂量的氨基水杨酸盐。免疫调节剂如硫嘌呤和甲氨蝶呤曾用于类固醇依赖性患者的长期维持治疗,但目前已基本被更有效和安全的疗法所取代,很少作为单药使用。
2. 生物制剂
抗TNF药物通过直接中和TNF抑制炎症,同时诱导巨噬细胞和T细胞凋亡,发挥免疫调节作用。目前获批的四种抗TNF药物 (英夫利西单抗、阿达木单抗、戈利木单抗、培塞利珠单抗) 在结构、给药途径和药代动力学特性上存在差异,总体有效且耐受良好,但需关注感染和免疫原性风险。
抗整合素药物通过阻断白细胞表面的整合素,抑制其向肠道炎症组织迁移。维多珠单抗选择性靶向α4β7整合素,精准抑制肠道淋巴细胞归巢,具有良好的安全性特征,特别适用于需长期治疗的患者。那他珠单抗因非选择性抑制α4亚基,与进行性多灶性白质脑病风险相关,临床应用受限。
抗IL-12/IL-23药物如乌司奴单抗,通过靶向IL-12和IL-23共有的p40亚基,调节TH1和TH17细胞介导的适应性免疫应答。抗IL-23药物 (古塞库单抗、瑞莎珠单抗、米利珠单抗) 则选择性结合IL-23的p19亚基,提供更特异的治疗选择,显示出良好的黏膜愈合率和安全性特征。
3. 小分子药物
JAK抑制剂通过阻断JAK-STAT通路,抑制多种促炎细胞因子的信号传导。托法替尼、菲戈替尼和乌帕替尼已获批用于IBD治疗,口服给药方便,起效迅速,但需关注感染 (尤其是带状疱疹)、血脂异常等风险。
S1P受体调节剂通过诱导淋巴细胞滞留于淋巴结,减少肠道炎症浸润。奥扎莫德和伊曲莫德已获批用于治疗UC,具有肠道选择性优势,但需在用药前评估心血管和眼部风险,治疗期间监测肝功能和血常规。
1. 克罗恩病的分阶段治疗策略
在CD的早期炎症阶段,抗TNF药物 (英夫利西单抗或阿达木单抗) 是一线选择,能快速抑制TH1主导的炎症。对于中重度患者,英夫利西单抗联合硫嘌呤可降低免疫原性,实现更深缓解。随着疾病进展,当出现IL-23/TH17主导的慢性炎症时,抗IL-23药物 (瑞莎珠单抗) 或JAK抑制剂可能更具优势。
肛周瘘管型CD是特殊挑战,通常由TNF介导。英夫利西单抗联合手术引流是一线选择,较高血清药物水平与较高瘘管愈合率相关。对抗TNF无效者,可考虑乌司奴单抗或维多珠单抗,乌帕替尼在部分患者中也显示出潜力,但需更多真实世界数据验证。
2. 溃疡性结肠炎的分阶段治疗策略
UC早期表现为TNF和TH1/TH17主导,轻度直肠炎可单独使用局部5-氨基水杨酸盐或直肠类固醇。对于常规治疗无效的孤立性直肠炎,伊曲莫德显示出独特优势。广泛性或左半结肠UC,抗TNF药物是常用选择,维多珠单抗在头对头试验中优于阿达木单抗,特别适用于体弱患者。
慢性或类固醇依赖性UC常表现强烈的IL-13、IL-9和IL-17表达,此时抗IL-23药物或JAK抑制剂可能更为合适。对于多线治疗失败的难治性UC,IL-23选择性阻断或JAK抑制剂 (如乌帕替尼) 可作为二线选择。
3. 治疗决策的个体化考量
先进疗法的选择应综合考虑:(1) 疾病表型:是否存在瘘管、肠外表现;(2) 患者因素:年龄、合并症、既往治疗反应;(3) 预测性生物标志物:如oncostatin M (OSM) 高表达预示抗TNF疗效差,应考虑抗IL-23或JAK抑制剂;(4) 安全性特征:感染高风险者优先选择肠道选择性药物如维多珠单抗。治疗药物监测可帮助优化抗TNF治疗,减轻免疫原性,联合治疗可提高缓解率并延长治疗获益。
尽管当前临床决策仍主要依赖疾病严重程度和内镜下表现,但越来越多证据支持引入免疫通路相关标志物指导治疗选择。C反应蛋白和粪便钙卫蛋白仍是评估炎症的核心指标,但无法区分具体的免疫通路。新兴的标志物包括:OSM (预测抗TNF疗效差)、avβ6自身抗体 (UC特异性,提示屏障功能缺陷)、粪便BAFF (B细胞活化标志,与内镜活动度相关)、microRNA panels (可能与激素抵抗和TH17表型相关)、PGE-MUM (尿中前列腺素代谢产物,反映UC活动度)。
这些标志物目前主要处于研究阶段,尚未广泛应用于临床决策,但未来有望整合入临床实践,实现动态监测和精准切换治疗。当生物标志物与内镜结果不一致时,应以达标治疗为目标,优先追求内镜愈合,避免过度解读单次检测结果。
IBD患者肠道存在过度激活的先天性和适应性免疫应答,同时具有疾病特异性和部位特异性的免疫特征。从早期到慢性阶段的转变过程中,细胞因子网络的动态变化揭示了IBD发病机制的差异性免疫病理,为靶向治疗的设计提供了重要框架。实现"正确阶段应用正确药物"需要综合考虑疾病表型、患者因素、预测性生物标志物和安全性特征。未来,将细胞因子特征转化为实用的临床工具,整合入基于严重程度的治疗算法,有望推动IBD治疗从经验性决策向真正个体化、动态优化的精准医疗模式演进。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)