Mirikizumab治疗中重度活动性
Efficacy and safety of mirikizumab in paediatric participants with moderately-to-severely active ulcerative colitis (SHINE-1): a multicentre, open-label, non-randomised phase 2 trial
The Lancet Gastroenterology & Hepatology
PMID: 41270771 [IF=38.6]
来源:IBD Daily
米吉珠单抗 (Mirikizumab) 是一种人源化免疫球蛋白G4单克隆抗体,靶向IL-23的p19亚基,已在溃疡性结肠炎 (UC) 和
这是一项为期52周的多中心、开放标签、非随机的II期研究,在加拿大、以色列、日本、韩国和美国的19个研究中心开展。研究纳入2岁至未满18岁、且对皮质类固醇、免疫调节剂、生物制剂或JAK抑制剂治疗应答不足、失应答或不耐受的中重度活动性UC患者。受试者在第0、4、8周接受静脉注射mirikizumab诱导治疗,剂量为5 mg/kg或10 mg/kg (体重≤40 kg),或300 mg (体重>40 kg)。临床应答情况依据改良Mayo评分 (mMS) 评估。第12周达到治疗应答的受试者进入治疗维持期,在第12至48周期间每4周接受一次mirikizumab皮下注射治疗,剂量为50 mg (体重≤20 kg)、100 mg (体重>20 kg且≤40 kg) 或200 mg (体重>40 kg)。第12周治疗无应答者则额外接受3次静脉诱导给药 (体重≤40 kg者10 mg/kg,体重>40 kg者300 mg,每4周一次) ,随后转为皮下注射维持治疗。鉴于药代动力学 (主要终点) 数据此前已发表,本文主要报告安全性和疗效等次要结局指标。改良意向性治疗 (mITT) 和安全性分析集人群纳入了所有至少接受过一次研究药物治疗的受试者,无论其对研究方案或治疗的依从性如何。
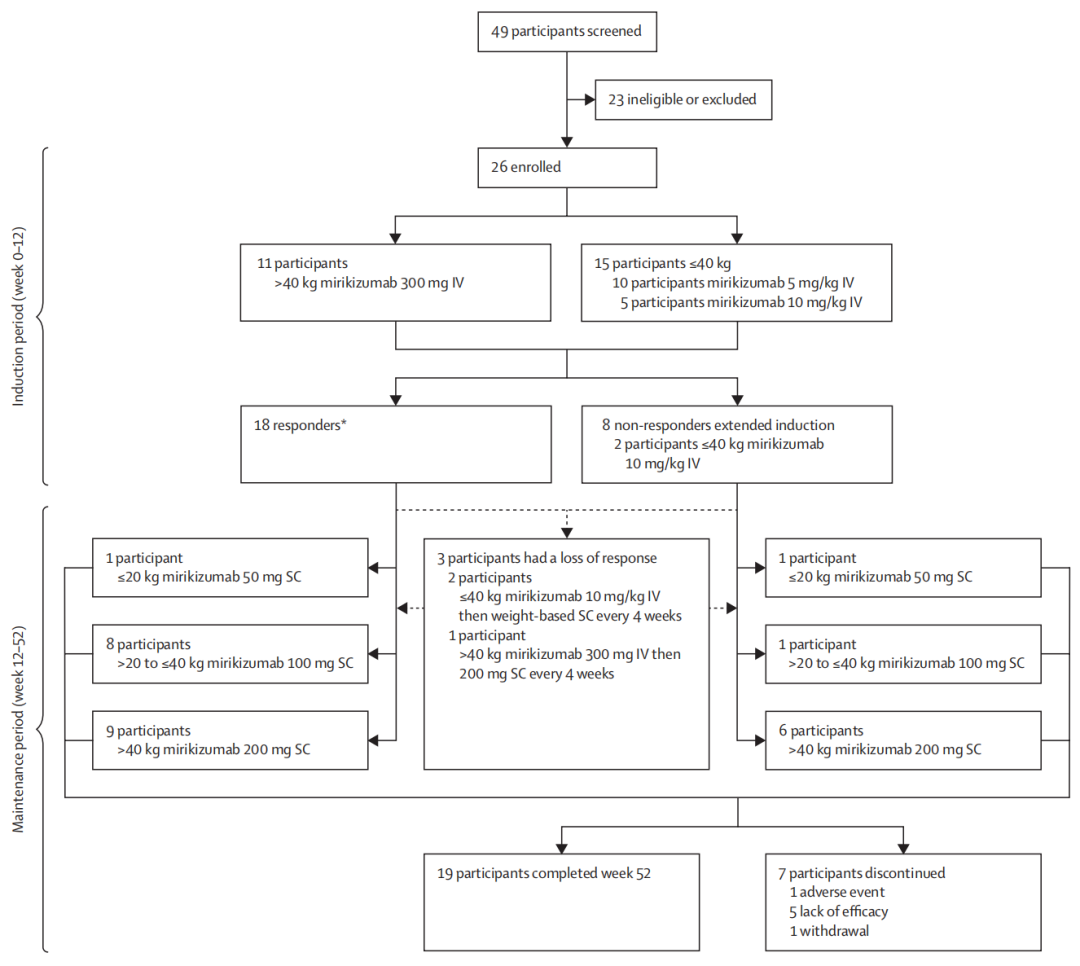
图1. 试验流程图。
注:IV, 静脉给药; SC, 皮下给药。临床应答的定义为改良Mayo评分较基线下降≥2分且降幅≥30%,同时直肠出血评分较基线下降≥1分或直肠出血评分为0或1。
2020年5月18日至2023年3月15日期间,研究共纳入26名受试者;平均年龄为11.8岁 (标准差 [SD] 3.4),平均体重为40.5 kg (SD 16.0)。受试者中女性15例 (58%),男性11例 (42%)。
第12周时,基于mMS评估,18例 (69.2%, 95% CI 50.0-83.5) 受试者获得临床应答,10例 (38.5%, 95% CI 22.4-57.5) 受试者达到临床缓解。此外,14例 (53.8%, 95% CI 35.5-71.2) 实现内镜下缓解,4例 (15.4%, 95% CI 6.2-33.5) 受试者达到组织学-内镜黏膜改善 (HEMI),1例 (3.8%, 95% CI 0.7-18.9) 达到组织学-内镜黏膜缓解 (HEMR),12例 (46.2%, 95% CI 28.8-64.5) 实现症状缓解。若依据儿童UC活动指数 (PUCAI) 评估,第12周时26例受试者中有20例 (76.9%, 95% CI 57.9-89.0) 获得临床应答,10例 (38.5%, 95% CI 22.4-57.5) 达到临床缓解。
第52周时,基于mMS评估,26例受试者中有14例 (53.8%, 95% CI 35.5-71.2) 受试者获得临床应答,10例(38.5%, 95% CI 22.4-57.5) 受试者处于临床缓解状态;基于PUCAI评估,14例 (53.8%, 95% CI 35.5-71.2) 受试者获得临床应答,13例 (50.0%, 95% CI 32.1-67.9) 受试者处于临床缓解状态。内镜及黏膜结局方面,第52周时10例 (38.5%, 95% CI 22.4-57.5) 受试者处于内镜下缓解状态,9例 (34.6%, 95% CI 19.4-53.8) 受试者达到HEMI,9例 (34.6%, 95% CI 19.4-53.8) 受试者达到HEMR,12例 (46.2%, 95% CI 28.8-64.5) 受试者处于症状缓解状态。此外,截至第52周,有10例 (38.5%, 95% CI 22.4-57.5) 受试者在此前至少12周未使用皮质类固醇或未接受UC相关手术的情况下达到了临床缓解。
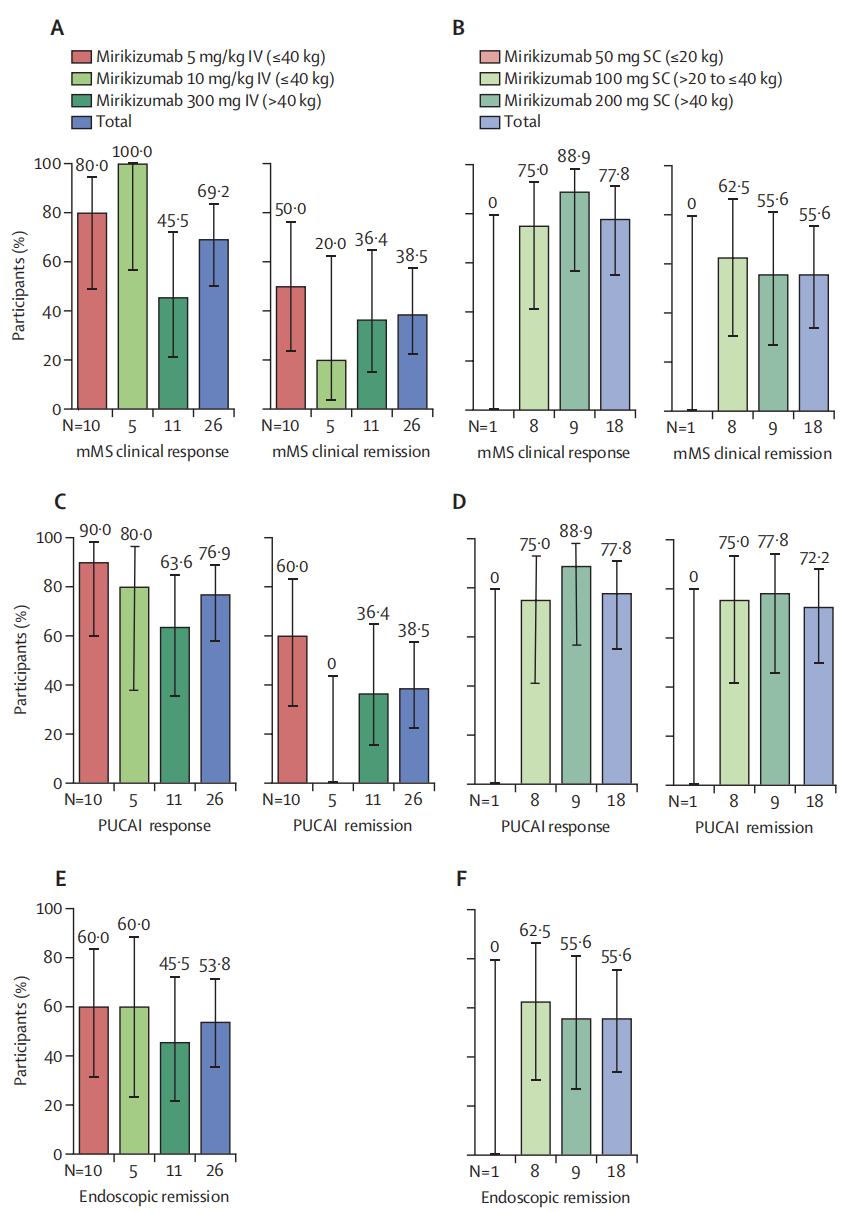
图2. 第12周和第52周的缓解与应答情况。
注:本图展示了诱导期 (第12周;mITT人群;图A、C和E) 和维持期 (第52周;第12周时mMS评估的治疗应答者;图B、D和F) 的疾病活动度情况,评估指标分别为mMS (图A和B)、PUCAI (图C和D) 以及内镜下缓解 (图E和F)。所有分析均采用无应答插补法。IV, 静脉给药; mITT, 改良意向性治疗; mMS, 改良Mayo评分; PUCAI, 儿童溃疡性结肠炎活动指数; SC, 皮下给药。
在诱导期和维持期内,共有3例 (12%) 受试者发生严重不良事件 (分别为非感染性
Mirikizumab在中重度活动性UC儿童受试者中表现出良好的安全性和疗效。研究结果支持进一步在儿童群体中评估mirikizumab。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)