
2026年4月1日,美国食品药品监督管理局(FDA)正式批准礼来公司(Eli Lilly and Company)口服
Foundayo被批准用于结合低热量饮食和增加体力活动,用于患有肥胖,或伴有至少一种体重相关合并症的超重成人患者,以减轻多余体重并长期维持减重效果。

此次审批不仅为全球减重领域带来了一款重磅口服新药,更创下了FDA自2002年以来新分子实体(NME)的最快审批纪录,标志着药品监管审批机制的一次历史性突破。
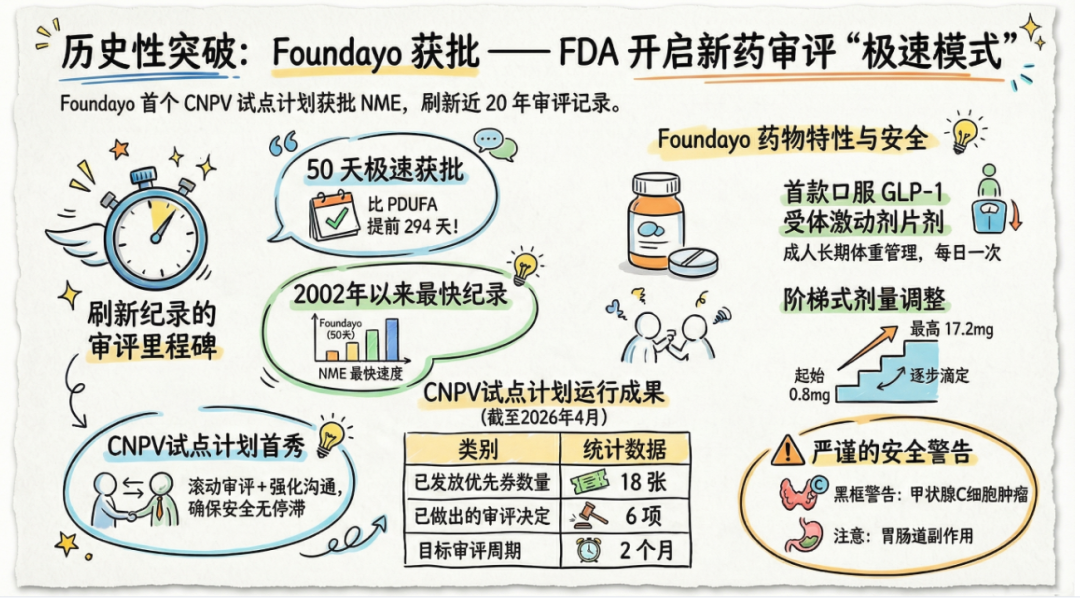
Foundayo的审评速度堪称“破冰”之举。该药物是FDA局长国家优先审评凭证(the Commissioner's National Priority Voucher,CNPV)试点项目下的第五款获批药物,更是该项目下首个获批的新分子实体(NME)。
具体而言,Foundayo在提交申请后仅50天即获批,比原定于2027年1月20日的《处方药使用者付费法案》(PDUFA)目标日期提前了整整294天。CNPV试点项目于2025年启动,旨在通过加强沟通和滚动审查,在不影响安全性的前提下缩短关键国家卫生优先事项的审查时间,其目标审批周期定为两个月。截至目前,FDA已颁发了18张凭证,并做出了6项决定。
FDA局长Martin Makary医学博士对此评价道:“这次获批展示了当我们消除延误、优先考虑机构与行业合作伙伴快速而彻底的工作时,FDA能够取得怎样的成就。这反映了公众对FDA应有的期望。”
作为一款口服制剂,Foundayo的给药途径为减重患者提供了极大的便利。FDA药物评估与研究中心(CDER)代理主任Tracy Beth Høeg博士特别指出,超重或肥胖人群现在有了一种新的选择——“一种不需要空腹服用的GLP-1受体激动剂口服制剂”。
在给药方案上,Foundayo采用严谨的阶梯式剂量递增策略,以确保治疗反应和耐受性:
起始剂量:每日一次,每次0.8 mg。
首次递增:用药至少30天后,剂量增加至2.5 mg。
后续递增:再经过至少30天后,剂量可增加至5.5 mg。
剂量维持:根据患者的个体治疗反应和耐受性,后续仍可按照每层级至少30天的间隔,进一步将剂量逐步上调至9 mg、14.5 mg,乃至最高17.2 mg。
Foundayo的疗效在两项随机、双盲、安慰剂对照的临床试验中得到了有力证实。这两项试验均针对患有肥胖,或患有超重且伴有至少一种体重相关合并症的成年人群体。
试验结果显示:在配合低热量饮食和增加体力活动的基础上,接受Foundayo治疗72周的患者组,其体重较安慰剂组出现了具有统计学意义且具有临床价值的显著下降。这为该药物的长期体重管理功效提供了坚实的临床证据支持。
尽管疗效显著,但基于GLP-1类药物的共性及现有临床数据,Foundayo的药品说明书中包含了严格的安全性警告。
1. 黑框警告(Boxed Warning): 该药的标签中带有针对甲状腺C细胞肿瘤的黑框警告。明确规定:对于有甲状腺髓样癌个人史或家族史的患者,或患有多发性内分泌肿瘤综合征2型(MEN 2)的患者,应禁止使用Foundayo。
2. 常见不良反应与联合用药禁忌: 使用该药物可能引发的不良反应主要包括:恶心、
3. 其他重要警告与注意事项: 处方医生在临床应用中还需警惕
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)