糖尿病可增加

近年来,降糖药物在预防AD方面的潜力日益受到关注。既往研究表明,


在T2DM-AD通路共病网络的疗效比较分析中,二甲双胍的药物影响评分最高,
在该网络中,药物-通路相互作用表明,二甲双胍的获益主要是通过AMPK、
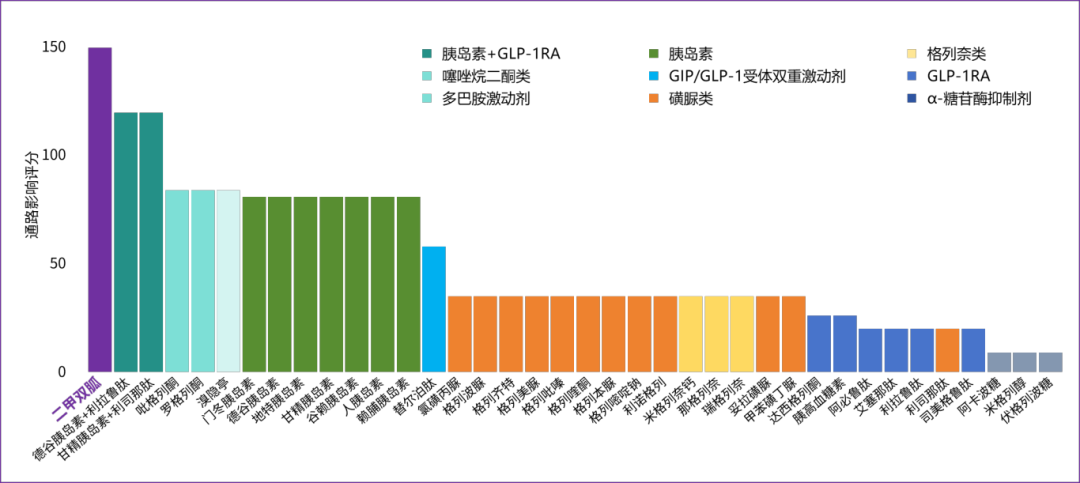
图1. 基于影响评分的T2DM治疗药物在调节AD通路方面的疗效比较
一阶邻域通路分析进一步凸显出二甲双胍直接靶向的胰岛素信号通路与AD通路存在相互作用,表明了二甲双胍的代谢效应与神经退行性机制的直接分子联系。此外,二甲双胍主要靶向通路的一阶邻域通路均与AD和T2DM相关,包括MAPK信号通路、PI3K-Akt信号通路、细胞凋亡通路及寿命调节通路等(图2)。它们对细胞存活、炎症反应和代谢调节至关重要,进一步支持二甲双胍预防AD的获益。此外还有
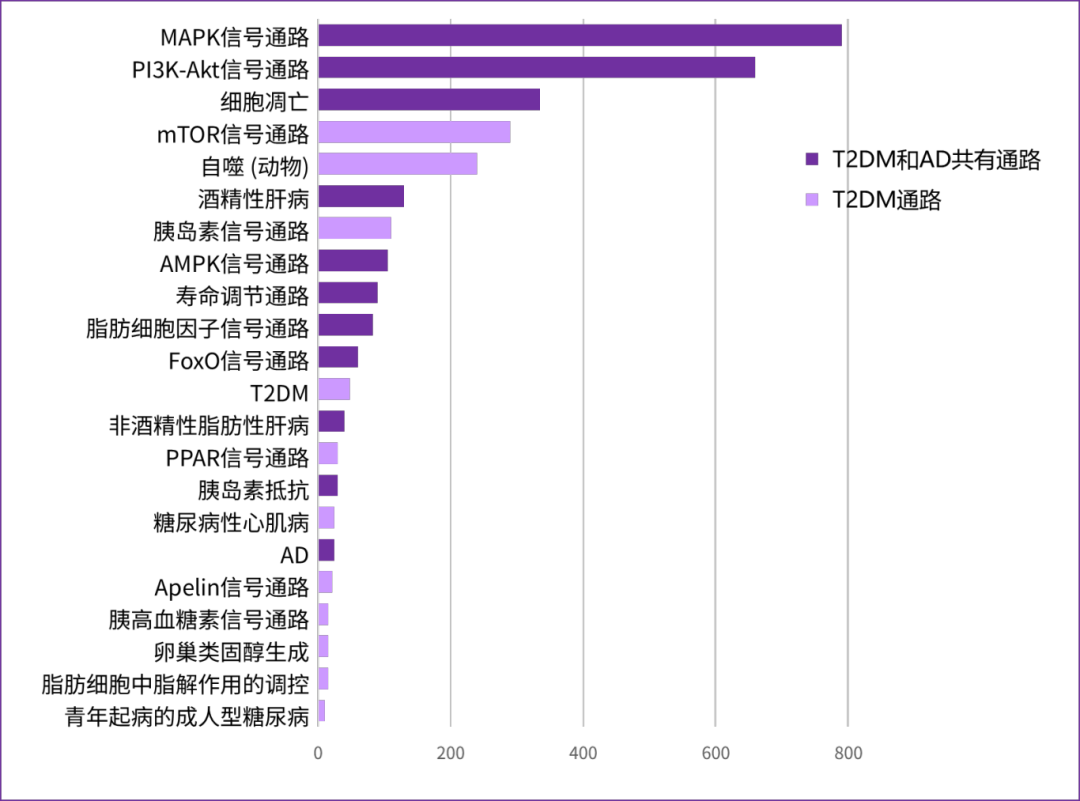
图2. 二甲双胍主要靶向通路在T2DM-AD共病网络中的一阶邻域通路综合影响评分
孟德尔随机化(MR)分析结果不支持二甲双胍和司美格鲁肽与AD风险存在显著的遗传因果关系(表1),提示这些药物的潜在作用可能是通过非遗传机制(如表观遗传、代谢调节等)介导。此外,敏感性分析未发现多效性证据(MR–Egger截距p>0.05;MR–PRESSO全局测试p>0.05),排除了单核苷酸多态性(SNP)对该因果关系的影响。
表1. 基因指示的二甲双胍、司美格鲁肽靶点与AD风险之间的关联

注:采用IVW MR及敏感性分析评估基因指示的二甲双胍、司美格鲁肽靶点与AD风险之间的关联。效应估计值采用OR及其95%CI。采用双侧IVW、加权中位数检验和MR-Egger回归检验评估统计学显著性,采用MR-PRESSO检验和Cochran‘s Q统计量评估水平多效性和异质性。
SNPs的F统计量>10,表明其作为遗传工具模拟二甲双胍、司美格鲁肽的工具变量具有较强效力。 IVW: 逆方差加权法; OR: 比值比
该研究为韩国一项横断面研究,分析来自KBASE研究(韩国阿尔茨海默病早期诊断与预测的脑老化研究)的不伴有痴呆的老年(55-90岁)T2DM患者76例(使用二甲双胍n=55,未使用二甲双胍n=21)。所有患者均接受全面的临床与神经心理学评估及多模态神经影像学检查,包括整体β-淀粉样蛋白(Aβ)沉积([11C]PiB-PET)、颞下颞叶tau蛋白沉积([18F]AV-1451 PET)、AD相关特征性皮质厚度(AD-CT)和白质高信号(WMH)体积。采用阿尔茨海默病注册研究联盟(CERAD)神经心理学量表评估患者的整体认知功能。
AD-CT变薄和相关特异性蛋白聚集是AD的核心病理特征之一,后者主要涉及Aβ和tau蛋白8,9。该研究通过探索性广义线性模型(GLM)分析显示,二甲双胍与更高的AD-CT值显著相关(p<0.05),与Aβ、tau蛋白或WMH体积无关(表2)。
表2. 二甲双胍与AD相关神经影像学生物标志物的关系

注:采用一般线性模型评估,协变量包括年龄、性别、APOE4状态、认知状态、血管风险评分(VRS)、HbA1c和是否使用其他降糖药物。SE: 标准误差
载脂蛋白E4(APOE4)是AD的主要遗传危险因素,而既往有研究表明APOE4的存在可能影响二甲双胍的神经保护作用7,9。因此,该研究以AD-CT为因变量进行GLM分析,结果表明,APOE4状态与二甲双胍的使用存在显著交互作用(表3)。
随后的亚组分析显示,在APOE4阴性个体中,二甲双胍的使用与较高的AD-CT显著相关(β=0.437,p<0.001),在APOE4阳性个体中则无此关联(表4, 图3A、B)。进一步探索性分析发现,在APOE4阴性个体中,二甲双胍的使用与整体认知功能显著相关(β=0.170,p=0.038),而在APOE4阳性个体中则无此关联(图3C、D)。
针对其他混杂因素的分析显示,年龄、性别、认知状态、
表3. APOE4状态对二甲双胍与 AD-CT之间关联的调节效应

注:采用一般线性模型评估,以AD-CT为因变量,以二甲双胍的使用×APOE4状态为交互项,以二甲双胍的使用和APOE4状态的主效应为自变量,协变量包括年龄、性别、认知状态、VRS、HbA1c和是否使用其他降糖药物。
表4. 二甲双胍与AD-CT关联的分析(基于APOE4状态分层)

注:采用一般线性模型评估,协变量包括年龄、性别、认知状态、VRS、HbA1c和是否使用其他降糖药物。*采用Bonferroni校正法校正多重比较,显著性阈值为p<0.025(i.e. 0.05/亚组分析次数=2)。
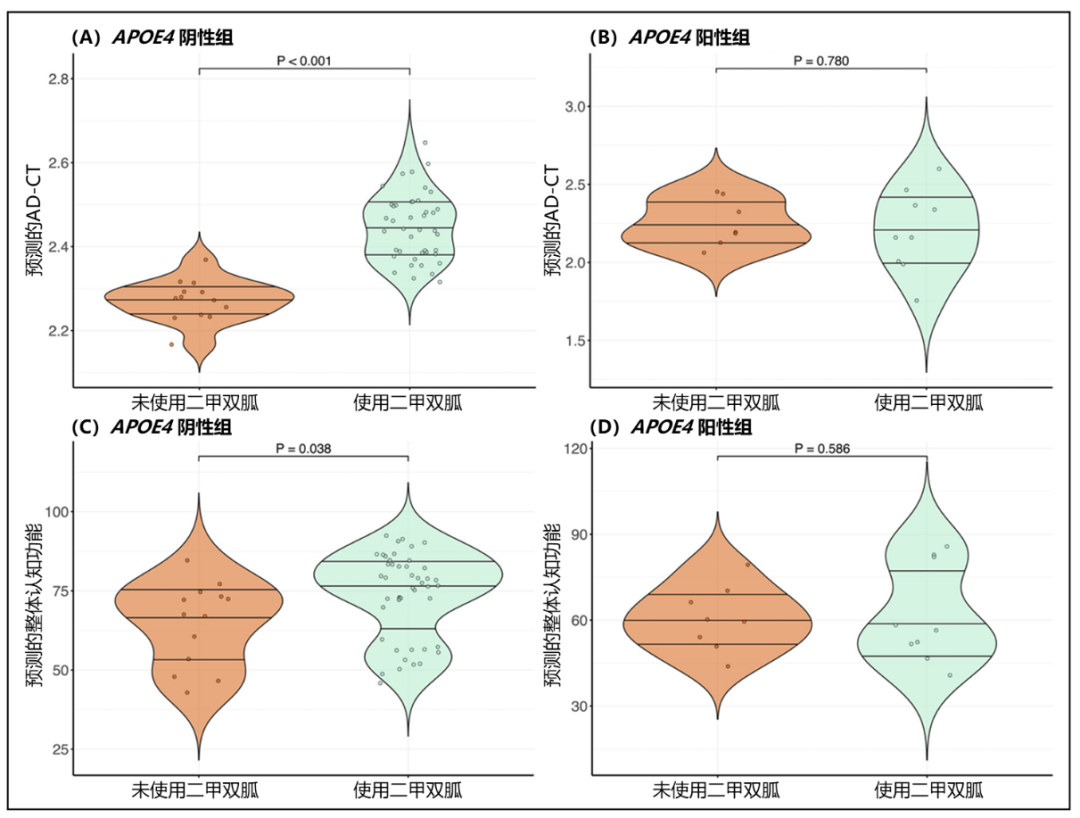
图3. 二甲双胍的使用与AD-CT和整体认知功能的关联(基于APOE4状态分层)


苏青 教授
上海交通大学医学院附属新华医院
两项研究从不同维度探讨了二甲双胍与T2DM相关AD的关系,网络药理学整合模型分析为临床探索提供理论支撑,韩国横断面研究从影像学层面进一步为二甲双胍的神经保护作用提供新证据。
网络药理学整合模型分析通过系统性的共病网络评估,发现二甲双胍在T2DM相关AD中的药物影响评分最高,提示二甲双胍较其他降糖药物在预防或降低T2DM相关AD风险方面具有优势。该分析还印证了司美格鲁肽3期临床EVOKE研究的结果:与安慰剂组相比司美格鲁肽组(应用104周)临床痴呆评定量表总分无统计学差异,对患者的认知功能及日常生活能力均未产生影响10。此外,在该研究的邻域通路分析中,二甲双胍的药物作用通路与T2DM、AD密切相关,除了直接靶向的胰岛素信号通路,还广泛覆盖与细胞存活、炎症反应和代谢调节相关的细胞凋亡通路、寿命调节通路和PI3K-Akt通路等,揭示了二甲双胍与神经退行性机制的潜在分子联系。MR分析则排除了显著的遗传因果关系,进一步提示二甲双胍的获益可能源于其对代谢微环境、表观遗传修饰或线粒体功能的动态调节。
韩国横断面研究则聚焦于研究对象的脑皮质改变,精准分析了二甲双胍与AD病理的关系。该横断面研究发现,二甲双胍在老年T2DM患者中与AD-CT值更高相关,但与Aβ、tau蛋白病理减少无关,表明二甲双胍的保护作用可能独立于特异性蛋白聚集机制;此外,不管是否使用二甲双胍,WMH体积未见差异,提示血管机制可能并非主要介导途径。进一步探索分析发现,二甲双胍仅在APOE4非携带者中与整体认知功能显著相关,为后续的深入研究和精准化医疗提供了坚实的基础。
以上研究结果凸显出二甲双胍在预防或治疗T2DM相关AD的潜力,其神经保护作用可能与增加皮质厚度有关,为未来进一步深入探索其作用机制及临床疗效提供了有力的循证医学支撑。
注意:二甲双胍在中国未获批用于阿尔茨海默病,本文仅供医疗卫生专业人士学术交流。
CN-MET-00149有效期至2028年03月26日
苏青 教授
医学博士,主任医师,博士生导师
上海交通大学医学院附属新华医院内分泌科主任
中华医学会糖尿病学分会常委
上海市医学会理事
上海市医学会糖尿病专科分会候任主任委员
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)