长期以来,
2026年2月9日,德国糖尿病研究中心(DZD)研究团队发表于《自然-通讯》(Nature Communications)期刊的一项研究利用可解释人工智能(XAI,Explainable AI)技术,通过对活体捐献者胰腺组织的高分辨率扫描分析,成功识别出与
AI揭示的病理图景显示:2型糖尿病并非单一细胞类型的病变,而是胰腺微器官水平上的整体演变,涉及胰岛萎缩、脂肪组织浸润、神经纤维重构以及间质纤维化等多维度的病理过程。
这一突破不仅为T2D的早期生物病理学研究开辟了新路径,也为未来精准医疗下的生物标志物开发奠定了数据基础。

在与2型糖尿病的长期斗争中,医疗界深知胰腺组织在疾病进展过程中会发生微观演变。然而,这些变化往往如丝如缕,极其细微,即便是经验最为丰富的病理学家通过常规组织组织病理学检查也难以实现稳定、可靠的识别。
获取高质量的研究样本更是难上加难。由于胰腺位于腹膜后深处,活检或手术切除风险巨大,导致过往研究大多依赖于尸检样本。然而,尸检组织不可避免地存在死后变化,这往往会掩盖或扭曲疾病早期的真实生物学信号。为了突破这一瓶颈,德国糖尿病研究中心(DZD)的研究团队汇集了目前最大规模的活体捐献者胰腺组织数据集,力求在最接近生理状态的组织中寻找疾病的真凶。
研究团队采用了跨学科的前沿手段,将传统的组织染色技术(显色染色及多重免疫荧光)与十亿像素级显微成像(Gigapixel Microscopy)相结合,对每一份组织切片进行了精细的数据化处理。
在此基础上,研究者训练了深度学习模型,旨在精确区分糖尿病与非糖尿病样本。尽管人工智能在分类任务中表现卓越,但该研究最核心的贡献在于引入了“可解释人工智能”(Explainable AI, XAI)。
不同于以往只给结论、不给理由的“黑盒”算法,XAI能够向研究者清晰地展示其判断依据。它不仅能精准预测疾病状态,更重要的是,它揭示了模型在观察哪些特定的组织特征。这种从“知其然”到“知其所以然”的转变,让AI真正成为了增强病理医生感知能力的利器,而不仅仅是简单的替代工具。
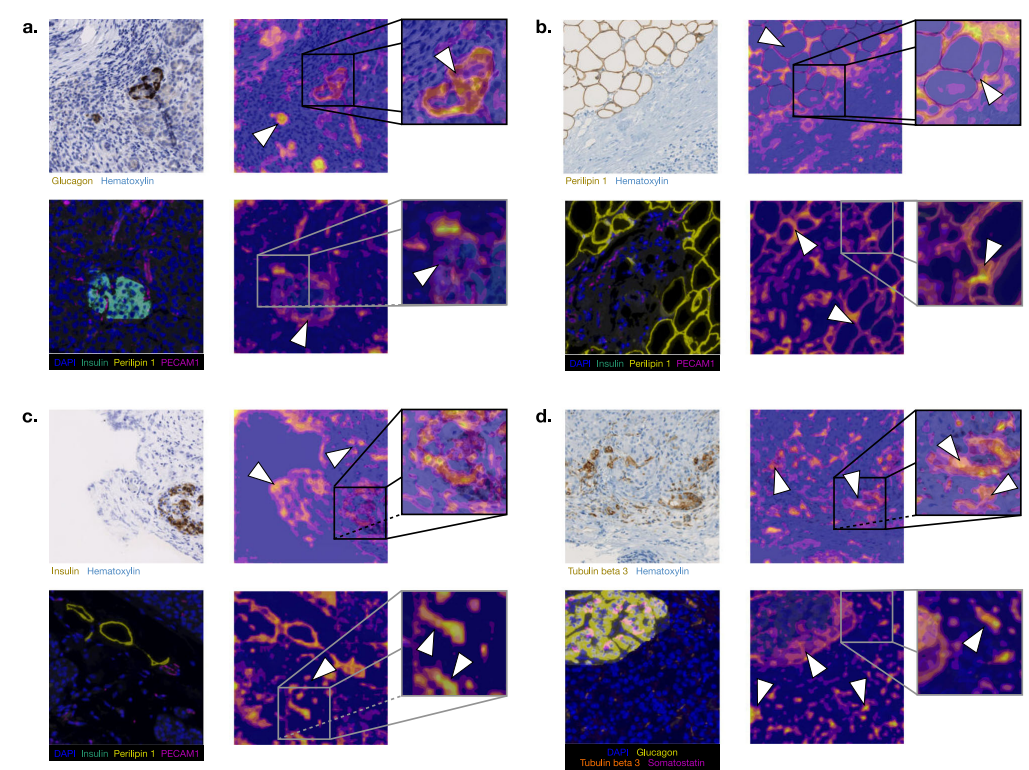
图 微观病理的像素级热图(Pixel-level heatmaps)
a:展示了 AI 对胰岛的高度关注;
b:展示了 AI 识别的脂肪细胞簇特征;
c:对应结缔组织/纤维化区域的视觉特征;
d:对应神经轴突结构(Tubulin beta 3 染色),这是 AI 区分糖尿病状态的关键信号。
通过XAI的辅助,研究团队成功锁定了一系列与2型糖尿病密切相关的组织学特征。这些发现如同一块块拼图,逐渐还原出疾病在微观世界的真实面貌:
• 胰岛体积缩小: T2D患者的胰岛平均面积显著小于非糖尿病患者。研究指出,这可能是因为较大的胰岛在疾病过程中被优先破坏或损失。
• 细胞组成的变化: AI模型发现,除了β细胞,α细胞和δ细胞的改变对预测疾病状态同样至关重要。虽然具体的细胞质量变化比例仍有讨论,但胰岛内部这些细胞的组织结构和空间关系发生了改变。
• 神经支配异常: XAI识别出神经轴突(由tubulin beta 3染色)的改变是T2D最显著的特征之一。在T2D患者中,神经纤维的密度或形态发生重构,尤其是胰岛内部的神经分布。
• 血管构象变化: 胰岛内的血管支配(通过PECAM1标识)表现出异常,暗示了血管细胞架构(cytoarchitecture)的改变对胰腺功能受损有贡献。
• 脂肪细胞簇增大:T2D患者胰腺内的脂肪细胞倾向于形成更大的簇,而非零散分布。脂肪细胞簇的面积与疾病病程呈正相关。
• 胰岛与脂肪的“近距离接触”:这是一个关键的发现。在T2D患者中,胰岛与脂肪细胞之间的距离显著缩小。这种空间上的邻近性可能通过旁分泌信号(脂肪细胞分泌物)对胰岛微环境产生负面影响,进而损害胰岛素分泌功能。
• 结缔组织富集:模型高度关注组织中的纤维化/结缔组织区域。T2D患者的胰腺组织中表现出更丰富的纤维状结构,且纤维化面积与胰岛素分泌水平(HOMA2B)呈负相关。
• 微环境恶化:这种涵盖了纤维化增加、脂肪浸润以及神经支配改变的综合变化,共同构成了一个不利于β细胞生存和发挥功能的“受损微环境”。
• 原子核与全局改变: 借助多重免疫荧光技术,AI发现核染(DAPI)信号在预测中也具有极高权重,这表明T2D伴随着胰岛内全局形态学(如细胞密度或核形态)的广泛改变。
总结而言,AI揭示的病理图景显示:2型糖尿病并非单一细胞类型的病变,而是胰腺微器官水平上的整体演变,涉及胰岛萎缩、脂肪组织浸润、神经纤维重构以及间质纤维化等多维度的病理过程。
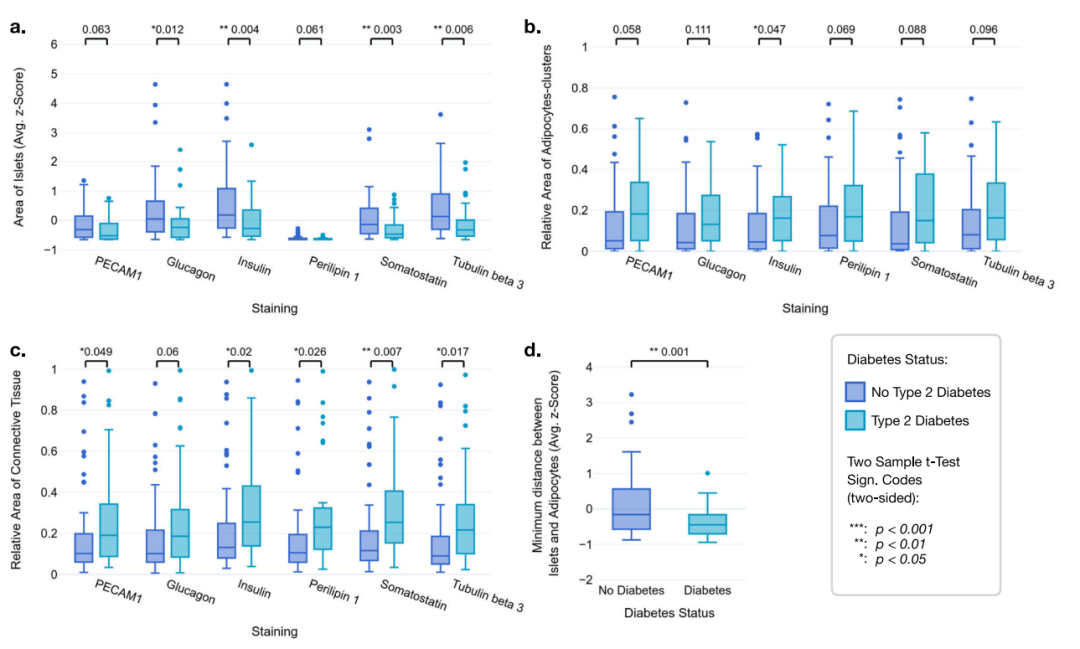
图 胰腺组织随疾病进展发生形态变化
• 胰岛萎缩:a 通过条形图展示了 T2D 患者在多种染色下(如 Insulin, Glucagon)胰岛面积(Area of Islets)均显著减小。
• 脂肪细胞簇增大:b 显示 T2D 患者胰腺内脂肪细胞簇的相对面积(Relative Area of Adipocytes-clusters)呈现增加趋势。
• 间质纤维化增加:c 量化了结缔组织(Connective Tissue)面积,证实 T2D 患者该区域明显更丰富。
• 胰岛-脂肪距离缩短:d 直接展示了 T2D 患者胰岛与最近脂肪细胞之间的平均最小距离(Minimum distance)显著降低。
这些定量化的特征被定义为潜在的生物标志物,为临床医生理解β细胞功能障碍提供了前所未有的空间维度视角。
目前,全球约有5亿人正受到2型糖尿病的困扰。在疾病早期精准识别组织水平的病变,对于延缓病程进展、开发针对性疗法具有里程碑意义。
同时本项研究证明,人工智能的价值不仅在于发现人类肉眼“看不见”的东西,更在于能够以逻辑严密的方式解释这些发现,从而深化我们对复杂疾病生物学的认知。这并非要取代传统病理学,而是通过精准度与可解释性的双重赋能,为糖尿病的诊疗开启一扇崭新的视窗。
在未来,这种基于AI的组织特征量化分析,有望成为预测患者病程、评估药物疗效的关键数据基石,让精准医疗在糖尿病领域真正落地生根。
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)