器官移植是器官终末期疾病的重要治疗手段,但移植物损伤是制约移植物存活的主要因素。因此,及时、准确判断移植物是否损伤成为临床热点话题。目前,活检是监测移植物状况的“黄金标准”,然而,活检具有侵入性,可能导致出血等并发症,患者接受度较低,亟需探索侵入性较小的检测方法。而供体来源游离DNA(dd-cfDNA)是一种无创、灵敏度高的新型生物标志物,为非侵入性识别移植患者移植物损伤提供了切实可行的途径。
近期,《dd-cfDNA在实体器官移植急性和慢性排斥反应中的应用》正式发布1,阐述了dd-cfDNA在不同器官移植中的挑战与价值。医脉通特整理该研究主要内容,以期为dd-cfDNA临床应用提供参考。
dd-cfDNA可在血液、尿液或其他体液中被定量检测,器官移植时,dd-cfDNA水平可升高至5%以上(可能是由于器官从供者体内取出及植入受者体内的手术过程造成的创伤),但1周后快速下降至接近零;而发生排斥反应等并发症时,dd-cfDNA水平可升至基线值的5倍,表明dd-cfDNA或可用于亚临床排斥反应的早期检测。
cfDNA检测是指对细胞或组织释放到血液或其他体液中的不同降解DNA片段进行定量分析,检测步骤包括:稳定化采血管中采集血液样本、制备血浆、分离cfDNA(含血浆与cfDNA储存)、cfDNA质量控制、cfDNA分析及报告生成、医生根据报告调整免疫抑制治疗方案等(图1)。
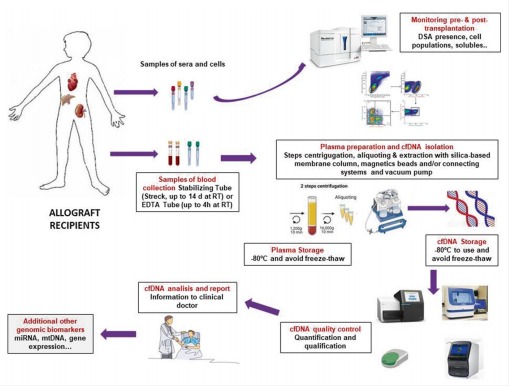
图1.cfDNA检测流程图
肾移植:dd-cfDNA可作为肾移植早期(临床症状出现前数月)监测排斥反应的生物标志物
肾移植患者发生排斥反应的dd-cfDNA阈值为>1%,dd-cfDNA水平与肾活检结果相关性较好,其水平升高与各类肾移植排斥反应(包括亚临床排斥反应)的发生和严重程度相关;且当dd-cfDNA>0.5%时,检测临床和亚临床排斥反应的效果或优于生化标志物。此外,将dd-cfDNA与传统肾移植标志物相结合,可提高排斥反应诊断区分能力。
但由于其他移植后或生物学并发症(如肥胖、自身免疫性疾病复发和感染)可能影响dd-cfDNA水平,导致阴性预测值降低,因此在解读结果时应予以考虑,部分dd-cfDNA检测阳性结果可能为“假阳性”。
肝移植:dd-cfDNA是检测移植物损伤的有力工具
dd-cfDNA与天冬氨酸转氨酶(AST)/丙氨酸转氨酶(ALT)比值相关,且在预测急性排斥反应方面,基于单核苷酸多态性(SNP)和二代测序(NGS)的dd-cfDNA检测优于传统肝功能检查。既往研究显示,基于SNP的dd-cfDNA诊断急性排斥反应的曲线下面积(AUC)为0.975,敏感度达100%,特异度达90.9%,阴性预测值为100%,提示dd-cfDNA低于阈值时,可避免侵入性活检。此外,cfDNA半衰期较短(数分钟-1.5小时),可实时反映移植物损伤情况;而生化肝功能检查半衰期较长,限制了对肝移植物持续变化的监测能力,这进一步表明dd-cfDNA检测在肝移植中的优势。
值得一提的是,疑似慢性排斥反应(伴有炎症和C4d沉积的纤维化)、活动性病毒和细菌感染以及血管和胆道并发症也可能导致dd-cfDNA水平升高,需引起临床关注。
心脏移植:dd-cfDNA的应用,或可减少心内膜心肌活检(EMB)次数
在检测排斥反应方面,dd-cfDNA敏感度和特异度与EMB相当;同时,dd-cfDNA水平与急性排斥反应严重程度相关,且具有较高阴性预测值:排斥反应发生时其水平升高,抗排斥治疗成功后则下降。
然而,心肌缺血、心肌损伤、妊娠以及多器官移植等因素可能导致患者dd-cfDNA水平升高,但未出现排斥反应,需谨慎对待。另外,dd-cfDNA无法鉴别细胞介导排斥反应和抗体介导排斥反应,未来仍需开展更多研究并获得更多验证结果。
肺移植:dd-cfDNA可作为诊断慢性移植肺功能障碍(CLAD)的潜在标志物
与肾移植、肝移植、心脏移植相似,评估肺移植物损伤的dd-cfDNA阈值为0.5%~1%。目前,关于dd-cfDNA水平如何影响CLAD进展的相关研究较少,且尚无法区分闭塞性细支气管炎综合征(BOS)和限制性移植物综合征(RAS)两种CLAD表型。但现有研究显示,CLAD患者的dd-cfDNA水平升高,且与第1秒用力呼气容积(FEV1)下降相关。另外,需要注意的是,样本采集时间、感染等因素均可影响dd-cfDNA水平,且患者个体变异性较大,若要将dd-cfDNA完全确立为CLAD的诊断生物标志物,还需开展更多研究。
目前,dd-cfDNA在器官移植中的重要性日益凸显,这主要归功于其敏感性和特异性,能够早期、可靠地检测潜在的移植物损伤。且该方法操作简便、结果易于解读,无需过度处理样本,仅需单份样本即可完成检测。
当移植物损伤时,dd-cfDNA水平会迅速升高,相较于生化指标,能够更快发现并治疗亚临床排斥反应。这不仅可减少不必要的活检次数,又使得临床医生能及时调整免疫抑制治疗方案,以防疾病进展。
然而,dd-cfDNA检测仍面临技术完善、标准化建设等多重挑战,需通过进一步研究突破局限。展望未来,相信随着检测技术的持续优化和临床证据的不断积累,dd-cfDNA将成为一种安全、经过验证且可靠的工具,最终为改善移植患者预后带来更多可能。
参考文献:
1. Muro-Perez J, et al. Results Probl Cell Differ. 2026;77:151-164.

戳“阅读原文”,查看更多内容
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)