肾单位是肾脏的核心结构与功能单元,主要承担
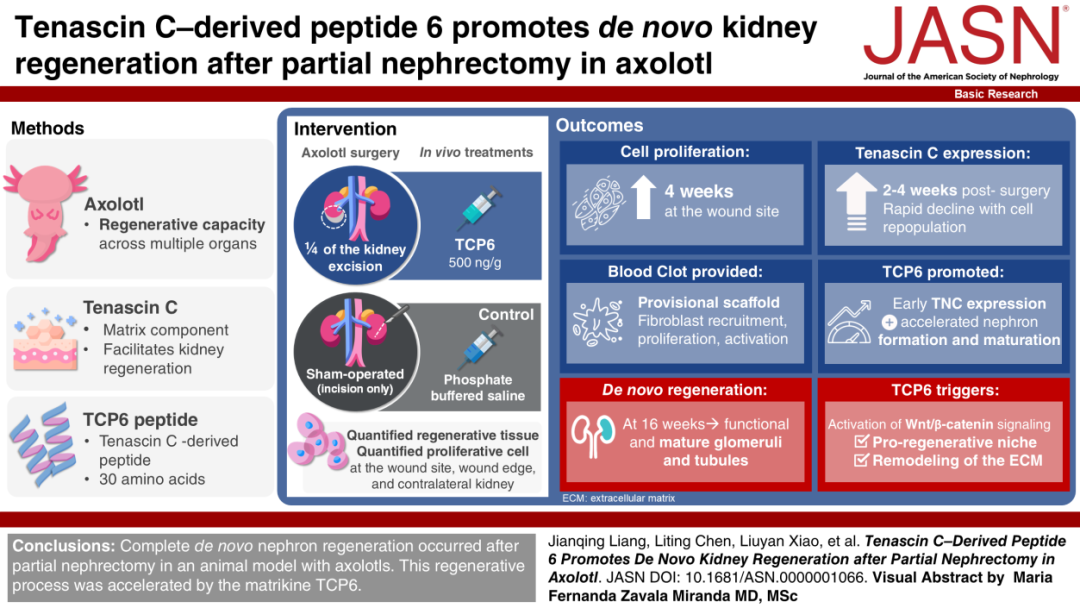
目前学术界普遍认为:成年哺乳动物肾脏遭受损伤后,无法完成肾单位的从头再生,缺失的肾单位难以修复复原,最终造成肾脏病呈进行性进展。该临床治疗瓶颈,充分凸显了肾单位新生再生的科研价值与临床意义,如若能够重建肾单位再生修复能力,或将从根源上革新现有肾脏病治疗体系。
本研究首次系统阐明美西螈部分肾切除术后,肾单位原位新生与完整再生的动态过程。研究结果显示:术后第1周,细胞开始向损伤创面迁移并启动增殖;至术后第4周,损伤侧肾脏细胞数量基本恢复至健侧正常肾脏水平。细胞增殖
刘友华 教授
南方医科大学南方医院肾内科教授、国家基金委肾脏病学创新研究群体负责人
曾任美国匹兹堡大学医学院终身教授、UPMC冠名讲席教授
美洲华人肾脏病学会(CASN)会长
中国病理生理学会肾脏病专业委员会副主任委员
JASN、KI等16个国际学术杂志的编委、副主编
长期从事肾脏纤维化病理机制的基础性研究,共发表SCI论文250余篇。论文被引33,600余次,h-指数102
研究方法
美西螈具备极强的组织再生能力,可完成肢体、心脏、部分脑组织及胰腺等复杂器官的修复再生,是再生生物学研究的经典模型。本研究采用美西螈作为模型,通过单侧四分之一部分肾切除术,进行肾脏质量消融。实验动物为约3个月大的幼年美西螈,鼻尾长5至7厘米。在手术中,动物被麻醉并随机分组,对照组为假手术动物(仅切口,无肾切除)。为了评估再生过程,在术后多个时间点(0、1、2、4、8、12和16周)收集肾脏组织进行评估。主要终点包括新生肾单位的形成、细胞增殖和组织恢复情况,次要终点包括TNC的表达动态、细胞外基质重塑以及再生肾小管的功能成熟。
核心结果
肾切除术后第1周起,细胞开始迁移至伤口部位并增殖,至第4周时,损伤侧肾脏的细胞数量已几乎恢复至对侧健康肾脏的水平。以未行肾切除术为基线,此时肾脏细胞的增殖率为2% ± 0.8%,细胞增殖在术后第2至4周达峰,增殖率在术后2
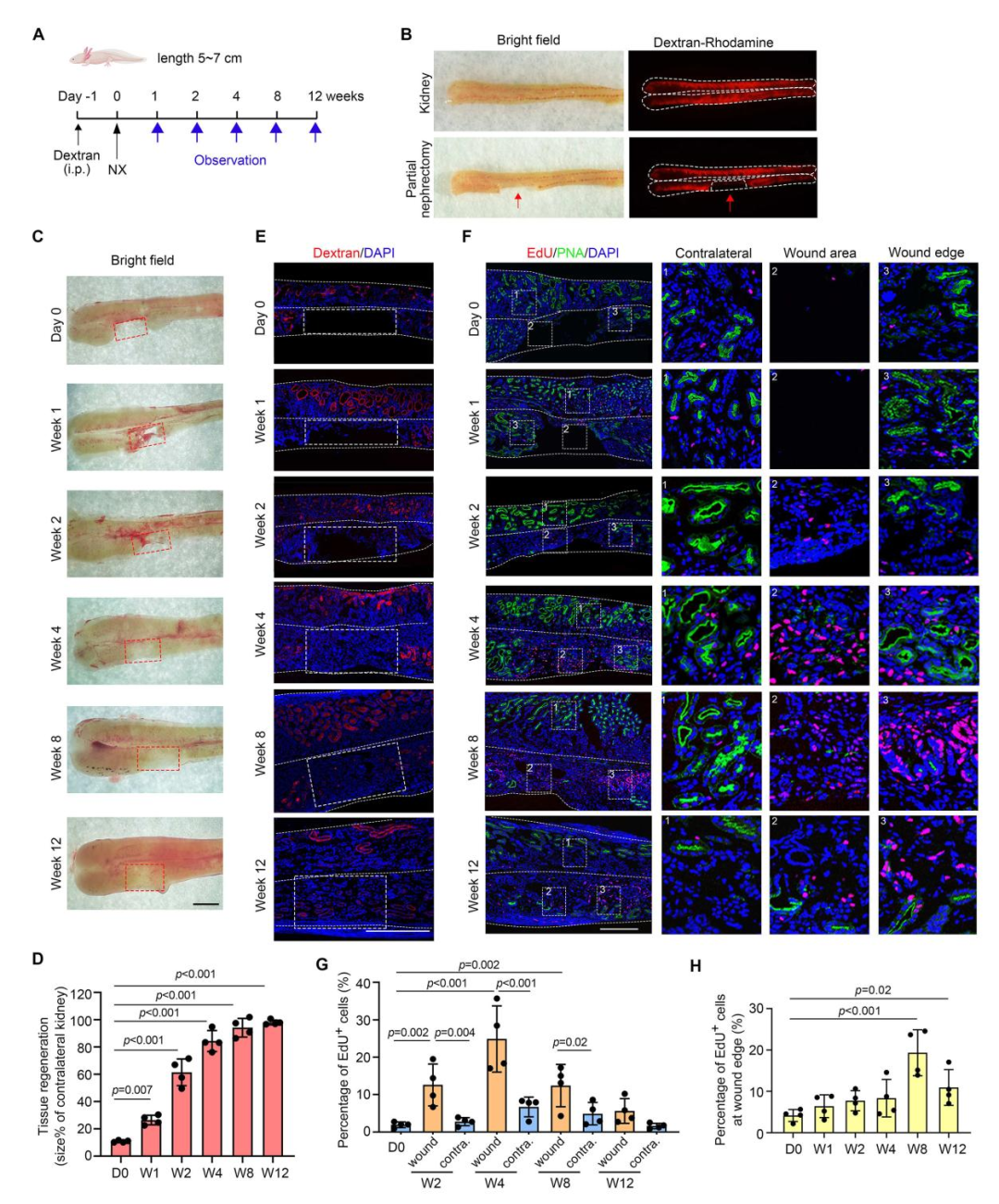
图1. 美西螈肾切除术后的细胞增殖与肾组织修复
(A)实验设计示意图,展示美西螈部分肾切除术后的实验方案及标本取材时间线。于术前1 天腹腔注射罗丹明 - 葡聚糖。NX:部分肾切除术;i.p.:腹腔注射。(B) 肾切除术前、术后代表性成像图。罗丹明 - 葡聚糖标记原有肾小管,手术切口部位无荧光信号(红色箭头标示)。(C) 不同时间节点肾脏切除术后再生过程的代表性时序图像。红色虚线框标示手术切口区域;比例尺:1 mm。(D) 再生组织面积定量分析,以同侧再生组织相对对侧健康肾脏的占比表示。误差棒:均值 ± 标准差(n=4);采用单因素方差分析计算P值,各组分别与第 0 天(D0)组进行比较。(E) DAPI 细胞核染色显示损伤区域的细胞补充情况;罗丹明 - 葡聚糖示踪原有肾小管;比例尺:1 mm。(F) 不同时间节点再生组织 EdU 染色代表性图像。内嵌图(白色虚线框)为对侧肾脏、损伤中心及损伤边缘区域的放大视野。FITC-PNA 标记近端肾小管,DAPI 标记细胞核;比例尺:500 μm。(G) 各指定区域内 EdU 阳性细胞 / 总细胞核占比的定量统计。误差棒:均值 ± 标准差(n=4);采用单因素方差分析计算P值。(H) 损伤边缘区域内 EdU 阳性细胞 / 总细胞核占比的定量统计。误差棒:均值 ± 标准差(n=4);采用单因素方差分析计算P值,各组分别与第 0 天(D0)组进行比较。D:天数;W:周数。
肾切除术后约8周,再生组织中可观察到未成熟肾小管结构;至术后第12周,肾小管结构逐步成熟完善;到术后第16周,再生肾组织已形成结构完整的肾小管及可清晰识别的肾小球。为评估肾小球滤过功能及肾小管重吸收功能,于组织采集前1日注射FITC-右旋糖酐。结果显示,部分肾切除术后第16周,70%的样本中新生肾小管出现右旋糖酐重吸收现象,证实肾小球滤过与肾小管重吸收功能已成功恢复。对近端肾小管及肾小球标志物进行免疫荧光染色,结果显示,新生的完整肾小管及肾小球单位在结构构型上与对侧健康肾脏高度一致;新生肾组织切片与对侧肾脏切片中的肾小球密度无明显差异。此外,部分肾切除术后第16周,亦可清晰检测到远端肾小管(calbindin阳性)及髓袢厚升支(NKCC2阳性)(图2)。上述结果共同证实,部分肾切除术后第16周,肾单位实现了全新且完整的结构与功能重建,新生肾小管及肾小球可再现天然肾脏组织关键的生理功能与结构特征。
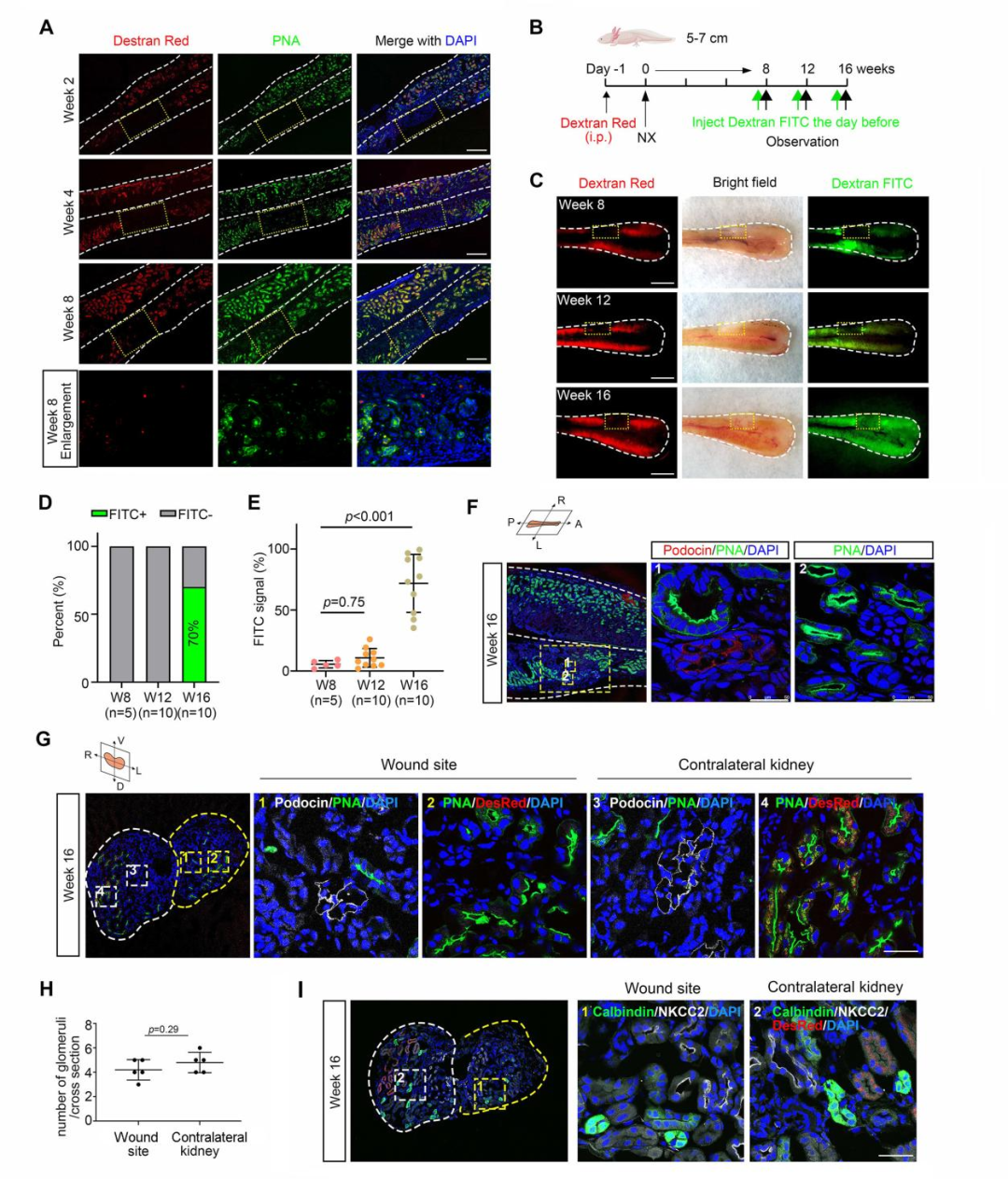
图2. 肾切除术后肾单位的从头再生
(A)FITC-PNA标记肾小管的荧光图像显示,部分肾切除术后第8周起,伤口区域开始出现肾小管结构。罗丹明-葡聚糖标记原有肾组织。DAPI染细胞核。黄色虚线框:伤口区域。(B)美西螈部分肾切除术后实验设计及功能评估时间线示意图。罗丹明-葡聚糖于术前注射;FITC-葡聚糖于观察前注射。NX:部分肾切除术;i.p.:腹腔注射。(C)肾切除术后不同时间点美西螈肾脏的代表性明场、罗丹明及FITC图像。罗丹明-葡聚糖和FITC-葡聚糖的注射方案见(B)。白色虚线:美西螈肾脏轮廓;黄色虚线框:含再生组织的伤口区域。(D)部分肾切除术后第8周(n=5)、第12周(n=10)及第16周(n=10)显示功能性肾小管再生(FITC阳性)的样本百分比。(E)再生肾脏中FITC阳性区域的定量分析,数据以同一动物对侧对照肾脏为基准进行标准化。数据来源于(D)中所示同一批动物。(F)纵向组织切片的podocin与PNA免疫荧光显示,部分肾切除术后第16周再生组织中可见新生肾小球及肾小管。细胞核以DAPI染色显示。比例尺:50 μm。(G)组织横切片的podocin与PNA免疫荧光显示,部分肾切除术后第16周再生组织中存在新生肾小球及肾小管。DesRed信号(罗丹明-葡聚糖)标示原有肾组织。DAPI染色标示细胞核。黄色虚线:再生组织;白色虚线:对侧未损伤组织。(H)横切面肾小球数量定量分析显示,再生侧与对侧之间无显著差异(n=5只动物)。(I)部分肾切除术后第16周再生组织中calbindin与NKCC2的免疫荧光染色。黄色虚线:再生组织;白色虚线:对侧未损伤组织。
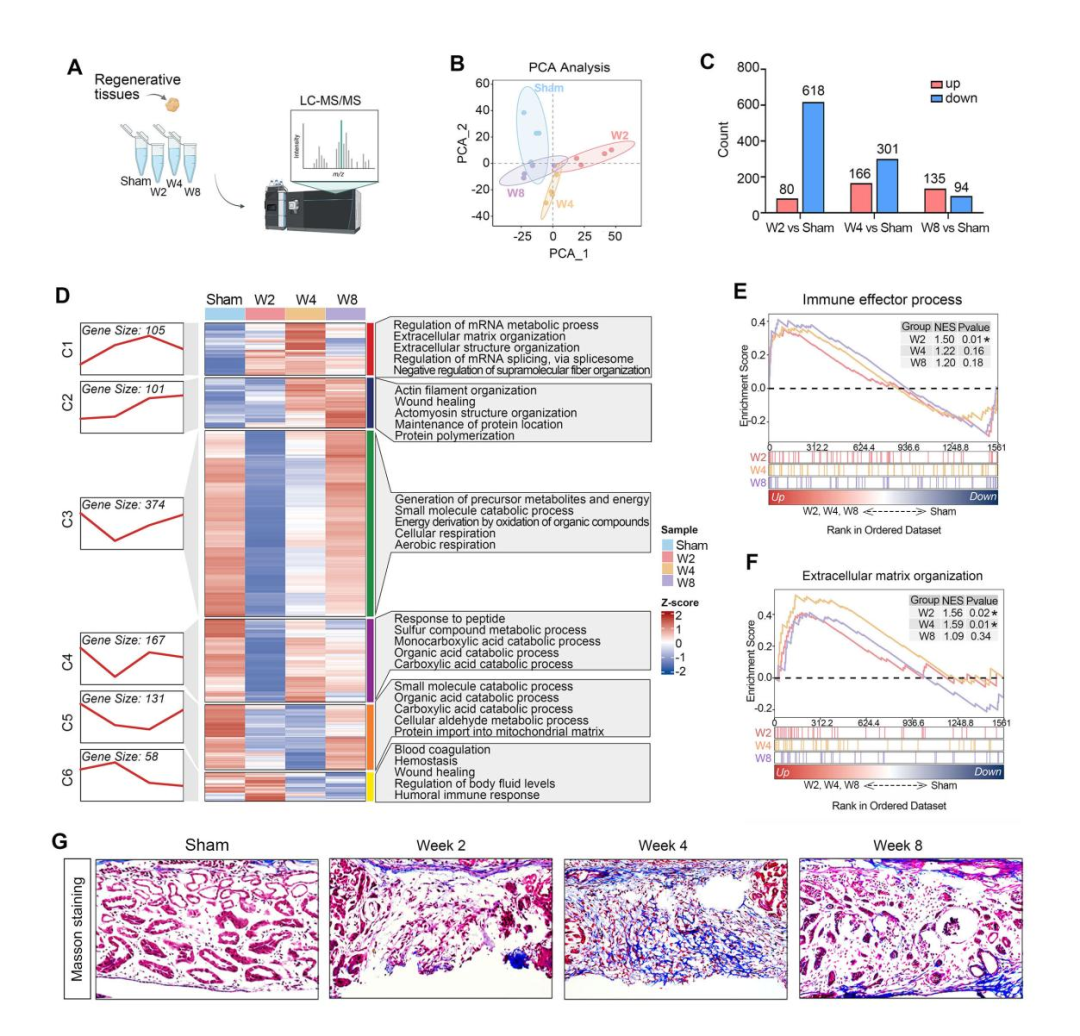
图3. 腱糖蛋白-C是肾单位再生的关键调控分子
(A)差异表达蛋白的火山图。红色:表达上调;蓝色:表达下调;灰色:无变化。腱糖蛋白-C已高亮标注。W:部分肾切除术后周数;Tnc:腱糖蛋白-C。(B)箱线图显示不同再生阶段腱糖蛋白-C蛋白水平的Log2转换值(n=4个生物学重复)。(C)部分肾切除术后再生过程中不同时间点美西螈肾脏的腱糖蛋白-C免疫荧光染色。DAPI染色标示细胞核。TNC:腱糖蛋白-C;Sham:未损伤对照组。(D)再生组织中腱糖蛋白-C表达面积的定量分析,与(C)图相对应。n=4只动物。(E)示意图展示美西螈中siRNA介导的腱糖蛋白-C敲低实验设计。siRNA于所示时间点经尾静脉注射;对照组接受等体积PBS注射。肾切除术后第28天(第4周)收集组织。(F)肾切除术后第4周,对照组与siTNC处理组肾脏的代表性明场图像。红色虚线:再生组织。比例尺:500 μm。(G)再生组织大小的定量分析,以对侧肾脏大小的百分比表示。均值±标准差,n=6只动物。p值由t检验确定。(H)肾切除术后第4周,对照组与siTNC处理组美西螈肾脏的腱糖蛋白-C免疫荧光染色。DAPI染色标示细胞核。比例尺:500 μm。(I)EdU染色显示肾切除术后第4周伤口区域的增殖细胞。DAPI染细胞核。比例尺:500 μm。(J、K)肾切除术后第4周,对照组与siTNC处理组美西螈肾脏中α-SMA和SOX9的免疫荧光染色。DAPI染色标示细胞核。比例尺:500 μm。(L)部分肾切除术后第4周,对照组与siTNC处理组美西螈肾脏的马松三色染色。NX:肾切除术;Ctrl:对照组;siTNC:腱糖蛋白-C特异性siRNA。
为评估TCP6对肾单位再生的最终效应,本研究检测了新形成肾小管的功能恢复时程,并通过FITC-葡聚糖重吸收实验进行功能验证。在组织收集前24小时经腹腔注射给予FITC-葡聚糖,以监测肾小管重吸收能力。结果显示,在TCP6治疗组中,再生肾小管在部分肾切除术后12周即表现出功能活性,比溶剂对照组提前4周;对照组直至术后16周才显示出功能成熟。与上述功能发现一致,免疫荧光染色显示TCP6促进了新肾单位的高级结构组织化,表现为结构清晰的肾小管构架及表达经典标志物足细胞蛋白的肾小球结构。通过RNA-FISH在这些肾小球中也检测到MAFB mRNA的表达。相比之下,部分肾切除术后12周的溶剂对照组再生肾脏中则观察到未成熟的肾小管结构,且缺乏肾小球标志物染色。以上结果表明,TCP6不仅加速肾单位再生,还促进再生肾单位的正确组装与功能整合(图4)。综上所述,这些结果提示TCP6具有作为加速肾损伤后肾单位再生的有效制剂的潜力。
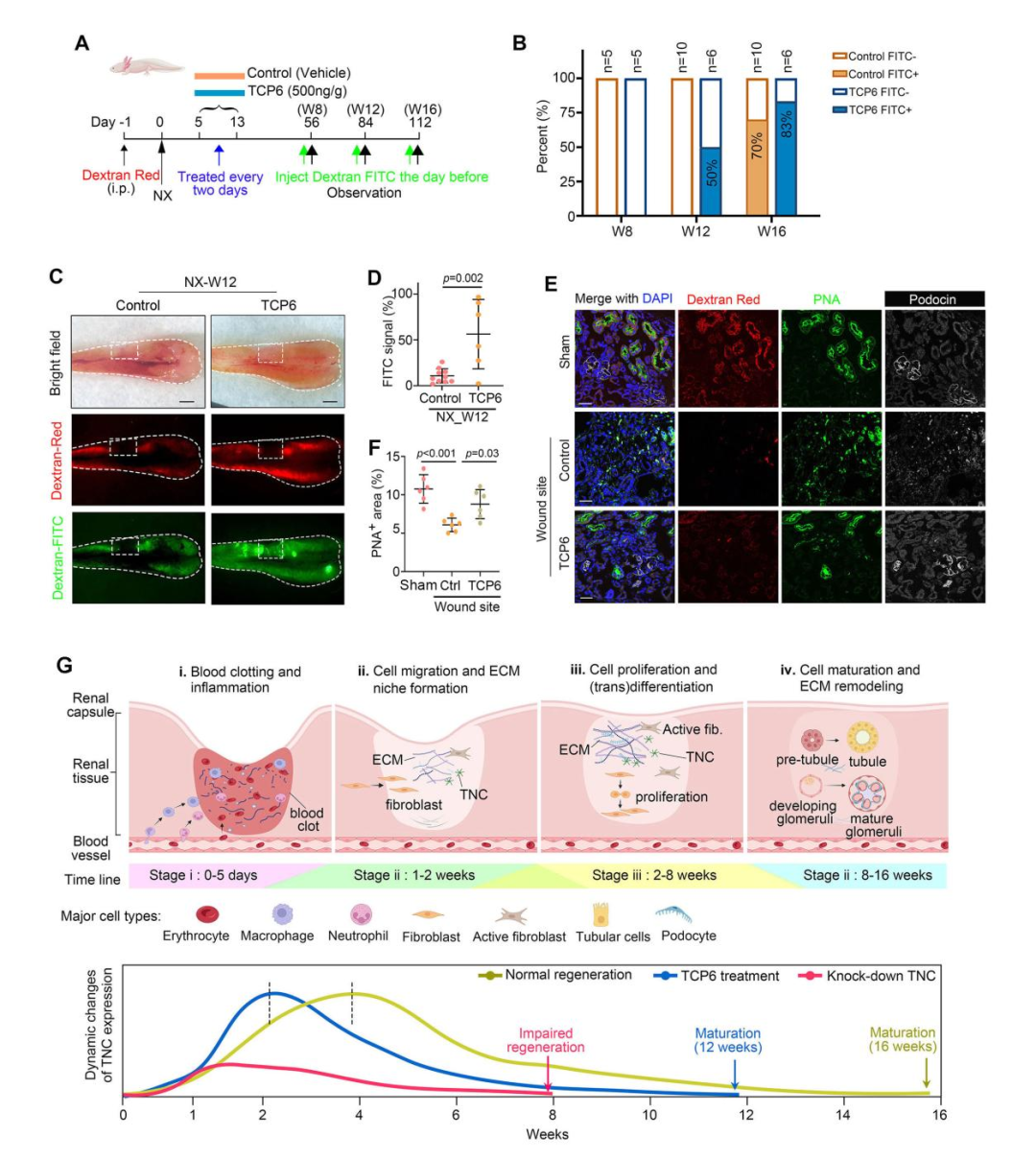
图4. TCP6加速肾脏再生及功能恢复
(A)示意图展示评估TCP6对美西钝口螈部分肾切除术后肾小管功能恢复治疗效果的实验设计。红色-葡聚糖于术前一天注射以标记原有肾小管。FITC-葡聚糖于观察前一天在所示时间点注射。(B)肾切除术后所示时间点,对照组与TCP6治疗组之间显示功能性肾小管再生(FITC阳性)样本百分比的统计分析。(C)肾切除术后第12周,对照组与TCP6治疗组美西钝口螈肾脏的代表性明场、罗丹明荧光及FITC荧光图像。白色虚线框标示含再生组织的伤口部位。比例尺:500 μm。(D)再生肾组织中FITC阳性区域相对于对侧对照肾脏的定量分析,数据来源于(C)所示相同样本。(E)肾切除术后第12周,溶剂对照组与TCP6治疗组美西钝口螈再生组织中podocin与PNA的免疫荧光染色。假手术肾脏作为正常未损伤对照。罗丹明-葡聚糖的红色荧光信号标示原有肾组织,DAPI染色标示细胞核。比例尺:100 μm。(F)第12周时假手术组与再生肾组织(溶剂对照组和TCP6治疗组)中PNA阳性区域的定量分析,数据来源于(E)所示相同样本。Ctrl:溶剂对照组。(G)部分肾切除术后肾脏再生不同阶段的示意图。TNC:腱糖蛋白-C;ECM:细胞外基质。
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。仅供HCP观看。
