导读
2026年2月9日,中国科学院深圳先进技术研究院童丽萍、陈棣、John R. Speakman、暨南大学张还添教授共同通讯在Cell Metabolism (IF=30.9)发表题为“Semaglutide ameliorates osteoarthritis progression through a weight loss-independent metabolic restoration mechanism”的研究论文。该研究揭示GLP-1受体激动剂
研究设计
研究采用高脂饮食诱导的肥胖小鼠模型,通过内侧半月板失稳(DMM)手术构建OA,并设立配对喂养(PF)对照组,以严格控制食物摄入量,使PF组与SG治疗组体重变化保持一致,从而排除减重本身对实验结果的干扰。随后,综合运用组织学、免疫组化、Micro-CT、行为学测试、蛋白质组学及Seahorse能量代谢分析等手段,系统评估SG的治疗效果。为进一步验证关键信号通路,研究还构建了全身性GLP-1R基因敲除(Glp-1r KO)小鼠和软骨特异性AMPKα1(Prkaa1)条件性敲除(cKO)小鼠。此外,为验证临床转化潜力,开展了为期24周的随机对照初步临床试验,评估SG联合
研究结果
研究表明,在肥胖合并DMM诱导的OA小鼠模型中,SG治疗显著改善关节软骨退行性变。表现为OARSI评分、滑膜炎评分及骨赘形成显著降低,同时软骨面积明显增加(图1D–J)。免疫组化分析显示,SG有效下调分解代谢标志物MMP13与ADAMTS5的表达,并恢复合成代谢标志物Aggrecan和COL-2的水平(图1K–O)。进一步研究发现,尽管配对喂养(PF)组小鼠的体重下降幅度与SG组相当,却未观察到类似的软骨保护效应,提示SG的治疗作用独立于体重减轻。

图1:SG抑制肥胖/骨关节炎小鼠的软骨降解
行为学测试结果显示,SG治疗显著改善肥胖合并DMM小鼠的机械痛阈和热痛敏(图2A–B),并提升其自发活动能力。免疫荧光染色揭示,SG处理可降低关节腔、背根神经节及脊髓中疼痛相关神经标志物(包括CGRP、PGP9.5、NGF和c-Fos)的表达水平(图2C–L),为其镇痛效应提供了多层面证据。
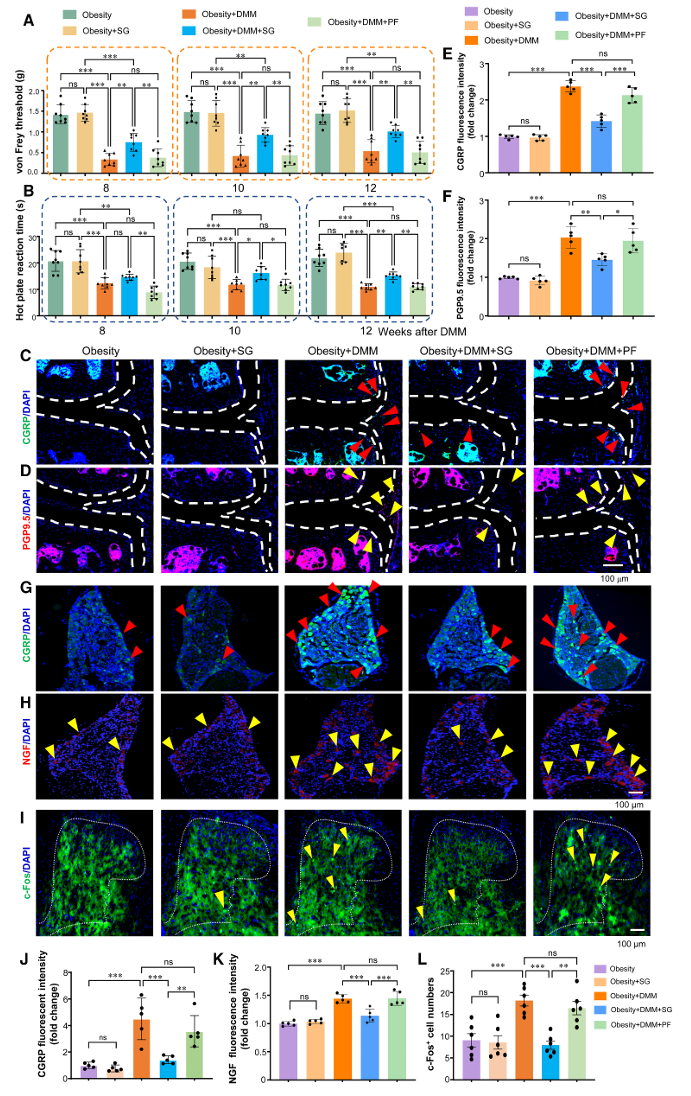
图2:SG抑制肥胖/骨关节炎小鼠的疼痛
蛋白质组学分析显示,SG处理后,软骨组织中糖酵解关键酶PFKFB2表达上调4.3倍(图3A)。KEGG和GSEA分析提示,SG主要影响代谢通路,尤其是脂肪酸代谢和糖酵解(图3C–E)。
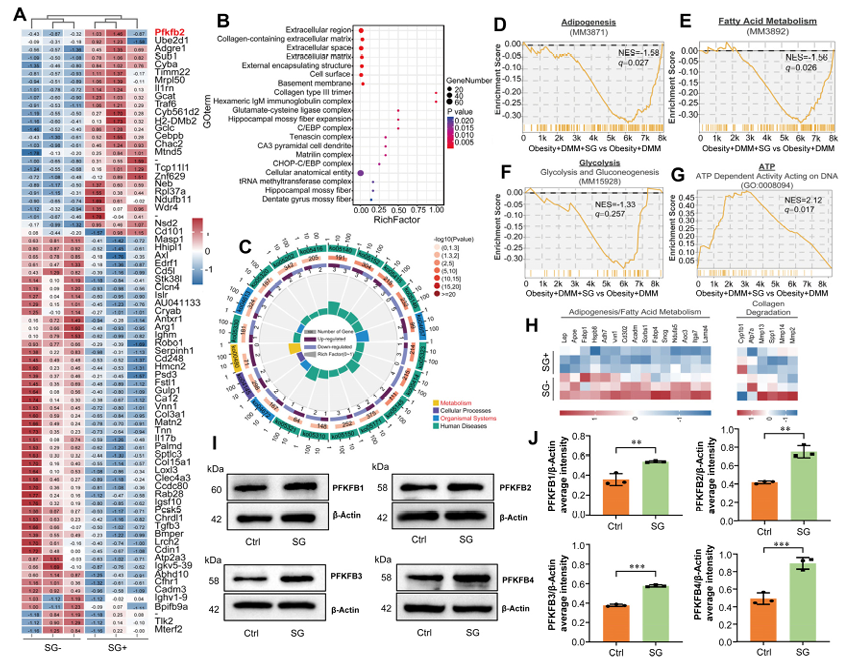
图3:司美格鲁肽(SG)通过 GLP-1R-PKA AMPK-PFKFB3 轴发挥其软骨保护作用
进一步研究发现,SG处理可上调PFKFB1–4的表达水平,其中PFKFB3的上调最为显著(图4C–D)。体外实验结果表明,SG通过促进AMPK磷酸化进而诱导PFKFB3的磷酸化修饰,而AMPK抑制剂Compound C可有效阻断这一效应(图4J–K)。
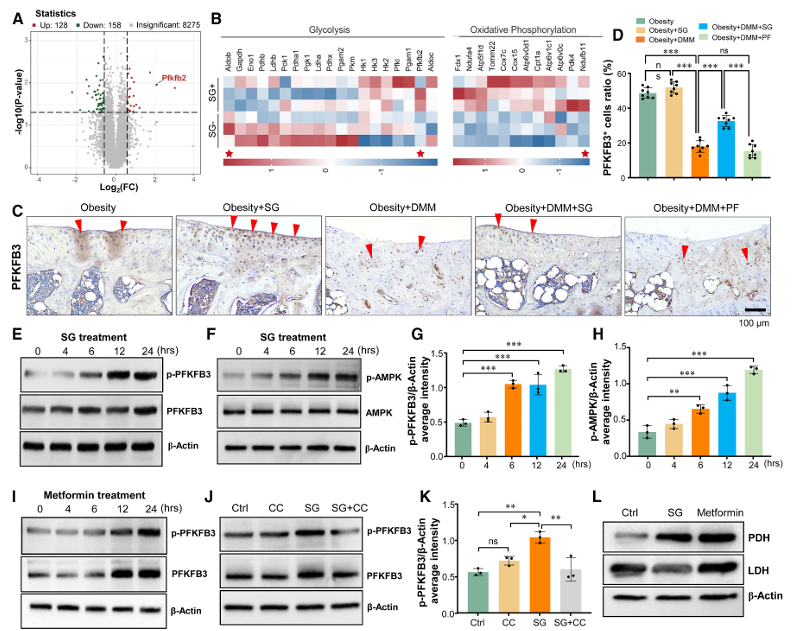
图4:SG 通过 GLP-1R-PKA-AMPK-PFKFB3 轴发挥其软骨保护作用
此外,PKA抑制剂H-89可抑制SG诱导的AMPK磷酸化,提示PKA位于AMPK上游(图5O–P)。
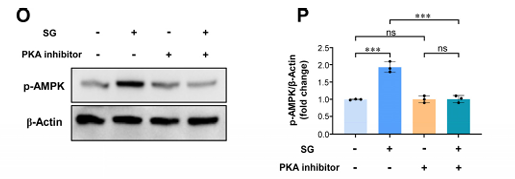
图5:H-89抑制SG诱导的AMPK磷酸化
Seahorse分析显示,在TNF-α诱导的炎症条件下,软骨细胞的糖酵解水平显著升高,而氧化磷酸化(OXPHOS)则受到明显抑制。SG处理后,细胞的糖酵解水平略有下降,而基础呼吸水平与OXPHOS来源的ATP生成均显著增加(图6A–G)。最终,细胞内总ATP产量恢复至正常水平,能量代谢模式由原先的糖酵解主导(占86.52%)转变为糖酵解与OXPHOS相对平衡的状态(图6H–I),提示SG能够有效促进软骨细胞的代谢重编程。
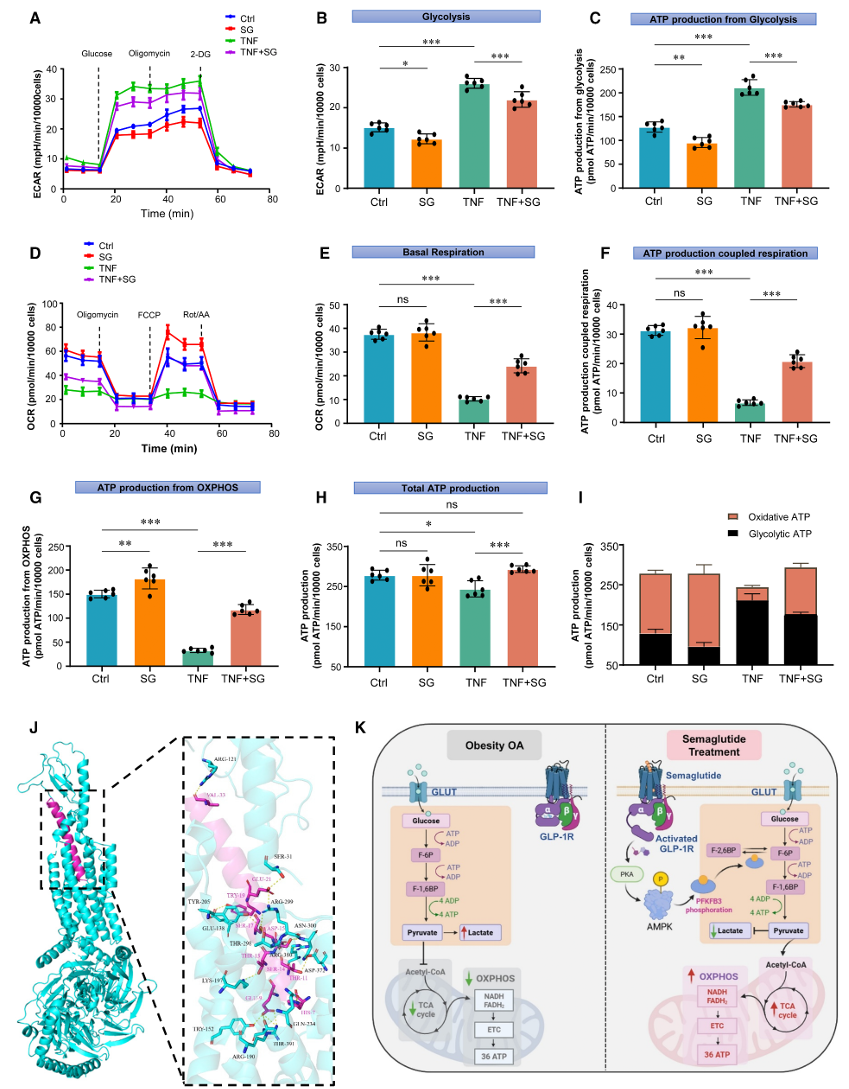
图6:SG 调节线粒体呼吸和糖酵解
在Glp-1r KO小鼠中,SG的软骨保护和镇痛作用完全消失(图7A–S)。
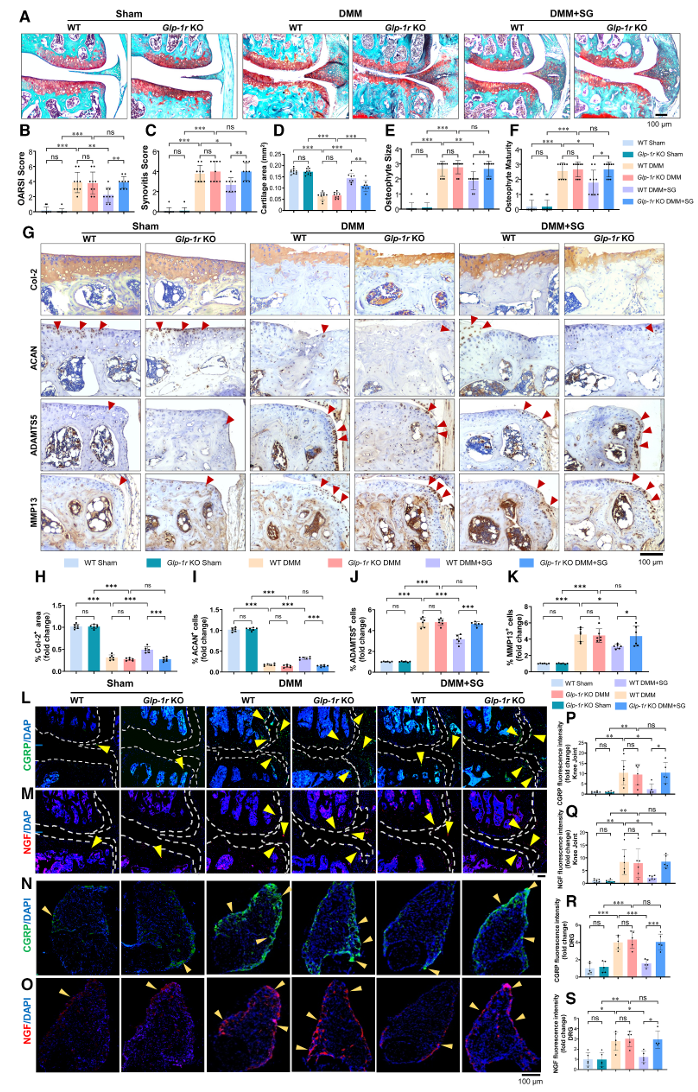
图7:GLP-1受体缺失消除了SG对软骨的保护作用
同样,在Prkaa1 cKO小鼠中,SG的治疗效果也显著减弱(图8A–S)。这些结果证实,SG通过GLP-1R-AMPK信号轴发挥其抗OA作用。
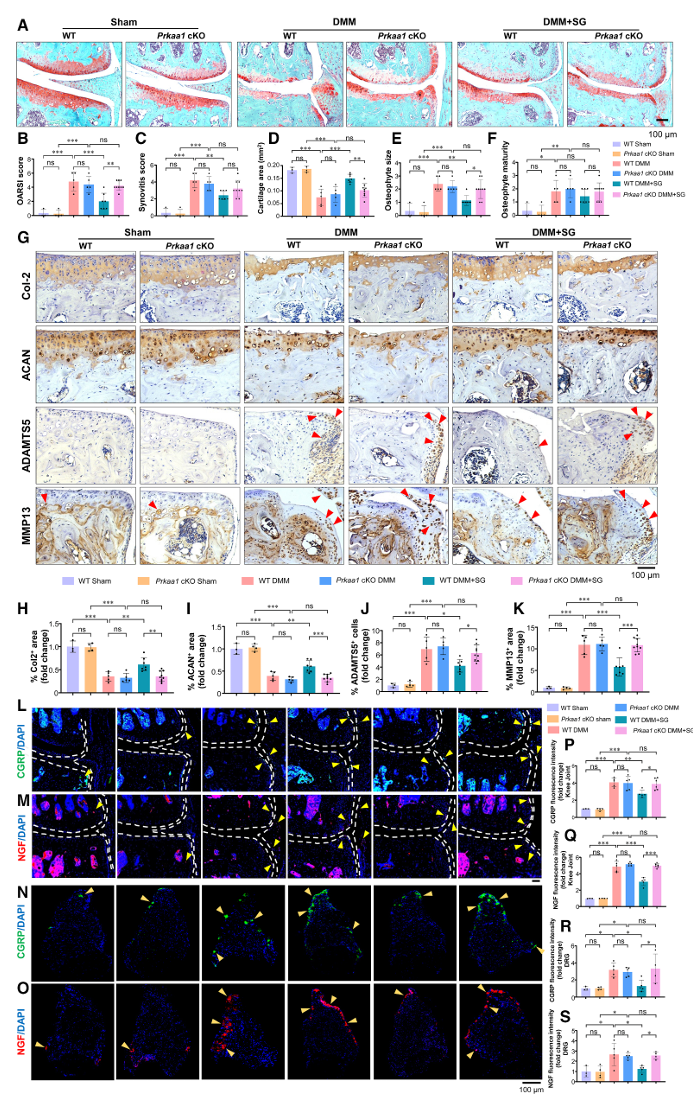
图8:Prkaa1敲除消除了SG对软骨的保护作用
在20名肥胖OA患者中,经过24周的HA联合SG治疗,患者BMI显著降低(−7.96% vs. −0.49%),WOMAC身体功能评分也显著改善(−32.75分 vs. −16.2分)(图9B–C)。MRI分析显示,HA+SG组患者的软骨厚度显著增加(约+17%),而单独HA治疗组未见明显变化(图9D–F)。
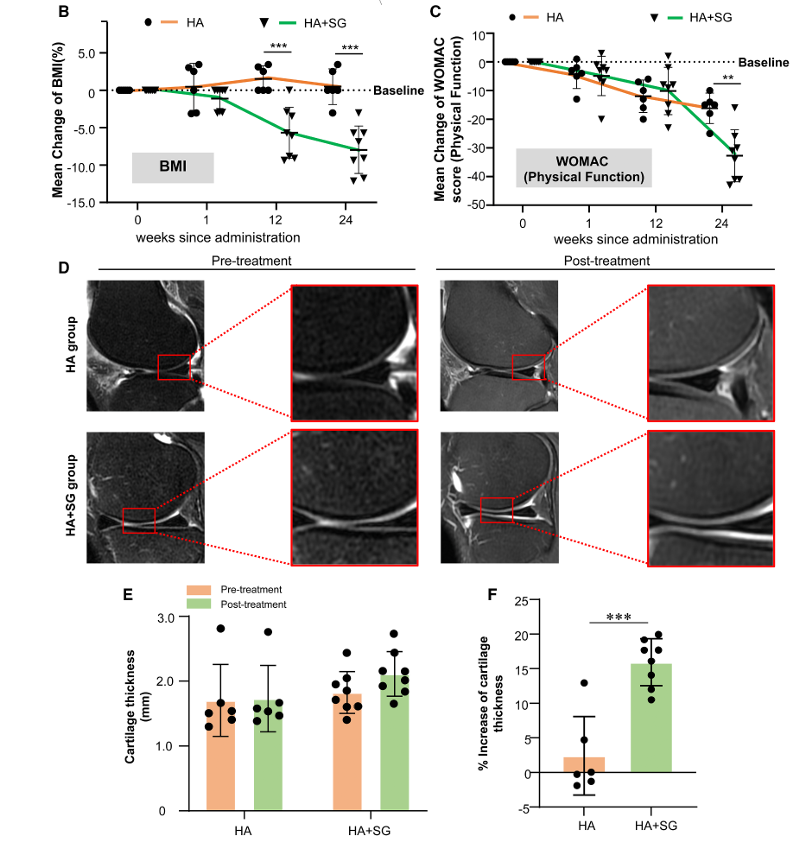
图9:SG改善了肥胖/骨关节炎患者膝关节的软骨退化
研究结论
研究揭示,SG通过激活GLP-1R-PKA-AMPK-PFKFB3信号轴,驱动软骨细胞能量代谢重编程,从糖酵解向高效氧化磷酸化,进而在不依赖体重减轻的前提下缓解肥胖相关OA的进展。该机制不仅恢复了软骨细胞的能量稳态,还促进细胞外基质合成,并减轻关节疼痛与炎症反应。基因敲除模型进一步验证了该信号通路的必要性。初步临床试验亦证实SG在改善关节功能与保护软骨方面具有潜在临床应用价值。
研究讨论
本研究揭示了SG通过代谢重编程发挥软骨保护作用的核心机制,且该作用独立于其减重效应。传统观点认为,减重主要通过降低关节机械负荷来缓解OA症状,而本研究通过配对喂养实验有效排除了这一干扰,明确了SG对软骨代谢的直接调控作用。进一步发现,GLP-1R在关节组织中的表达提示其可能直接作用于软骨细胞,而非仅依赖于全身代谢调节。
值得关注的是,SG上调了糖酵解关键调控因子PFKFB3的表达,却同时抑制糖酵解、促进氧化磷酸化(OXPHOS)。这一看似矛盾的现象可能与AMPK介导的代谢通量重分配密切相关。作为能量感应器,AMPK在低能量状态下被激活,不仅促进线粒体生物合成与OXPHOS,还可通过调控PFKFB3的磷酸化状态改变其酶活性,从而协调糖酵解与线粒体代谢之间的平衡。尽管PFKFB3通常被认为是促糖酵解因子,本研究结果表明其在软骨细胞中的功能具有可塑性:SG处理后,糖酵解被抑制的同时ATP产量反而增加,提示能量代谢效率的提升。这一转变有助于软骨细胞获得更多ATP以支持细胞外基质合成,同时减少乳酸堆积与酸中毒,从而延缓软骨退化。
此外,SG的镇痛作用亦值得关注。疼痛是OA患者最为困扰的症状之一。本研究发现SG不仅改善了机械痛阈和热痛敏,还降低了神经肽CGRP和NGF等疼痛相关标志物的表达,提示其可能通过调控神经-免疫交互作用发挥镇痛效应。这一发现为OA的综合性治疗提供了新视角。
综上所述,本研究为SG在OA治疗中的应用提供了坚实的理论基础和实验依据,提示其不仅是减重药物,更是一种潜在的疾病修饰药物。未来,随着对其代谢调控机制的深入探索,GLP-1R激动剂有望在骨科、代谢病乃至衰老相关疾病中发挥更广泛的作用。
参考文献:Qin H, Yu J, Yu H, Zhou C, Yuan D, Wang Z, Zhu Z, Wei G, Ou P, Li Z, Jiang H, Shen J, Xiao G, Bai X, Wang H, Zhang HT, Speakman JR, Chen D, Tong L. Semaglutide ameliorates osteoarthritis progression through a weight loss-independent metabolic restoration mechanism. Cell Metab. 2026 Feb 9:S1550-4131(26)00008-2.
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。仅供HCP观看。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)