导读
类风湿
研究设计
专家委员会组建
2020年,EULAR成立了“有RA风险的关节痛”领域专家委员会。2023年,ACR和EULAR决定纳入ACR专家,作为EULAR/ACR联合倡议继续推进。最终的专家委员会由来自10个欧洲国家和北美的20名风湿病学家、2名研究员、1名EMEUNET代表、4名患者研究伙伴、2名相关卫生专业人员、1名方法学家和2名统计学家组成。
研究人群
部分队列纳入因自身抗体阳性且伴有任何关节痛/肌肉骨骼(MSK)症状而被定义为有RA风险的人群;其他队列则基于风湿病学家的专业意见选择具有高进展为RA风险的关节痛特征的人群(即CSA)。专家委员会同意纳入这两种人群。此外,决定排除至少有部分个体在关节痛/MSK症状阶段接受过改善病情抗风湿药物治疗的队列。
终点设定
主要终点是在1年随访时,通过风湿病学家的体格检查确定出现临床显性IA,所有队列均收集此数据。次要终点包括1年时符合2010年EULAR/ACR的RA分类标准以及2年随访时出现IA。
研究的预测变量分为三类:临床和血清学变量(所有队列均有),以及(若有)超声(US)或
研究结果
研究10个队列包括2583名有症状的有风险人群的数据,排除了2个接受改善病情抗风湿药物治疗的队列后,有2293人纳入分析。
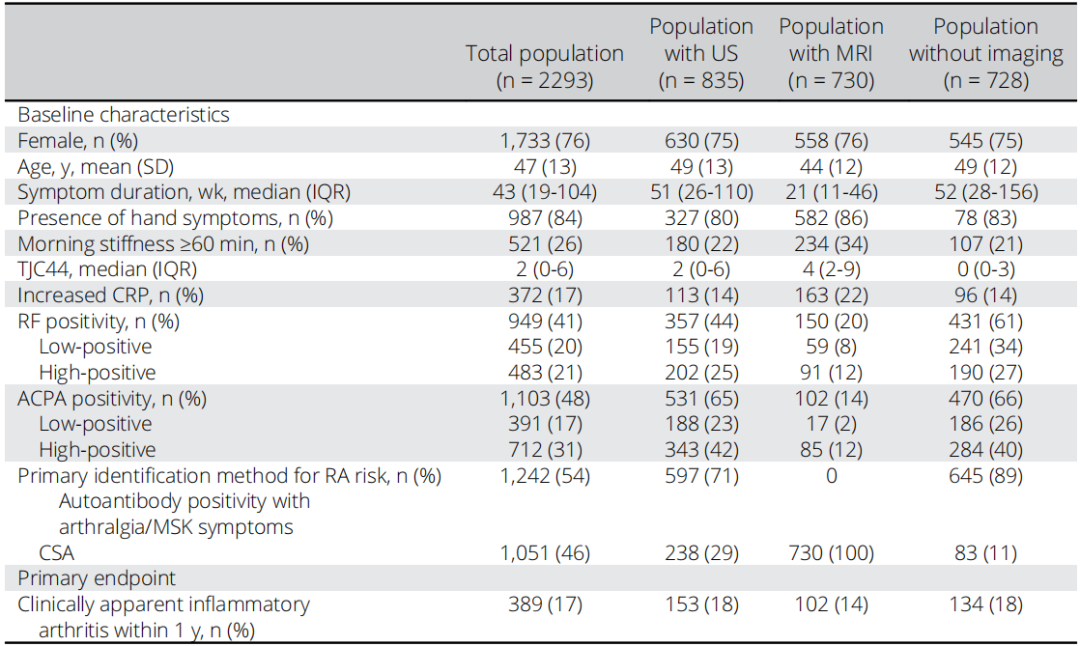
表1. 基线特征及主要终点发生频率
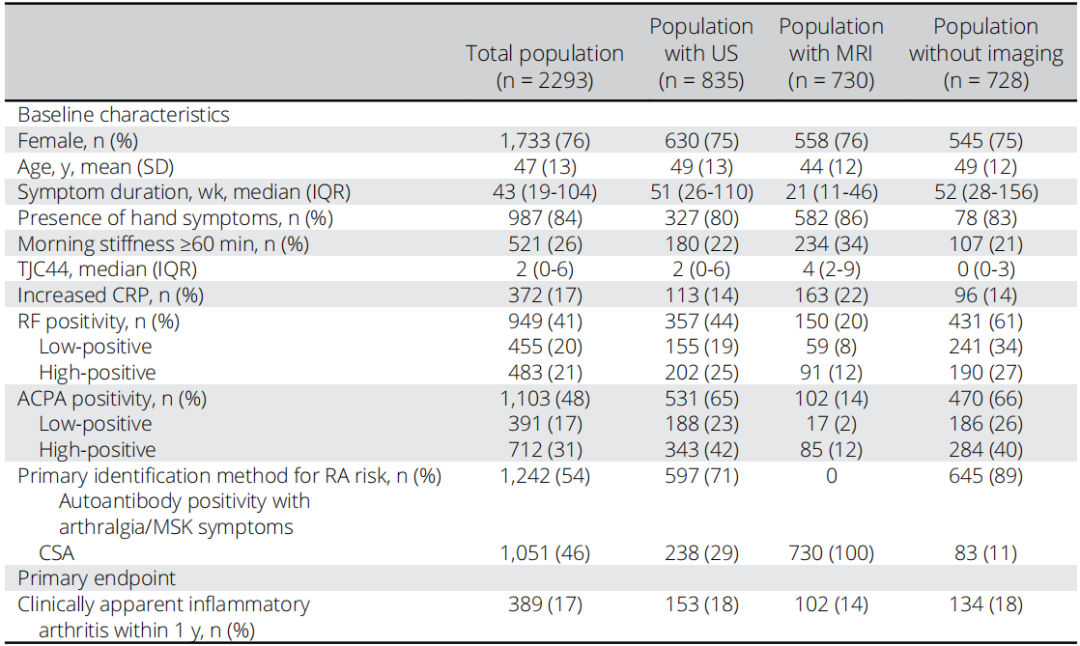
注:ACPA,抗瓜氨酸肽抗体;CRP,C反应蛋白;CSA,临床可疑关节痛;IQR,四分位距;MRI,磁共振成像;MSK,肌肉骨骼;RA,类风湿关节炎;RF,
主要终点
17%(389人)在1年内出现临床显性IA[282人抗瓜氨酸肽抗体(ACPA)阳性,107人ACPA阴性]。研究了临床、血清学和影像学因素与该终点的关系。
扩展版风险分层的制定
基于分析结果得出一种算法,使用6个临床和血清学变量[晨僵(30-60分钟、≥60分钟)、患者报告的关节肿胀、握拳困难、C反应蛋白(CRP)升高、类风湿因子(RF,低阳性、高阳性)、抗瓜氨酸肽抗体(ACPA,低阳性、高阳性)]、队列变量(基于CSA或自身抗体阳性的关节痛/肌肉骨骼症状)以及5个US[能量多普勒(PD)滑膜炎(近端指间关节PIPs)、PD腱鞘炎、PD滑膜炎(跖趾关节MTPs)、灰度(GS)滑膜炎(腕关节)、GS腱鞘炎]或6个MRI变量(腕部屈肌腱鞘炎、掌指关节伸肌腱鞘炎、跖趾关节伸肌腱鞘炎、腕部伸肌腱鞘炎、腕部骨炎、掌指关节滑膜炎)(图1)。可能的分数范围为:无影像学检查时0-28分,有US时0-40分,有MRI时0-45分。按风险分数绘制预测风险,确定了不同风险分数临界值的测试特征和预测值。
性能表现
3个模型(临床和血清学模型、+US模型、+MRI模型)的AUC分别为0.80、0.80、0.87(表2)。只有纳入MRI数据且风险分数≥12分时,才能达到敏感性79%和特异性78%(图1)。
表2. 包含临床和血清学变量及额外US或MRI检测的亚临床关节炎症的Lasso回归结果
注:数值为回归系数得出的比值比(OR)。回归系数用于推导图1中每个变量的权重。由于Lasso将系数压缩至零,变异度量无参考意义。在n=835和n=730人群中,临床和血清学Lasso模型的AUC分别为0.78(95%CI0.72-0.83)和0.84(95%CI0.79-0.88)。
ACPA,抗瓜氨酸肽抗体;AUC,曲线下面积;CI,置信区间;CRP,C反应蛋白;CSA,临床可疑关节痛;GS,灰度;Lasso,最小绝对收缩和选择算子;MCP,掌指关节;MRI,磁共振成像;MTP,跖趾关节;OR,比值比;PD,能量多普勒;PIP,近端指间关节;RA,类风湿关节炎;RF,类风湿因子。a基于CSA或自身抗体阳性关节痛/肌肉骨骼症状的RA风险识别方法。
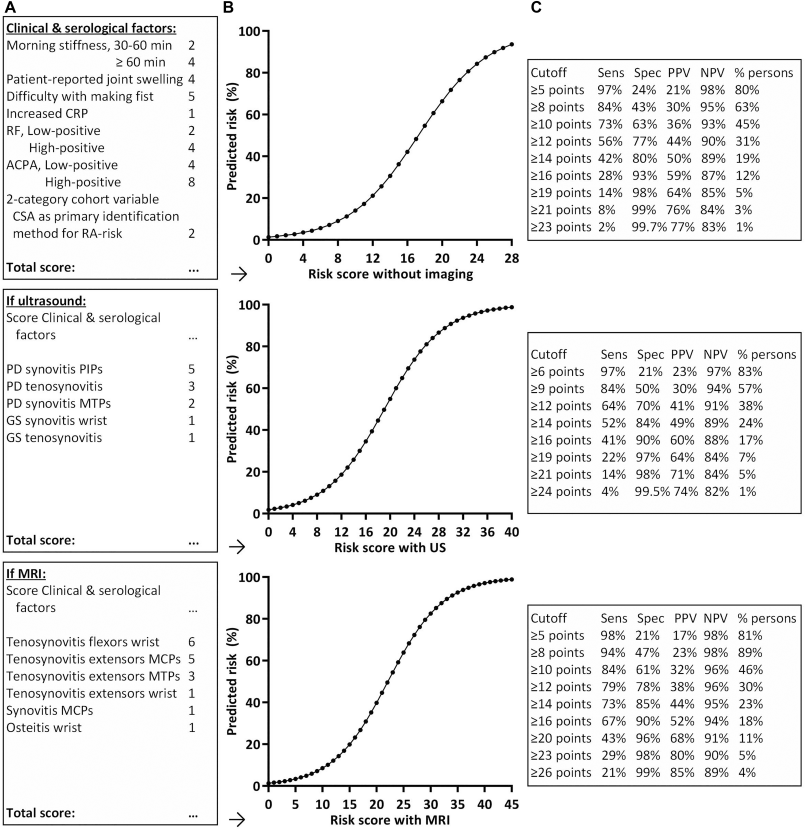
图1. 使用临床和血清学数据及额外US或MRI检测的亚临床关节炎症,对有RA风险的关节痛患者1年内发展为炎症性关节炎的风险分层(A)、各风险评分对应的预测风险(B)及不同风险评分临界值的检测特征和预测值(C)
注:无影像学检查的风险评分范围为0-28分,有超声检查的风险评分范围为0-40分,有MRI检查的风险评分范围为0-45分。纳入队列变量以调整队列间异质性,该变量按RA风险的主要识别方法分为两类,即基于自身抗体阳性关节痛/肌肉骨骼症状或CSA识别有风险人群。
ACPA,抗瓜氨酸肽抗体;CRP,C反应蛋白;CSA,临床可疑关节痛;GS,灰度;MCP,掌指关节;MRI,磁共振成像;MTP,跖趾关节;NPV,阴性预测值;PD,能量多普勒;PIP,近端指间关节;PPV,阳性预测值;RA,类风湿关节炎;RF,类风湿因子;Sens,敏感性;Spec,特异性;US,超声。
验证情况
内部验证显示AUC变异较小(表3)。在三分之二和三分之一的人群中进行的分析显示AUC仅略有变化。对5个队列组分别进行分析,AUC范围为0.75-0.84。
次要终点情况
12%(1708人中的209人)在1年时根据2010年EULAR/ACR分类标准发展为RA。该次要终点的AUC:临床和血清学数据为0.85,添加US数据后为0.84,添加MRI数据后为0.93(表3)。21%(2055人中的441人)在2年内出现临床显性IA。该终点的AUC与1年随访时大致相似(表3)。
表3. 基于Bootstrap法和数据拆分的验证性能及次要终点的性能
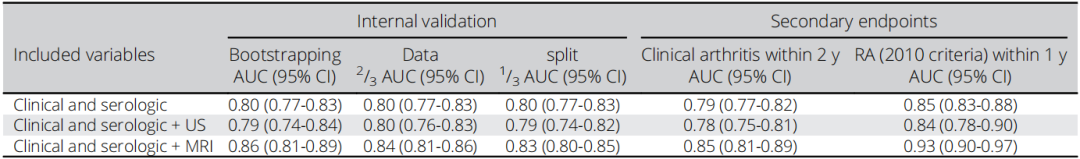
注:共2055人有2年随访数据,其中441人(21.5%)在2年内进展为临床关节炎。共1708人有临床关节炎发展及符合2010年EULAR/ACR类风湿关节炎分类标准的数据,其中209人(12.2%)在1年内发展为RA。推导模型在按队列和结局水平进行的2/3-1/3拆分后进行评估。
ACR,美国风湿病学会;AUC,曲线下面积;CI,置信区间;MRI,磁共振成像;RA,类风湿关节炎;US,超声。
简化风险分层的制定
为便于使用,对主要终点的算法进行了简化。最终标准中的临床和血清学变量为晨僵、患者报告的关节肿胀、握拳困难、CRP升高、RF和ACPA状态(表4)。对于影像学检查,纳入腕部屈肌腱鞘炎、腕部伸肌腱鞘炎、掌指关节伸肌腱鞘炎和跖趾关节伸肌腱鞘炎(表4)。临床和血清学评分范围为0-26分;添加MRI数据后,评分范围为0-42分(表4)。
简化后的临床和血清学模型AUC为0.80;添加MRI数据后,AUC为0.86。只有结合MRI数据的风险分层标准且分数≥10分时,才能达到≥75%的敏感性和特异性(敏感性75%,特异性79%)。
基于临床和血清学数据,将参与者分为低、中、高风险(分别<25%、25%-75%、≥75%),未发展为临床显性IA的患者几乎都在低风险组,发展为临床显性IA的患者分布在所有3个组中(图3)。纳入MRI数据时,中等风险组最小,占11%(图3)。
共识达成
在最终会议的投票中,96%的任务组成员批准了该分层标准。同意同时呈现扩展版和简化版,并就资格标准中定义的目标人群达成一致(表4)。
表4. 简化后的EULAR/ACR有RA风险的关节痛患者风险分层标准(在有无影像学检查时均可使用)
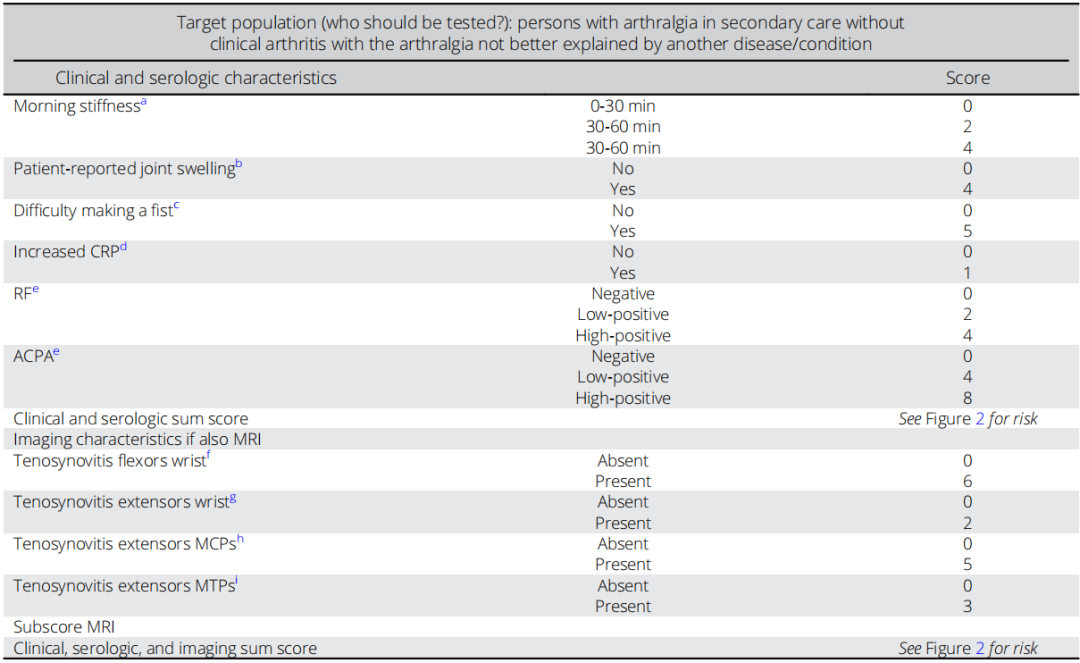
注:无影像学检查的总风险评分范围为0-26分,有影像学检查的总风险评分范围为0-42分。各风险评分临界值对应的预测风险和检测特征见图2。无影像学检查的标准AUC为0.80,有MRI数据的标准AUC为0.85。仅当有影像学数据且评分≥10分时,风险分层标准的敏感性和特异性才能达到≥75%。
ACPA,抗瓜氨酸肽抗体;CRP,C反应蛋白;IU,国际单位;MCP,掌指关节;MRI,磁共振成像;MTP,跖趾关节;RAMRIS,类风湿关节炎MRI评分;RF,类风湿因子;ULN,正常上限。
a 晨僵指患者自述的早晨关节僵硬持续时间。
b 患者报告的关节肿胀指患者自述存在关节肿胀。
c 握拳困难定义为至少一侧拳头无法完全闭合(主动握拳时指尖无法触及手掌)。
d CRP升高指超过当地实验室参考值。
e 对于RF和ACPA,阴性指国际单位值小于或等于实验室和检测方法的正常上限;低阳性指国际单位值大于正常上限但≤正常上限的3倍;高阳性指国际单位值>正常上限的3倍。
f 腕部屈肌腱鞘炎:存在(RAMRIS≥1),包括尺侧腕屈肌、尺侧滑囊(含指深屈肌和指浅屈肌腱组)、桡侧滑囊内的拇长屈肌(肌腱)或桡侧腕屈肌的任何腱鞘炎。
g 腕部伸肌腱鞘炎:存在(RAMRIS≥1),包括6个伸肌鞘中的任何腱鞘炎:(I)拇短伸肌、拇长展肌;(II)桡侧腕短伸肌、桡侧腕长伸肌;(III)拇长伸肌;(IV)指总伸肌、示指固有伸肌;(V)小指固有伸肌;(VI)尺侧腕伸肌。
h 掌指关节伸肌腱鞘炎:存在(RAMRIS≥1),指第2-5掌指关节伸肌的任何腱鞘炎。
i 跖趾关节伸肌腱鞘炎:存在(RAMRIS≥1),指第1-5跖趾关节伸肌的任何腱鞘炎。
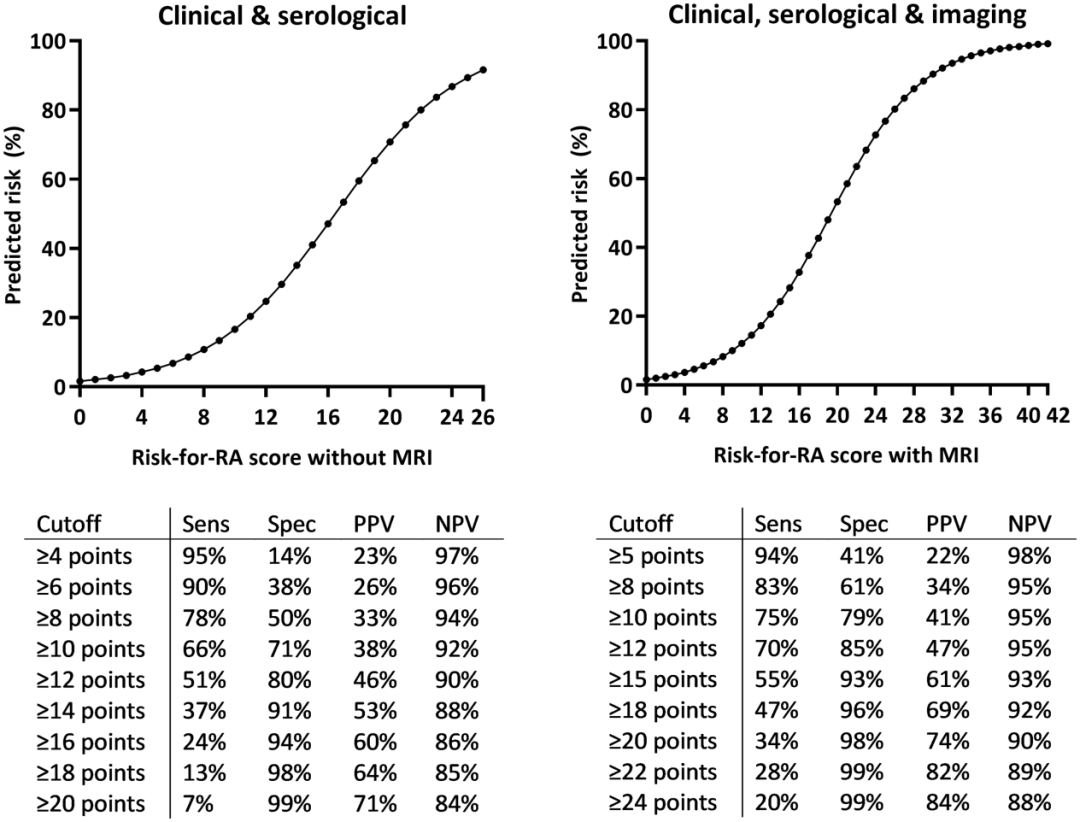
图2. 有无影像学检查的风险分层标准的预测风险(图)及各评分临界值的检测特征和预测值(表)
注:表4中总评分对应的预测风险。显示了各风险评分临界值的检测特征和预测值。无影像学检查的标准曲线下面积为0.80,有MRI数据的标准曲线下面积为0.85。
MRI,磁共振成像;NPV,阴性预测值;PPV,阳性预测值;RA,类风湿关节炎;Sens,敏感性;Spec,特异性。

图3. 基于表4中临床和血清学数据的风险分层标准,未达到终点和达到终点的受试者的预测风险分布
注:在基于临床和血清学数据的总人群(n=2293)中,将风险类别定义为低风险(<25%)、中风险(25%-75%)和高风险(≥75%)。在额外使用MRI数据的人群(n=703)中也进行了相同定义。
研究结论
基于国际队列数据和专家共识,欧洲抗风湿病联盟和美国风湿病学会联合组建的专家委员会已制定出针对有RA风险的关节痛患者的风险分层标准。该标准经过验证,旨在支持在未来的预防试验中纳入同质风险组,为RA的早期干预研究提供了有力工具,有望推动RA预防领域的发展。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)