尽管当前主流降脂疗法已显著改善
近日,《欧洲心脏杂志》(EHJ)发表的一篇综述,系统梳理了新兴降脂靶点及相关疗法。
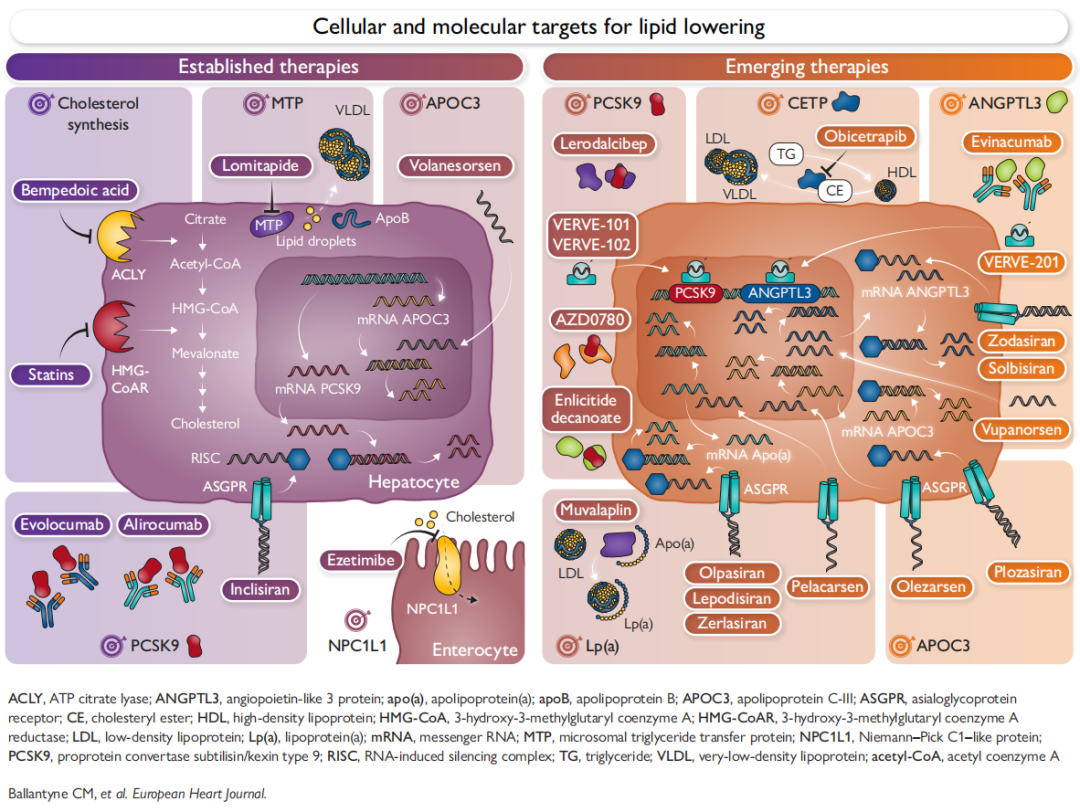
摘要图
注:当前临床常用及新兴的降脂疗法,均通过多种作用机制靶向调控脂质与脂蛋白代谢通路中的关键靶点。他汀类药物与Bempedoic acid分别作用于胆固醇生物合成通路的不同环节,
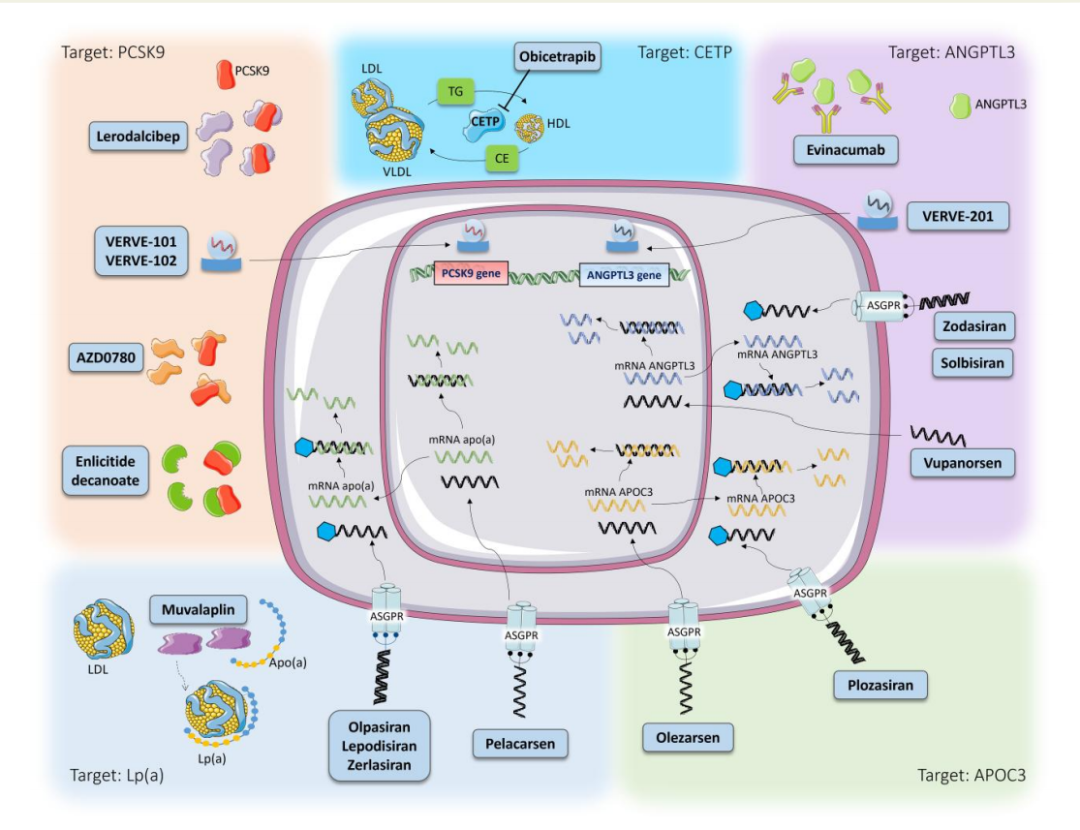
图1 新型降脂疗法的细胞和分子靶点
注:新型降脂疗法通过干扰特定的分子途径发挥作用:
(i)PCSK9抑制剂,如Lerodalcibep、Enlicitide decanoate、AZD07080及基因编辑;
(ii)CETP抑制剂,如Obicetrapib;
(iii)ANGPTL3抑制剂,如Evinacumab(单抗)、Zodasiran(siRNA)、Vupanorsen(ASO,已停止研发)以及VERVE 201(基因编辑)。
(iv)ApoC III抑制剂,如Olezarsen、普乐司兰(Plozasiran);
(v)载脂蛋白(a)靶向药物,包括基因沉默疗法和口服分子Muvalaplin,其中前者包括ASO类的Pelacarsen和siRNA类的Olpasiran、Zerlasiran和Lepodisiran。
血管生成素样蛋白3(ANGPTL3)仅在肝脏产生,在脂质代谢中发挥重要作用。ANGPTL3分泌到血液后,会抑制
Evinacumab是一种靶向循环ANGPTL3的单克隆抗体,可使HoFH患者的LDL-C水平降低50%,而与LDLR功能程度无关,其降脂效果可维持长达2.5年。
Zodasiran(ARO-ANG3)是一种靶向肝脏ANGPTL3 mRNA的GalNAc偶联小干扰RNA(siRNA)。在混合性
Solbinsiran(LY3561774)是另一种靶向ANGPTL3的GalNAc偶联siRNA,在混合性血脂异常患者的2期剂量递增研究中,中剂量组可使apoB降低14%(主要终点)、甘油三酯降低50%、LDL-C降低17%。尽管ANGPTL3的降低呈剂量依赖性(54%-77%),但低剂量和高剂量组的apoB降低无统计学意义。
载脂蛋白C-III(apoC-III)通过抑制脂蛋白脂肪酶(LPL,负责水解血液中的甘油三酯)活性,在脂质代谢中发挥关键作用。apoC-III水平升高与高甘油三酯血症相关,这是由于富含甘油三酯脂蛋白的清除受损。
旨在降低apoC-III水平的药物(包括两种ASO和一种siRNA)正在研发中,用于治疗高甘油三酯血症、预防
表1 富含甘油三酯脂蛋白靶向治疗 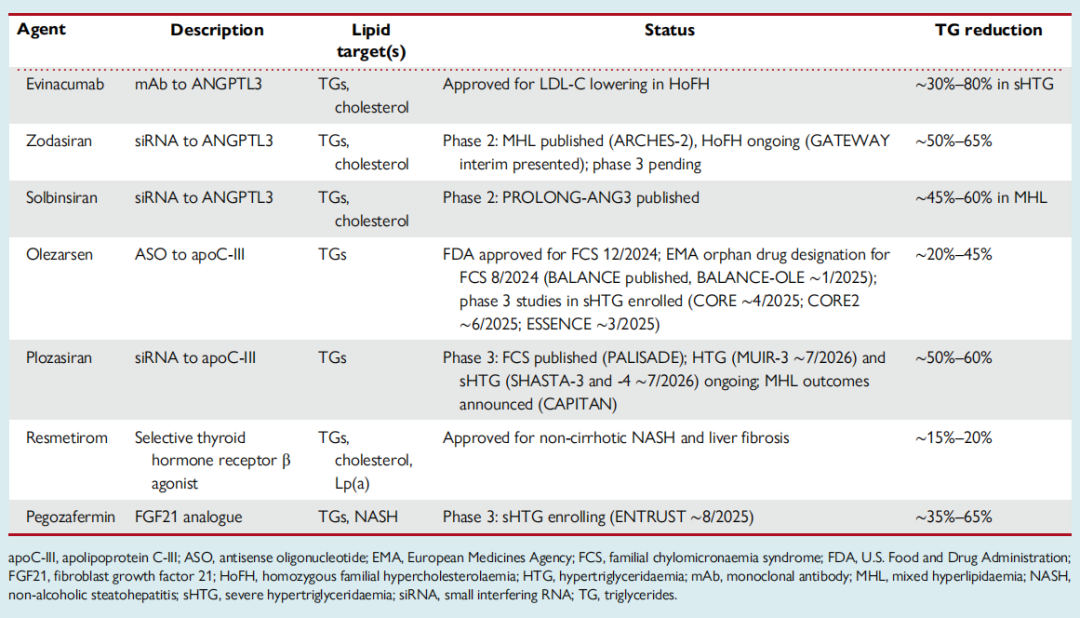
Volanesorsen是第二代ASO,特异性靶向APOC3 mRNA。在高甘油三酯血症患者中,Volanesorsen单药治疗或与稳定的贝特类药物联合治疗时,可使apoC-III降低达80%,甘油三酯降低达71%,且对FCS患者也有效。Volanesorsen治疗与
Olezarsen是一种GalNAc偶联ASO,可选择性靶向肝脏apoC-III的合成。其核酸序列与Volanesorsen相同,但GalNAc部分的存在使其给药频率更低、剂量显著降低(50 mg或80 mg),且作用持续时间更长(每4周注射一次)。在中度高甘油三酯血症且有高心血管疾病风险或已确诊心血管疾病的患者中,Olezarsen可显著降低甘油三酯水平和致动脉粥样硬化脂蛋白水平。在FCS患者中,Olezarsen可显著降低apoC-III(81%)和甘油三酯(59%)水平;治疗53周时,安慰剂组发生11次急性胰腺炎,而Olezarsen各剂量组均仅发生1次。Olezarsen已获得美国食品药品监督管理局(FDA)批准,用于降低FCS患者的甘油三酯水平,并被欧洲药品管理局(EMA)指定为FCS治疗的孤儿药。Olezarsen的3期临床试验正在进行中,以进一步评估其安全性和有效性,涉及的终点包括肝脏脂肪含量变化、血浆甘油三酯水平变化以及冠状动脉斑块进展情况。
Plozasiran是一种GalNAc偶联siRNA,可抑制肝脏apoC-III的产生。在混合性血脂异常患者中,与安慰剂相比,第1天和第12周皮下注射Plozasiran 10 mg、25 mg或50 mg(每季度一次),甘油三酯水平显著降低50%-62%;第1天和第24周注射Plozasiran 50 mg(每半年一次),甘油三酯显著降低44%(MUIR;2期)。Plozasiran 25 mg剂量已用于正在进行的3期研究。Plozasiran对重度高甘油三酯血症也有效,90%的患者甘油三酯降低至< 500 mg/dL(这被认为是急性胰腺炎风险的阈值)(SHASTA-2;2期);且在FCS患者中,Plozasiran可显著降低甘油三酯水平和胰腺炎发生率(PALISADE;3期)。核磁共振分析显示,Plozasiran可使富含甘油三酯脂蛋白的数量减少约50%,并使LDL分布向更大、致动脉粥样硬化可能性更低的颗粒转移。
成纤维细胞生长因子21(FGF21)主要由肝脏分泌,在脂肪组织、骨骼肌和胰腺中表达。FGF21调节脂质和
Pegozafermin是一种FGF21类似物,通过位点特异性糖基转移酶进行
胆固醇酯转移蛋白(CETP)促进甘油三酯从VLDL和LDL转移至HDL,同时交换胆固醇酯。遗传研究表明,CETP活性降低可改善脂蛋白谱,并降低心血管事件发生率。这些发现促使科学家研究CETP抑制对血浆脂质和心血管疾病结局的影响,最初的研究重点是升高HDL-C水平。更强效的CETP抑制剂还可降低血浆LDL-C和apoB水平;尽管Anacetrapib对非HDL-C的降低作用不大,但这也解释了在REVEAL试验中其主要不良心血管事件发生率更低的原因。由于Anacetrapib半衰期较长,且会在脂肪组织中蓄积,其开发后来被终止,但REVEAL试验的观察结果为进一步研究CETP作为降低血浆LDL-C水平和改善心血管疾病结局的潜在靶点奠定了基础,随着随访时间延长观察到心血管事件减少幅度更大。
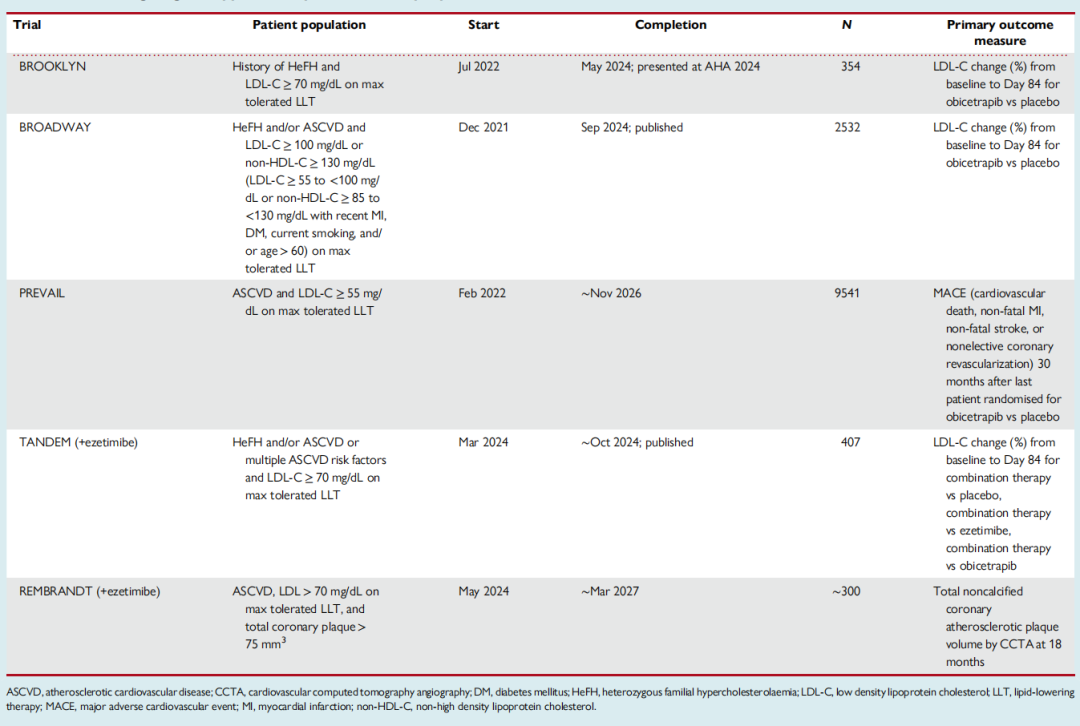
迄今为止,Obicetrapib是临床研发中最强效的CETP抑制剂(表2)。在尽管使用了高强度他汀但LDL-C仍≥70 mg/dL的患者中,加用Obicetrapib可使LDL-C降低50%,并降低apoB、非HDL-C和Lp (a) 水平;Obicetrapib联合依折麦布可使LDL-C降低63%。研究显示,HeFH和/或ASCVD患者接受Obicetrapib治疗可进一步降低LDL-C水平。Obicetrapib的潜在获益似乎与apoB和LDL-C降低直接相关,这表明CETP抑制可降低不同类型的致动脉粥样硬化脂蛋白。
表2 研发中的CETP靶向治疗
Lp(a) 是一种LDL样颗粒,其中apoB与载脂蛋白(a) [apo (a)] 共价结合。Lp(a) 水平升高是心血管疾病(包括
目前的降脂疗法对Lp(a) 水平无影响或仅能降低20%-25%。现有数据表明,迄今为止最强效的CETP抑制剂Obicetrapib可使Lp(a)水平降低达56%,甲状腺激素受体β选择性激动剂Resmetirom可使Lp(a)降低约33%。然而,这样的降低幅度似乎不足以降低Lp(a)的致动脉粥样硬化潜力。事实上,据估计,Lp(a)水平降低> 80% 才具有临床有效性,这表明需要更强效的治疗方法。
尽管目前尚获批的无专门用于降低血浆Lp(a)水平的药物,但已有多种疗法处于临床研发阶段,包括:(i)反义寡核苷酸;(ii)小干扰RNA;(iii)Lp(a)翻译后组装的特异性抑制剂;(iv)通过CRISPR-Cas9技术进行apo(a)基因编辑(表3)。
表3 脂蛋白(a)靶向治疗
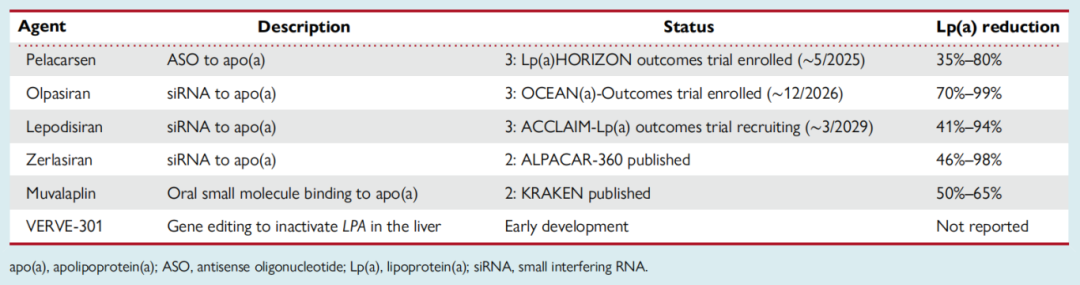
Pelacarsen是一种靶向apo(a)的ASO。在血浆Lp(a)水平升高的心血管疾病患者中进行的临床试验显示,Pelacarsen降低Lp(a)达66%-92%。HORIZON是一项3期心血管结局试验,纳入Lp(a)≥70 mg/dL的心血管疾病患者,随访4年,旨在评估每月皮下注射Pelacarsen 80mg对患者主要不良心血管事件风险的影响。
目前至少有三种靶向apo(a) mRNA的siRNA处于研发阶段:Olpasiran、Zerlasiran和Lepodisiran。这些分子均采用GalNAc化学修饰以选择性靶向肝脏,但药代动力学特征不同。Olpasiran可使Lp(a)降低71%-98%,一项针对Lp(a)水平极高(≥200 nmol/L)患者的心血管结局试验OCEAN (a)-Outcomes-TIMI 75正在进行中。Zerlasiran和Lepodisiran可在短期内使Lp(a)降低超90%,且长期平均降低幅度超80%。Lepodisiran的3期心血管结局研究ACCLAIM-Lp(a)正在招募参与者。
除了ASO和siRNA外,口服药物Muvalaplin通过阻断apo(a)与apoB结合来降低Lp(a)水平。研究表明,Muvalaplin可显著降低Lp(a)达50%-86%。
尽管这些方法几乎可以完全清除循环中的Lp(a),但在考虑将降低升高的Lp(a)水平纳入心血管风险降低策略之前,关键是要明确这种降低幅度对心血管保护的转化程度。在等待心血管结局试验结果的同时,监测长期血浆Lp(a)水平极低是否会导致葡萄糖代谢变化也至关重要,因为遗传性血浆Lp(a)水平极低的个体患
文献索引:Christie M Ballantyne , Giuseppe D Norata. The evolving landscape of targets for lipid lowering: from molecular mechanisms to translational implications. European Heart Journal, 2025: 46(44): 4737–4750.
上篇推荐
医脉通是专业的在线医生平台,“感知世界医学

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)