当单一靶点的肠促
近期,三靶点受体激动剂Retatrutide的TRANSCEND-T2D-1试验数据公布,或许正预示着这一转折点的到来。
2026年3月19日,礼来(Eli Lilly)公司公布了其在研的

数据显示,该新型分子在40周的治疗期内[疗效估计目标(Efficacy estimand)],不仅实现了高达2.0%的
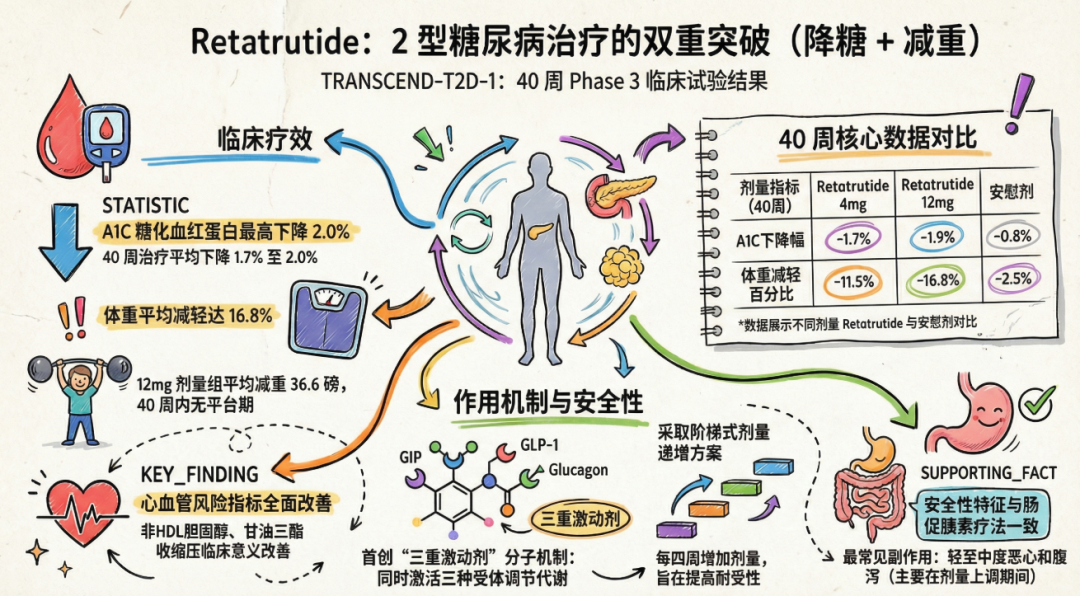
TRANSCEND-T2D-1是一项为期40周的随机、双盲、安慰剂对照Ⅲ期临床研究。研究共纳入了537名仅靠饮食和运动无法有效控制血糖的成年T2D患者。这些患者的平均糖尿病病程为2.5年,在研究的第一次访视时,其HbA1c水平介于7.0%至9.5%之间,
研究将患者按1:1:1:1的比例随机分配至retatrutide 4 mg、9 mg、12 mg剂量组或安慰剂组。治疗方案采用严谨的阶梯式剂量递增策略:患者以每周一次2 mg的剂量起始,每四周递增一次。具体爬坡路径如下:
4 mg目标剂量组:经过一步2 mg剂量过渡。
9 mg目标剂量组:依次经过2 mg、4 mg和6 mg剂量递增。
12 mg目标剂量组:依次经过2 mg、4 mg、6 mg和9 mg剂量递增。
该试验成功达到了主要终点及所有关键次要终点,无论基于疗效估计目标(efficacy estimand)还是治疗方案估计目标(treatment-regimen estimand),retatrutide在40周时的降糖和减重效果均显著优于安慰剂。
显著的HbA1c改善: 针对主要终点(基线A1C平均为7.9%),基于疗效估计目标,retatrutide 4 mg、9 mg和12 mg组的A1C分别平均降低了1.7%、2.0%和1.9%,而安慰剂组仅降低0.8%。
持续且显著的体重减轻: 在关键次要终点方面(受试者基线平均体重为96.9 kg,平均BMI高达35.8 kg/m²),基于疗效估计目标,12 mg剂量组患者在40周时实现了高达16.8%(平均16.6 kg)的体重减轻。9 mg组和4 mg组也分别实现了15.5%和11.5%的显著减重,相比之下安慰剂组仅减重2.5%。值得注意的是,retatrutide治疗组在40周时并未观察到减重平台期,患者的体重下降趋势在整个治疗期内都在持续。
除核心指标外,retatrutide还展现出广泛的代谢获益。临床数据显示,该药物显著改善了包括非高密度脂蛋白(non-HDL)胆固醇、甘油三酯和
在安全性方面,retatrutide的不良事件(AEs)特征与目前临床上其他肠促胰岛素类疗法观察到的情况保持一致。
胃肠道反应: 最常见的不良事件为恶心(4 mg、9 mg、12 mg组的发生率分别为16.4%、19.5%、26.5%,安慰剂组为3.7%)、
其他不良事件及停药率: 感觉异常(dysesthesia)的发生率分别为4.5%(4 mg组)、2.3%(9 mg组)和4.4%(12 mg组),而安慰剂组为0.0%。这些事件通常程度较轻,且大部分在治疗期间自然缓解。因不良事件导致的停药率在retatrutide 4 mg、9 mg和12 mg组中分别为2.2%、4.5%和5.1%,安慰剂组为0.0%。
TRANSCEND-T2D-1研究的详细数据预计将于2026年6月的美国糖尿病协会(ADA)科学年会上正式公布,并在同行评审期刊上发表。
此外,整个TRANSCEND-T2D Ⅲ期临床项目共包含三项全球注册试验,自2024年启动以来已入组超过2050名参与者,更多关于retatrutide治疗
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)