30年前,患有中重度
而如今,我们正见证儿科AD治疗范式的根本性转变。
从生物制剂获批扩展至6月龄的婴儿,到JAK抑制剂在青少年中的探索,再到早期积极治疗能否改变特应性进程这一核心命题——在2026年AAD年会上,国际
对于反复发作的中重度特应性皮炎患儿,何时该启动系统治疗?

点击图片打开MedSeeker了解详细解答。您也试试向MedSeeker提问吧!
升级至系统治疗并非单纯依据
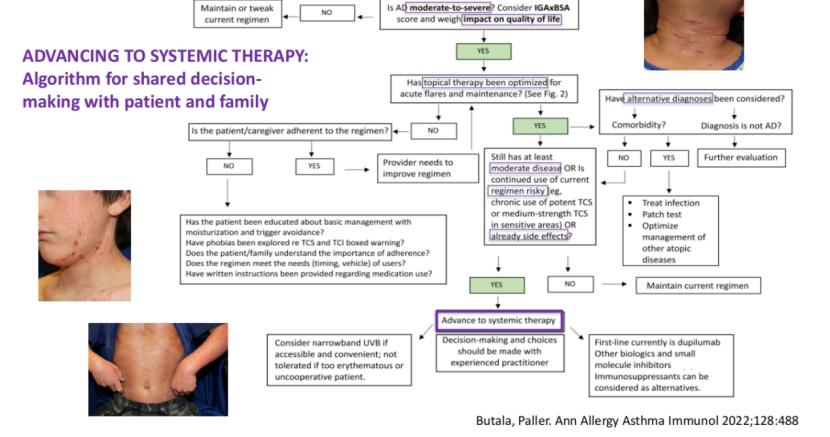
图1 临床决策流程图
当患儿经规范局部治疗仍持续存在中度以上皮损,或当前方案存在风险(如长期强效外用激素导致皮肤萎缩、敏感部位使用风险),或已出现明显副作用时,方可考虑推进至系统治疗。这一决策需由经验丰富的临床医师与患儿家庭共同完成,充分权衡疗效、安全性及家庭实际情况。
在生物制剂时代之前,光疗与系统性免疫抑制剂是主要选择,但均存在显著局限。窄谱UVB(nbUVB)光疗要求每周2-3次治疗,对家庭时间成本要求极高;家用光疗设备价格昂贵且需专业培训,皮肤炎症明显时患儿往往无法耐受。系统性糖皮质激素虽起效迅速,但毒性累积与停药后反跳现象使其不适合持续使用。

图2 光疗、系统性激素、环孢素A、甲氨蝶呤四大传统治疗及其对应局限性
这些传统疗法的共性困境在于:要么疗效与毒性难以平衡,要么治疗负担过重,难以满足儿童长期疾病管理的需求。因此,基于发病机制的靶向治疗成为必然方向。
现代AD治疗的核心在于精准干预2型炎症通路。Paller教授展示的发病机制图清晰揭示了AD的病理生理网络:表皮屏障破坏导致过敏原、病原体侵入,进而激活朗格汉斯细胞、真皮树突状细胞及2型固有淋巴细胞,驱动辅助性T细胞2(Th2)过度活化,释放IL-4、IL-13、IL-31等关键细胞因子,通过JAK-STAT信号通路促进角质形成细胞过度增殖与瘙痒传导。
作为首个获批用于6个月以上中重度AD患儿的生物制剂,度普利尤单抗通过阻断IL-4Rα同时抑制IL-4与IL-13信号传导。长达5年的学龄前儿童随访数据显示,该药未出现新的安全性信号,常见不良反应仍为注射部位反应与
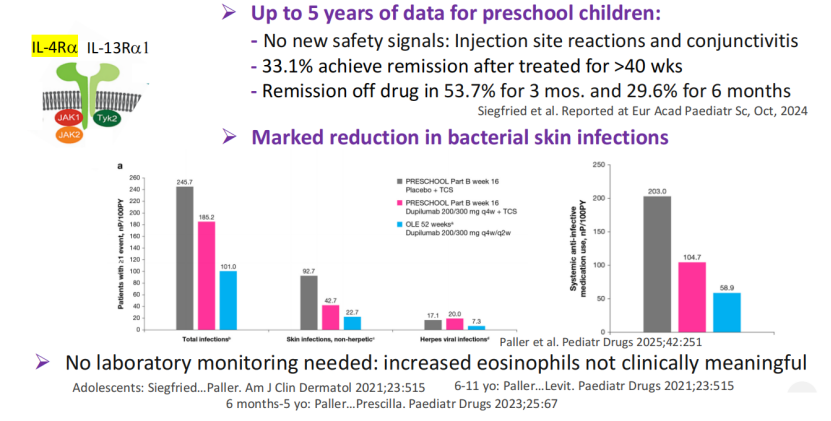
图3 度普利尤单抗机制图(IL-4Rα/IL-13Rα1/JAK1/Tyk2)及感染数据柱状图
在儿童生长发育维度,度普利尤单抗同样带来积极信号。一项纳入1329名12岁以下中重度AD患儿的10年观察性研究(PEDISTAD)发现,未经系统治疗的患儿虽体重/体质指数(BMI)偏高,但身高发育相对滞后。而在度普利尤单抗III期试验及其开放标签延伸研究中,6-11岁患儿在治疗0-52周期间,平均
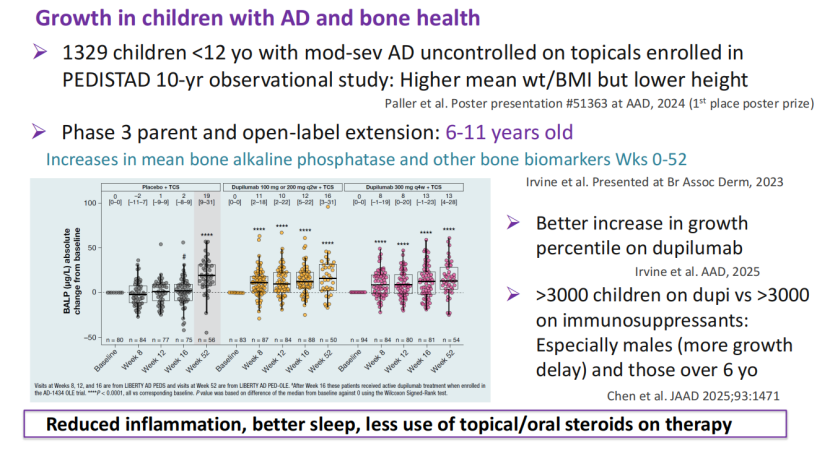
图4骨碱性磷酸酶(BALP)绝对变化箱式图
Paller教授同时提出了若干前瞻性临床问题:鉴于度普利尤单抗在6月龄以上患儿中表现出的强劲安全性,是否应降低早期积极治疗的阈值?早期干预能否改变AD的自然病程乃至"特应性进程(Atopic March)"?真实世界BioDay研究给出了部分启示:84名接受度普利尤单抗治疗52周的患儿中,合并
IL-13特异性抑制剂:青少年治疗的新选择
针对IL-13通路的单克隆抗体为青少年AD患者提供了更精准的靶向方案。曲罗芦单抗在12-17岁中重度AD青少年中开展的III期研究显示,150mg每两周(Q2W)给药组在第16周时IGA 0/1应答率达21.4%(p<0.001),EASI 75应答率达28.6%(p<0.001),峰值瘙痒NRS≥4分改善率达23.2%(p<0.001),儿童皮肤病生活质量指数(CDLQI)≥6分改善率达31.0%(p<0.05),均显著优于安慰剂。
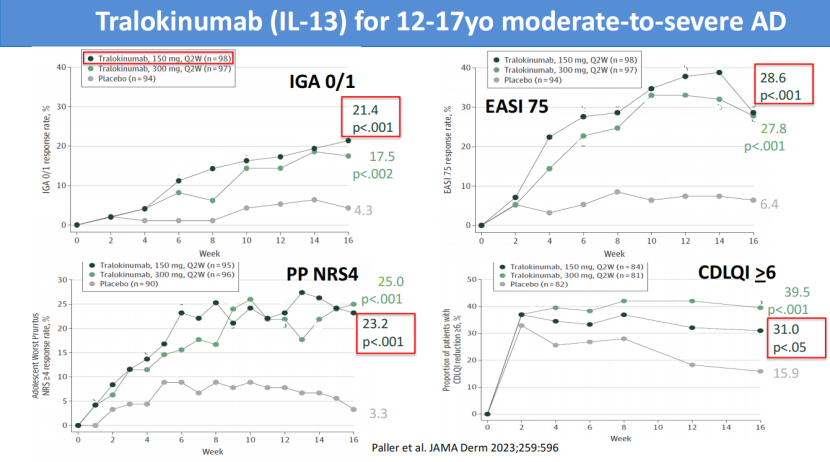
图5 曲罗芦单抗12-17岁疗效四联图(IGA 0/1、EASI 75、PP NRS4、CDLQI ≥6)
在维持治疗阶段,曲罗芦单抗展现出灵活的剂量调整潜力。数据显示,第52周时150mg Q2W组IGA 0/1应答率为66.7%,而延长给药间隔至每四周(Q4W)仍维持60.0%的应答率;300mg Q4W组IGA 0/1应答率更达87.5%。EASI 75方面,150mg Q4W维持率为50.0%,300mg Q4W达53.8%。其安全性特征与度普利尤单抗相似,为长期用药提供了保障。
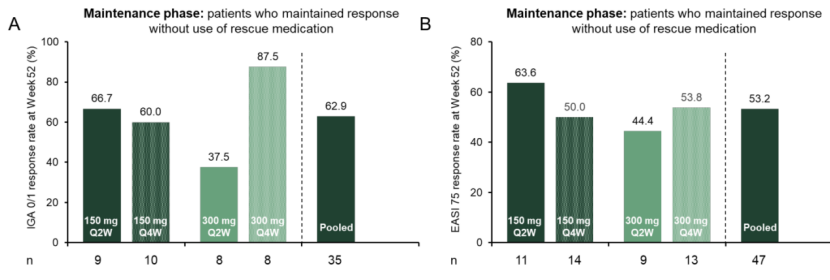
图6 曲罗芦单抗维持治疗柱状图(IGA 0/1与EASI 75在Week 52的Q2W vs Q4W对比)
来
Nemolizumab:靶向瘙痒通路的突破
IL-31是AD瘙痒信号传导的关键介质。Nemolizumab通过阻断IL-31受体实现快速止痒。青少年数据显示,治疗16周时瘙痒NRS<2的患儿比例达30.1%,显著高于安慰剂组的6.7%(p<0.0001);IGA 0/1应答率48.9% vs 34.4%(p=0.0453)。但需注意,该药抗炎起效相对较慢,需联合外用TCS/TCI;同时需警惕哮喘加重或水肿风险。
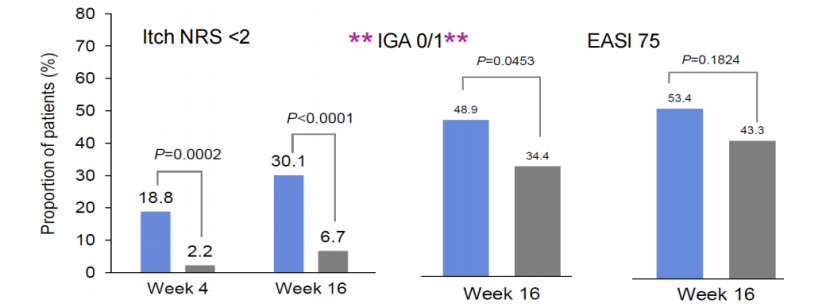
图7 Nemolizumab青少年疗效三联图(Itch NRS<2、IGA 0/1、EASI 75)
JAK抑制剂:口服便利与风险权衡
JAK抑制剂通过阻断JAK-STAT信号通路,同时抑制IL-4、IL-13、IL-31、IL-33及TSLP等多条瘙痒与炎症轴,具有口服便利、起效迅速、清除快速的独特优势,尤其适用于合并斑秃或白癜风的患儿。网络Meta分析显示,在青少年及成人中,乌帕替尼30mg(RD 0.62,95%CI 0.53-0.71)与15mg(RD 0.52)在IGA 0/1应答方面位居前列,阿布昔替尼200mg(RD 0.40)与度普利尤单抗300mg+TCS(RD 0.43)紧随其后,而巴瑞替尼1mg与安慰剂无显著差异。
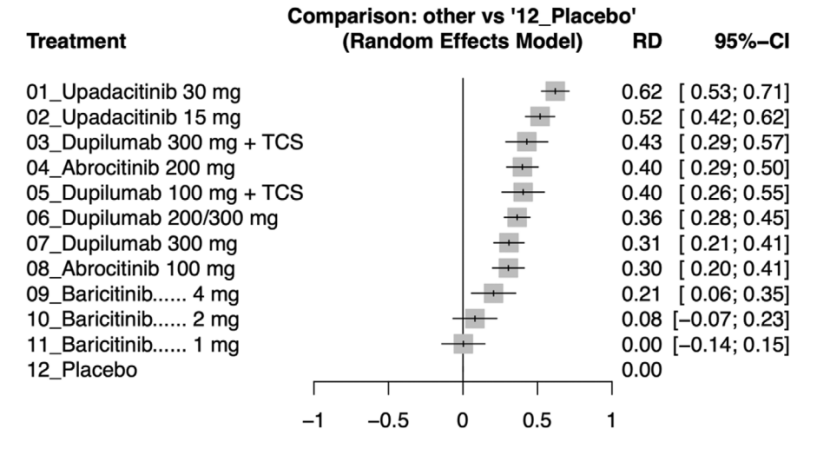
图8 网络Meta分析森林图
然而,JAK抑制剂目前在美国仅获批用于12岁以上患者,且此类药物均携带FDA黑框警告,提示严重感染、血栓、心血管事件及恶性肿瘤的潜在风险。此外,该类药物需实验室监测,痤疮、疱疹感染及中性粒细胞减少的发生率高于生物制剂。Paller教授指出,安全性顾虑通常是家长拒绝JAK抑制剂的首要因素,临床医师需充分沟通获益-风险比,并密切随访。
结膜炎是IL-4Rα与IL-13靶向生物制剂的共同关注点,因IL-13对结膜杯状细胞黏液分泌具有生理刺激作用。Paller教授建议,若基线已存在结膜炎并非用药禁忌,但需提前联络眼科医师;治疗期间可使用无防腐剂人工泪液预防,必要时于眼睑外用他克莫司软膏。
在疗程规划上,生物制剂转换需预留1-2个月重叠期;应持续外用TCS直至皮损基本清除,并维持至少一年后再评估是否尝试减停。若需停药,建议逐步延长给药间隔而非骤停;一旦复发,优先强化局部治疗,若应答不佳则考虑换用其他生物制剂或JAK抑制剂(适用于>12岁)。
儿科AD系统治疗的未来图景令人期待。延长半衰期抗体技术有望将给药间隔延长至每12周甚至每年一次,极大减轻患儿及家庭的治疗负担。双特异性及三特异性抗体正在研发中,通过同时靶向IL-4R、IL-13、IL-18、IL-31R、IL-33及TSLP中的多个靶点,追求更高疗效与更长给药间隔。此外,OX40L抑制剂Amlitelimab已在青少年中开展2b期试验,其6个月应答可持续至1年,为T细胞共刺激通路抑制提供了新证据。
从传统免疫抑制剂的"力不从心",到度普利尤单抗、曲罗芦单抗、来瑞奇珠单抗等生物制剂在儿科人群中的循证突破,再到JAK抑制剂提供的口服替代方案,儿童中重度AD的系统治疗已进入精准化、个体化的新纪元。Paller教授强调,临床医师需在治疗升级节点与家庭共享决策,在长期管理中平衡疗效、安全性与患儿生长发育需求,同时关注注射体验与生活质量改 善。 随着更长效制 剂与多靶点药物的研发推进,儿科AD的治疗前景将更加广阔,最终实现从"控制疾病"到"修饰病程"的 跨越。
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。