前言
研究背景
尽管
研究设计
本研究为一项基于RESPECT III期随机临床试验(NCT01104935)的预设转化研究(Trans-RESPECT)。RESPECT试验纳入275例70-80岁、已完成根治性手术的I-IIIA期HER2阳性早期乳腺癌女性患者,随机分配至曲妥珠单抗单药治疗组或曲妥珠单抗联合化疗组。
Trans-RESPECT研究主要研究终点为评估HER2DX风险评分与无复发生存期(RFS)的关联,总生存期(OS)为关键次要终点,同时分析HER2DX pCR可能性评分对化疗获益的预测价值,以通过基因组工具优化老年HER2阳性乳腺癌的治疗决策。
研究结果
► 患者临床特征
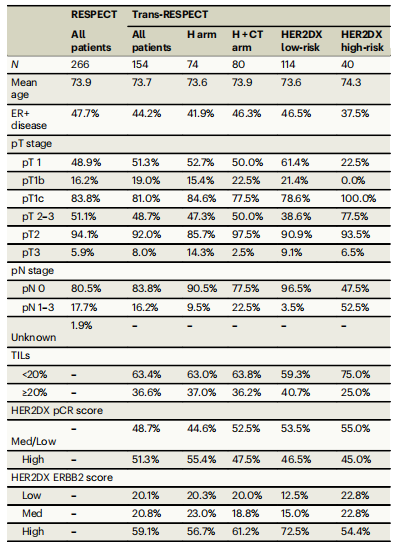
本研究对RESPECT试验中成功完成HER2DX检测的154例患者进行了分析。该亚组患者平均年龄73.7岁,44.2%为
患者特征:74例(48.1%)接受曲妥珠单抗单药治疗,80例(51.9%)接受联合化疗。HER2DX高风险患者更常见淋巴结阳性(52.5% vs 3.5%)和较大肿瘤(77.5% vs 38.6%)。
生存结局:中位随访9.3年期间,共记录30例RFS事件和22例OS事件。所有OS事件均发生在RFS之后。
治疗组比较:与原始试验一致,两治疗组在RFS和OS方面均无显著差异。
预后因素:单变量分析显示,年龄是唯一与生存结局显著相关的临床变量。
表1 RESPECT及Trans-RESPECT队列患者的临床与病理特征2
► HER2DX风险评分及其预后价值
根据HER2DX风险评分,74.0%(114例)的患者被划分为低风险,26.0%(40例)为高风险。
生存分析显示,HER2DX低风险组患者长期结局更优:
整体人群:低风险组10年RFS率为77.9%,高风险组为68.0%(HR=0.48;95%CI 0.23–1.01;p=0.05);10年OS率分别为85.9%和69.7%(HR=0.34;95%CI 0.15–0.80;p=0.01)(图1A、B)。
淋巴结阴性亚组:低风险患者10年RFS率为77.8%,高风险患者为58.6%(HR=0.36;95%CI 0.15–0.86);10年OS率分别为86.3%和47.7%(HR=0.20;95%CI 0.08–0.53)(图1C、D)。
多变量分析:在校正年龄、肿瘤分期等因素后,HER2DX风险分组仍与总生存率显著相关。
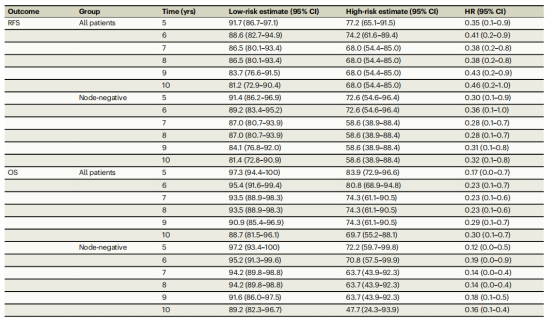
结果稳健性:5-10年间敏感性分析显示结果一致,所有风险比估计值均持续低于0.50(表2)。
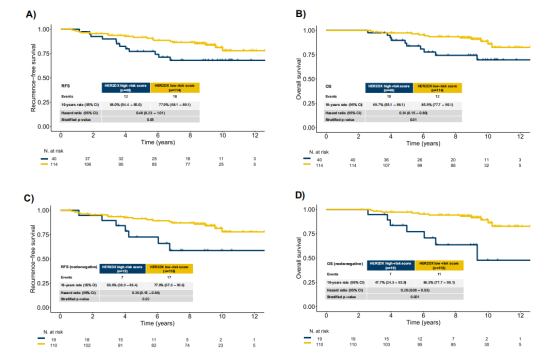
图1 | HER2DX风险评分对长期结局的预后价值2
A 根据HER2DX风险分组的全体患者RFS的Kaplan-Meier曲线。
B 根据HER2DX风险分组的全体患者OS的Kaplan-Meier曲线。
C 淋巴结阴性亚组中按HER2DX风险分组的RFS。
D 淋巴结阴性亚组中按HER2DX风险分组的OS。
表2 HER2DX风险评分在整体队列及淋巴结阴性亚组中RFS与OS的敏感性分析2
► 单独接受曲妥珠单抗治疗的淋巴结阴性患者的HER2DX风险评分分析
在该研究人群中,根据HER2DX风险评分,85.1%(57例)为低风险,14.9%(10例)为高风险。
5年结局:低风险组与高风险组的RFS率分别为88.6% vs. 68.6%,OS率分别为96.4% vs. 80.0%。
10年结局:低风险组与高风险组的RFS率分别为76.2% vs. 57.1%,OS率分别为81.1% vs. 45.7%。
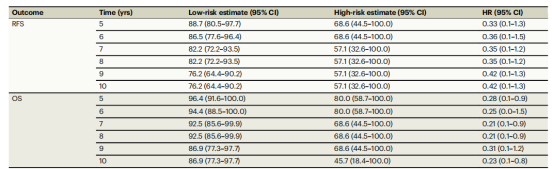
结果稳健性:敏感性分析证实在5-10年间,风险比估计值均支持低风险组获益更优,其RFS和OS的风险比持续低于0.50(表3)。
表3 单独接受曲妥珠单抗治疗的淋巴结阴性患者HER2DX风险评分对RFS与OS的敏感性分析2
► HER2DX风险评分、年龄与生存结局
年龄影响:年龄与RFS(HR=1.21;95%CI 1.07-1.36;p=0.002)和OS(HR=1.26;95%CI 1.09-1.46;p=0.002)显著相关。
HER2DX风险与年龄分布:HER2DX高风险组与低风险组患者的年龄分布无显著差异,中位年龄分别为74岁和73岁(p=0.20)。
HER2DX风险的预后价值:经年龄校正后,HER2DX风险与生存结局的关系保持稳定。(RFS:全体患者HR=0.57,0.27-1.21;淋巴结阴性患者HR=0.42,0.17-1.03)(OS:全体患者HR=0.42,0.18-0.99;淋巴结阴性患者HR=0.21,0.08-0.56)。
► 生物学特征、TILs与预后价值
生物学特征分析:对HER2DX风险评分包含的增殖、免疫和管腔三个生物学特征进行独立评估,热图(图2A)显示出显著的生物学异质性,各特征间存在适度的两两相关性,包括增殖特征与免疫特征的正相关(r=0.19),以及免疫特征与管腔特征的弱负相关(r=-0.11),支持其存在生物学互补性。
单变量分析:各特征均按预期方向与生存结局相关:高免疫和高管腔特征与较低的复发和死亡风险相关,而高增殖特征则与风险增加相关(图2B)。
复合评分构建:基于三个有利特征(免疫高、管腔高、增殖低)构建0-3分复合评分,结果显示随着分数升高,患者长期生存结局逐步改善,形成明显预后梯度。Kaplan-Meier分析表明,8年RFS和OS率随复合评分增加而逐步提升(图2C、D)。
与传统指标对比:基质TILs与HER2DX免疫特征呈中度相关(Pearson r=0.66;图2E),但在本研究队列中,TILs未显示出与生存结局的显著关联。此外,HER2DX低风险肿瘤中高TILs水平(≥20%)的比例明显高于高风险组(表1)。
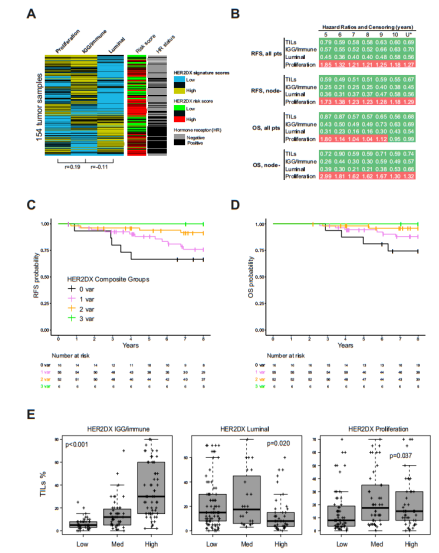
图2 HER2DX各生物学特征及复合评分的预后价值2
A 基于154例肿瘤样本绘制的免疫、管腔和增殖特征百分位数评分热图。
B 三种HER2DX生物学特征与TILs在全体队列及淋巴结阴性亚组中对生存预后的风险比分析。
C-D 基于复合评分的10年无复发生存率与总生存率Kaplan-Meier曲线。
E TILs水平与各HER2DX生物学特征的关联分析箱线图。
► HER2DX风险评分、年龄、激素受体状态与治疗交互作用
HER2DX风险分组与化疗疗效:HER2DX风险分组与治疗组间未观察到统计学显著的交互作用,RFS和OS的交互作用p值分别为0.187和0.392。
其他因素与化疗获益:年龄和激素受体状态均未显示与化疗获益存在显著关联,交互作用分析均无统计学意义。
► HER2DX pCR评分的预后价值及治疗交互作用
根据HER2DX pCR评分,在154例患者中,51.3%为pCR-高分组,21.4%为中分组,27.3%为低分组。pCR评分与RFS或OS均无显著关联。
pCR-高分组:化疗改善RFS呈现非显著趋势(HR=0.44,95%CI 0.14-1.44),化疗+曲妥珠单抗组10年RFS为88.9%,而单用曲妥珠单抗组为61.4%(图3A)。OS同样呈现出数值上的改善(HR=0.23,95%CI 0.05-1.08),10年OS率分别为94.4%和66.4%(图3B)。
pCR-中/低分组:未观察到化疗对RFS(HR=1.18,95%CI 0.45-3.10;10年RFS:化疗+曲妥珠单抗组70.6% vs 单药组76.2%)或OS(HR=1.68,95%CI 0.50-5.60;10年OS:76.2% vs 88.6%)的获益证据(图3C、D)。
交互作用:RFS和OS的交互作用p值分别为0.200和0.045。
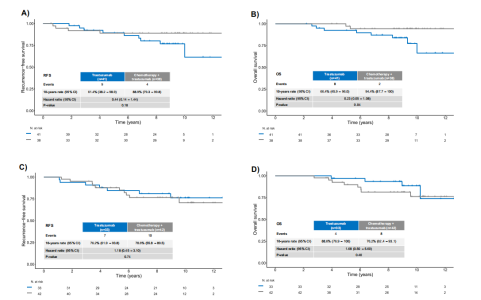
图3 | 按HER2DX pCR可能性评分分层的化疗获益2
A pCR-高评分肿瘤中不同治疗组(曲妥珠单抗单药 vs 曲妥珠单抗+化疗)的无复发生存期Kaplan-Meier曲线。
B pCR-高评分肿瘤中不同治疗组的总生存期Kaplan-Meier曲线。
C pCR-中/低评分肿瘤中不同治疗组的无复发生存期。
D pCR-中/低评分肿瘤中不同治疗组的总生存期。
研究结论
本研究基于RESPECT临床试验的长期随访数据,在70–80岁HER2阳性早期乳腺癌老年患者中评估了HER2DX基因组检测的价值。研究证实,在此人群标准临床病理特征与生存结局无显著关联的背景下,HER2DX风险评分可提供独立的长期预后信息,展现其基因组分层的附加价值。
HER2DX将大多数患者(74.0%)划分为低风险组,该组患者显示出优异的长期生存,尤其在淋巴结阴性亚组中。该评分所依托的免疫、管腔和增殖特征均与生存结局相关。在预测方面,探索性分析提示,HER2DX pCR评分可能识别出能从联合化疗中获得潜在生存获益的亚组(pCR-高),而低风险且pCR-中/低的患者或是考虑治疗降级的患者,对相关结果仍需谨慎解读。综上所述,HER2DX为老年HER2阳性早期乳腺癌提供了重要的预后信息,结合pCR评分,有望为识别化疗获益人群及个体化治疗决策提供参考。
参考文献:
1. Bray F, et al.CA Cancer J Clin. 2024 Apr 4.
2. Nozawa K,et al. Nat Commun. 2025 Nov 4;16(1):9585.
编辑:dana
审校:KIKI
排版:KIKI
执行:KIKI
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)