Document Numeber:7356-CN-2600047

从健康肝脏发展至
O+Y双免疗法则精准靶向这一核心机制,伊匹木单抗通过阻断CTLA-4,不仅可提高效应T细胞数量,还可通过抗体依赖的细胞介导的细胞毒性作用(ADCC)/抗体依赖的细胞吞噬作用(ADCP)效应清除Treg细胞,改善免疫抑制[3];纳武利尤单抗则阻断PD-1通路,恢复效应T细胞对肿瘤的识别与杀伤能力。数量增加的效应T细胞还可分化出更多记忆T细胞,从而保持对肿瘤的长期免疫监视。因此,O+Y双免疗法直击HCC发展核心机制,全面重启肝癌患者免疫开关,实现高效、持久的抗肿瘤效果[4]。

全球多中心、随机、开放标签的III期CheckMate9DW研究共纳入668例未接受过系统治疗的不可切除或晚期HCC患者,按1:1的比例随机分配至O+Y组或
在靶病灶可评估的患者中,O+Y双免疗法展现出快速且强效的缩瘤效果:中位至缓解时间(TTR)仅为2.2个月,客观缓解率(ORR)达36%,约为对照组的3倍。此外,O+Y组中实现深度缓解的患者比例更高,有37%的患者靶病灶缩小一半以上 [5,6]。更值得注意的是,O+Y组患者的中位缓解持续时间(DoR)长达34.3个月,同样接近对照组的3倍[7]。这表明O+Y双免疗法不仅具有优异的短期疗效,且一旦起效,能够持久维持,将ORR转化为长期生存获益。
在总生存期(OS)方面,中位随访52.5个月时,O+Y组中位OS长达近2年(23.7个月 vs 20.6个月,HR=0.78)。2026年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)4年随访数据更新显示,O+Y组4年OS率为31%,意味着超过三成的晚期HCC患者在接受O+Y治疗后能存活超过4年[7]。
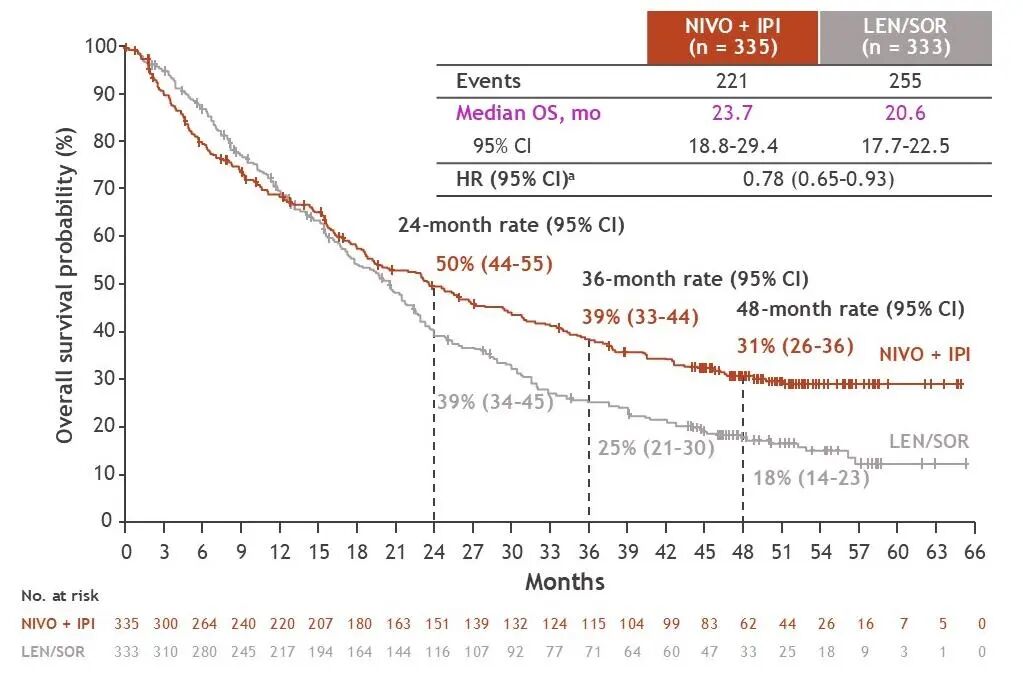
图2 CheckMate 9DW研究OS结果[7]
(引自2026 ASCO GI LBA479)

CheckMate 9DW研究是目前*唯一在Ⅲ期临床试验中同时对比索拉非尼和仑伐替尼两大标准治疗并取得阳性结果的研究。基于该研究数据,O+Y方案于2025年3月正式获批用于中国不可切除或晚期HCC的一线治疗[8],成为目前中国肝癌领域首个获批的双免联合疗法。同时,O+Y方案的显著长生存获益也有望推动肝癌治疗向“慢病化管理”迈进,开启肝癌双免治疗新时代。此次该方案又被纳入《原发性肝癌诊疗指南(2026年版)》,为临床规范化选择全新、高效的治疗方案提供了依据;目前,基于多项III期临床研究,以O+Y为代表的免疫联合方案的疗效显著优于索拉非尼或仑伐替尼单药,已经成为临床实践中的优先选择。
未来,随着真实世界数据的积累、生物标志物的深入探索以及与其他治疗手段的协同优化,双免策略或将进一步拓展至更广泛的患者人群,甚至前移至辅助或新辅助治疗场景,为实现“健康中国2030”癌症防治战略目标贡献重要力量。

图3 原发性肝癌诊疗指南(2026年版)更新总结



*截至2026年4月14日
编辑:Rosewei
审校:Selina
排版:Chipsy
执行:Lya
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。