导语
恶性肿瘤诊疗正在进入精细化管理时代,

破局 “一刀切”,新路径引领DTC术后精准管理
林教授指出,《路径》由中华医学会核医学分会牵头,全国49位来自超声、放射、核医学、内分泌学、外科学等多学科领域专家历时两年余协力完成,旨在规范国内DTC术后评估与患者精细化管理。与2017版《分化型甲状腺癌术后131I治疗临床路径专家共识》1不同的是,《路径》突出了核医学作为DTC术后诊疗管理的平台性作用,强调甲状腺全切或近全切术后DTC患者进入路径评估,强化其术后全程管理,基于动态评估形成包括131I在内的综合诊疗决策。此外,DTC术后管理目前尚缺乏大样本、多中心、前瞻性临床研究及随访时间足够长的回顾性研究,借此呼吁行业同道共同深耕,为 DTC 诊疗规范完善提供更多高质量证据支撑。
DTC独特的生物学特征为放射性
早期DTC术后RAIT决策之困,“刻舟求剑式决策”亟待破局
林教授提到,美国早期ATA指南的DTC风险分层是基于手术瞬间抓拍的TNM分期和复发风险分层3-5;但其权重因子主要基于回顾性研究和碎片化循证证据,往往从单一因素考量风险因子在甲状腺癌预后中的作用,缺乏因果关系推断和多因素权重整合。这样的RAIT决策过程宛如“刻舟求剑”,而在核医学接诊这些病人时,其实已经“轻舟已过万重山”。核医学的诊疗理念和实时评估将在避免此类RAIT决策过程中发挥重要作用。
林教授通过一例典型病例阐述了仅依据DTC复发风险直接决策RAIT的局限性。一位29岁女性患者,术后TNM分期为T4aN1aM0(I期),按复发风险分层属于高危人群,若直接决策治疗可能接受100-150mCi的治疗剂量。但通过实时疗效反应动态评估,血清学显示sTg在1ng/ml以下、TgAb阴性,影像学检查均为阴性,诊断性显像未见明确残余甲状腺组织和甲状腺癌转移征象,患者的治疗决策调整为积极随访、继续TSH抑制治疗,暂不启动RAIT。多项研究也为上述局限性提供了有力的佐证:北京协和医院联合桂林医学院和青医附院的三中心研究显示,在ATA指南中高危风险分层人群中,近50%经RxWBS证实仅为甲状腺残留, 大剂量131I辅助治疗或可避免(图1)6。2018年斯坦福大学的一项回顾性研究发现,如RAIT前依据DxWBS实时评估,49%患者的RAIT剂量将被优化7。提示DTC术后风险分层应该结合实时的动态评估来决策后续治疗,以助力病人精准化的治疗和管理。

图1.北京协和/桂医/青医三中心研究结果
另外,尽管2019年欧美多个学会联合提出了“马提尼克原则”8,该原则意识到术后RAIT前多因素、动态评估的重要性,但并未涉及RAIT决策要害问题:高风险≠RAIT获益,并没有直接解决临床上简单粗暴“算命式”的风险分层来决策RAIT过程。
“核医学诊疗一体化”理念促进DTC的精准评估及全程管理
面对上述痛点,中国临床肿瘤学会甲状腺癌专业委员会率先迈出了理念革新的步伐。2019年国内《分化型甲状腺癌术后131I治疗前评估专家共识》9首次明确RAIT前评估的意义,倡导在DTC术后风险分层(TNM分期、复发风险)基础上进行术后实时评估,基于血清学和影像学两方面,强调核医学诊断性显像在诊疗决策中的助力作用,帮助筛选高危人群以及真正需要RAIT的患者。2025年《CACA指南:甲状腺癌》10进一步强调基于三重风险分层(在TNM分期和复发风险基础上,增加动态疗效评估)决策后续治疗,充分体现"诊疗一体化"理念,同时将患者意愿纳入决策过程。
欧洲核医学协会甲状腺委员会主席Luca教授发表于Cancer的一篇综述指出,术后DxWBS可显著改善DTC患者的风险分层和分期,并指导后续的131I治疗,肯定了“131I诊疗一体化”在DTC术后评估及管理中的价值11。在CACA指南患者宣教过程中,我们也强调131I是优良的诊疗一体化核素,加上rhTSH将助力碘治疗前精准评估及治疗计划制定、甲状腺癌术后及任意时间动态风险评估。多项研究证明,通过DxWBS进行精准评估,有助于避免病灶漏诊,优化RAIT决策(15%患者的风险分层改变12,53%患者的管理方案优化13)。值得关注的是,2025版ATA指南首次提出的 DATA 框架也强调RAIT前后评估与治疗同等重要14。因此,DTC的评估理念已从静态的风险分层向治疗前精准评估以及全程管理演进(图2)。
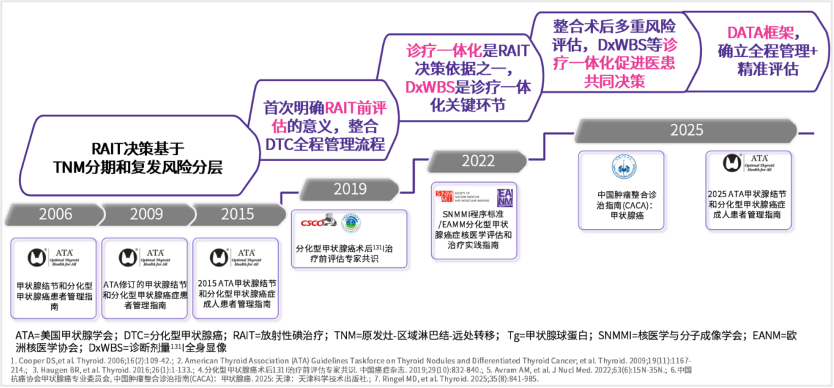
图2.DTC评估理念演进:从片段化监测到全程管理+精准评估
新一代rhTSH赋能DTC术后精准评估及决策
目前,助力RAIT前精细化评估及疗效的两大因素是升高促甲状腺激素(TSH)水平和低碘饮食。既往国内患者升高 TSH 水平的唯一方式,是停用甲状腺激素(至少2 周),叠加低碘饮食与血清学、影像学评估,整个RAIT前准备周期至少需要 3 周,不仅耗时较长,患者还需承受甲减带来的诸多不适。而 rhTSH 可将整个准备周期压缩至1 周内完成,是优选的升高TSH方案。近年来,TSH助力RAIT的历程也在不断优化。1950年代,牛TSH用于临床辅助RAI治疗15;1991年国外学者基于基因重组技术开发了rhTSH16,1998年首个用于DTC随访诊断适应症的rhTSH获批17,开启了rhTSH助力131I诊疗的起点;2026年,#注射用人促甲状腺素β (新一代rhTSH)在国内获批上市18,成为国内目前唯一助力DTC术后精准评估的rhTSH(图3)。
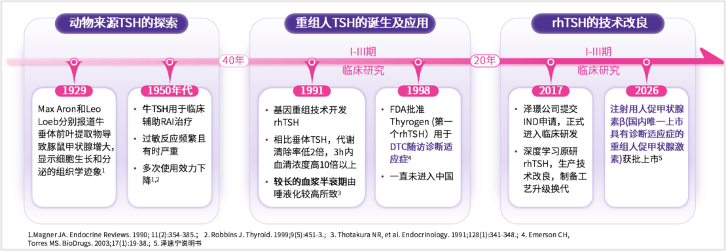
图3.TSH助力RAIT的历程
目前,#注射用人促甲状腺素β 的2期和3期临床研究均已正式见刊。作为该药物全国多中心临床试验的牵头专家,借此对全国 27 家参研中心的付出表示感谢。#注射用人促甲状腺素β 具有起效快、安全性良好、避免甲减症状等多重优势,克服了传统停药法的局限,将助力开启国内DTC术后患者精准评估新篇章。
报告最后,林教授总结道:诊断性碘扫描作为诊疗一体化的范本,随着SPECT/CT的发展、124I/123I显像的应用,其已成为核医学进行NIS靶向临床决策的重要抓手,也正为患者、家属及相关科室同道提供了令人信服的碘治疗依据。因此,诊断性显像的意义在于可结合血清学等其他评估一起为辅助碘治疗决策提供实时影像学依据,而治疗后显像应作为此次碘治疗决策的质控而非仅“马后炮式”诊断价值。可视化决策及质控是核医学医生的利器,我们应充分利用这一可视化探测优势筛选真正的131I适应症人群、预估治疗疗效,而避免仅依据风险分层“猜盲盒”式简单粗暴治疗。升高TSH是助力RAIT前评估及疗效的因素之一,rhTSH是升高TSH的优选方案。#注射用人促甲状腺素β 是国内首个助力推动RAIT精准评估的rhTSH,将助力我国DTC诊疗一体化水平迈上新台阶。
林岩松 教授
北京协和医院(PUMCH) 核医学科 主任医师、教授、博士导师
国际原子能机构(IAEA) RAS6105项目中国区国家协调员
中国医疗保健国际交流促进会甲状腺疾病学分主任委员
中华预防医学会甲状腺疾病防治专业委员会副主任委员
国家癌症中心甲状腺癌质控专家委员会副主任委员
中国医师协会肿瘤医师分会第三届委员会甲状腺癌学组副组长
曾被评为1999年卫生部优秀青年科技人才、第三届国之名医及第七届“敬佑生命-荣耀医者”专科精英。先后六次主持国家自然科学基金,围绕甲状腺领域以第一或通讯作者发表文章180余篇 (SCI 60余篇),单篇最高影响因子 31.7
文献回顾
编辑:Espacelibre
审校:Espacelibre
排版:Checky
执行:Aurora
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)