一

CAA 是涵盖多种临床疾病的总称
临床经验和神经影像学发现表明,CAA 涵盖了几种不同的临床疾病,主要统一于脑血管Aβ沉积这一病理基础:
出血性CAA:常见于卒中单元,其特征是CAA相关的脑叶脑出血(ICH)、短暂性局灶性神经系统发作(TFNE)和凸面
非出血性CAA:常见于神经认知门诊,包括CAA相关性血管性认知障碍和痴呆,或与阿尔茨海默病(AD)重叠。
炎症性CAA:尤其是脑淀粉样血管病相关炎症(CAA-ri)这一自身免疫综合征,以及淀粉样蛋白相关影像学异常(ARIAs)。
这些临床-
关键信息:
CAA不仅仅是与ICH相关的脑血管疾病,还应将其视为神经退行性过程的促成因素,并在某些情况下作为一种自身炎症性疾病。
二

CAA是老年大脑中常见的病理改变
CAA在老年人中非常普遍。尸检研究显示,超过50%的脑叶ICH患者存在中度至重度的CAA病理改变。CAA病理改变几乎总是见于AD(约80%),通常为轻度形式;约一半的AD患者表现出中度至重度的CAA。在基于人群的尸检研究中,约40%的老年人存在一定程度的CAA,其中约25%存在中度至重度受累。因此,在老年人因
关键信息:
与症状性CAA相比,偶发性或无症状性CAA的临床相关性通常不确定。
临床要点:
将“CAA”用作临床诊断名称时,应保留用于表示中度至重度 CAA 病理负荷高度可能引发相关症状,这与波士顿标准2.0版中“probable CAA ”类别相一致(本文中均使用此版本)。
三

CAA 的病理生理学仍未完全阐明
CAA发生和发展的分子驱动因素尚未完全阐明。三种神经病理生理学途径在起作用:(1)血管Aβ聚集,(2)血管脆性伴出血,(3)神经炎症。所有形式CAA的核心是Aβ在软脑膜和大脑/小脑皮质的小动脉、微动脉和毛细血管中进行性沉积,主要由血管周围(类淋巴)清除受损驱动。慢性淀粉样蛋白沉积诱导血管平滑肌细胞变性和血管生理功能受损,最终导致非出血性
关键信息:
CAA 患者会因血管壁破裂而进展为脑叶/浅表出血性损伤。
向出血表型的转变可能涉及血管破裂途径激活、神经炎症反应和随机因素(如血压升高)的多步骤过程。
四

CAA 的诊断主要依赖于 MRI(波士顿标准2.0版)
对于年龄≥50岁、出现脑叶脑出血、短暂性局灶性神经系统发作、凸面蛛网膜下腔出血或认知功能下降的患者,临床上应怀疑CAA。波士顿标准为CAA的临床-影像学诊断提供了重要框架,通过验证"可能CAA"与中重度CAA病理改变相比具有良好的诊断准确性(图)。2022年更新的波士顿标准2.0版细化了脑叶/浅表出血标志物的评估,并纳入了特征性白质改变,在医院队列中实现了74.5%的敏感性(95%CI,65.4%-82.7%)和95.0%的特异性(95%CI,83.1%-99.4%)。在无显明显出血表现的记忆门诊患者中,该标准的灵敏度仍然有限(漏诊率较高)。
临床-影像学要点:
为获得最佳诊断准确性,建议使用3T磁共振成像结合磁敏感加权成像技术,以最大限度检测细微的出血性病变。
如何处理混合性脑叶和深部出血性病变的患者:
根据波士顿标准,当存在任何深部出血性病变(如深部CMB/ICH)时,不能诊断为"可能CAA"。对于混合性出血(脑叶和深部)的患者,存在皮质表面铁沉积症 (cSS),尤其是多灶性时,强烈提示存在潜在的晚期软脑膜 CAA,即使不符合正式的"可能CAA"标准。
临床要点:
对于无法进行MRI的脑叶ICH患者,基于CT的简化爱丁堡标准可用于 CAA 诊断,其依据是存在指状突起和 cSAH 延伸。
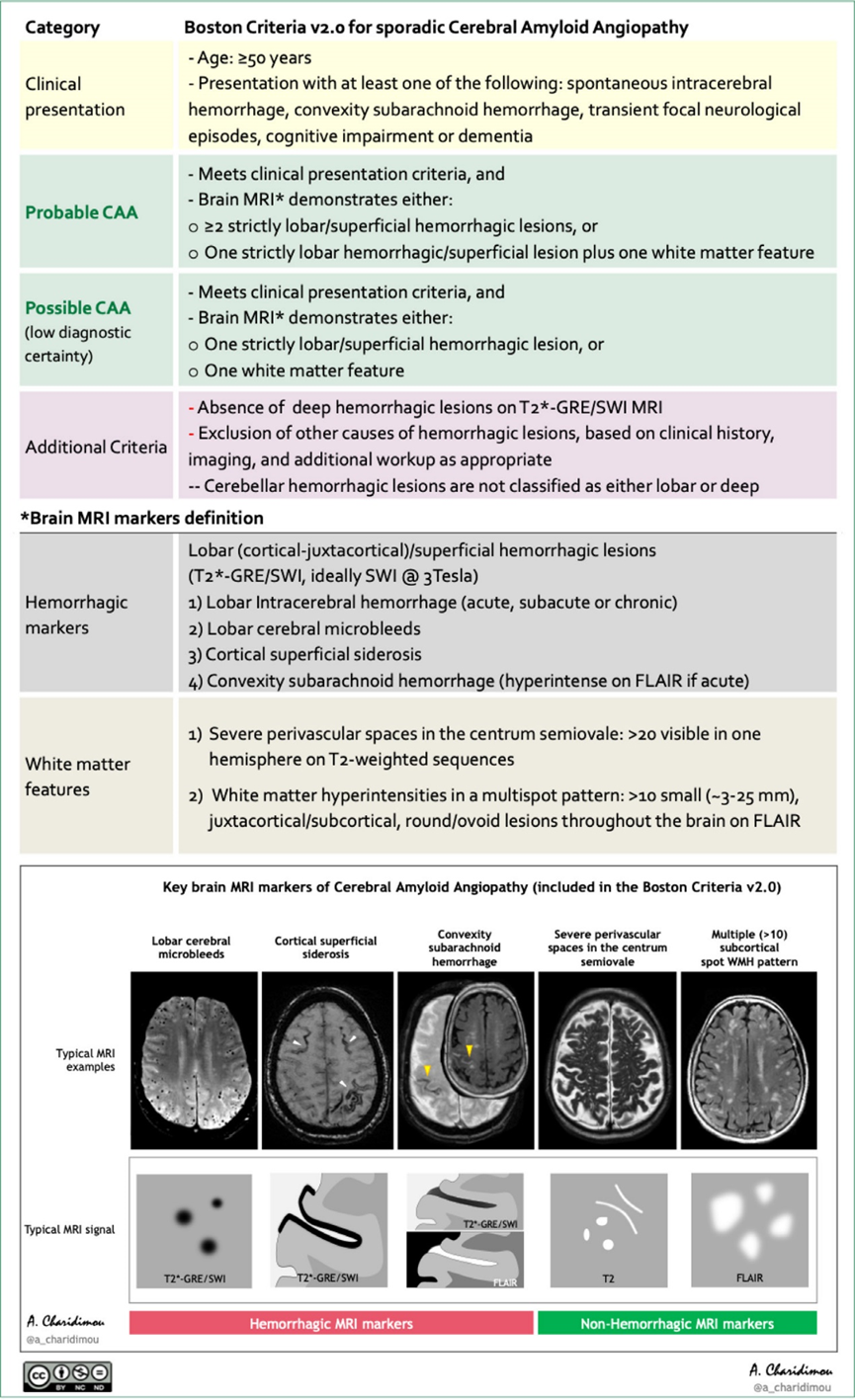
图. CAA诊断的临床MRI框架(上:波士顿标准2.0版的CAA诊断框架;下:CAA的关键MRI生物标志物)
五

对不确定CAA病例进行辅助诊断检查
在无法应用或不符合波士顿标准2.0版的情况下,如年轻患者(<50岁)有相关神经外科病史,或可能存在竞争性病因时,额外的检查可能提高诊断确定性。这种方法仅应在提高诊断确定性确实会影响关键临床决策(如启动或停用抗凝治疗)时使用。
临床要点:
6-12个月后的随访MRI(理想情况下使用3T磁共振及磁敏感加权成像)可通过观察期间新出现的脑叶CMB或cSS的来明确CAA的诊断。作者认为这种策略是一种强有力的诊断辅助手段,出血会显露真相。
如何使用其他诊断辅助手段:
脑脊液分析:在无认知障碍的疑似CAA中可能有信息价值:孤立的脑脊液Aβ42和Aβ40降低(无p-tau升高)支持潜在的CAA。
淀粉样蛋白正电子发射断层扫描:诊断上受限,因为放射性配体无法区分脑血管与实质Aβ沉积。阴性淀粉样蛋白正电子发射断层扫描可能排除晚期CAA。
载脂蛋白E基因分型:无标准化临床作用,尽管APOE ε2和ε4等位基因会增加CAA的预检概率。
六

淀粉样蛋白发作带来麻烦
与CAA相关的短暂性局灶性神经系统发作(TFNE)表现为短暂、反复发作的局灶性神经功能异常,其特征是刻板的运动、躯体感觉、视觉或其他皮质症状。这些发作最可能反映异常的皮质活动,通常是对小的浅表CAA出血(急性cSAH)的反应,由受晚期CAA影响的软脑膜小动脉破裂引起。正确识别CAA相关TFNE至关重要:它们与cSS/cSAH的密切关联显著增加了后续颅内出血的风险。识别CAA相关TFNE并通过临床判断和适当的神经影像学将其与TIA区分开来,对于避免不适当的抗血栓治疗至关重要。
临床要点:
CAA相关性TFNE是CAA最具挑战性的表现之一,除非临床医生能够主动加以考虑,否则难以诊断。只有通过血液敏感的MRI序列才能确立诊断,并且应被视作所有出现新症状(提示TFNE)的老年患者(年龄>50 岁)均需考虑的一项检查。
如何区分CAA相关TFNE与TIA:
与TIA不同,CAA相关TFNE往往表现为阳性症状在数分钟内沿着相邻皮质区域扩散进展,持续时间通常不超过30分钟,且具有高度刻板性和多发性。这些是应在老年患者中引起警惕的CAA相关性TFNE的显著临床特征。此外,也可能出现阴性症状。
症状管理要点:
虽然通常是自限性的,但在特定患者中,某些具有偏头痛预防特性的抗癫痫药物,如左乙拉西坦、托吡酯或拉莫三嗪,可能减少发作频率。
额外临床要点:
局灶性神经炎症活动,有时可通过短暂的软脑膜血管壁增强可见,可能导致延长或持续的TFNE,因此应考虑潜在的CAA-ri。
七

ICH风险通过临床和MRI CAA表型进行分层
"可能CAA(probable CAA)"的诊断并不一概意味着高ICH风险,因为这一风险在不同患者间存在显著差异,具体取决于临床及MRI表型标志物。表现为出血性CAA表型的患者基线风险最高:CAA相关脑叶ICH患者的年度复发率约为7.4%(95%CI,3.2%-11.6%);表现为CAA相关cSAH的患者则面临更高的年出血风险,约21.4%(95%CI,16.7%-26.9%)。在非出血性或偶发CAA中,未来ICH风险则要低得多。
在临床实践中,可使用以下方法对未来出血风险进行分层:
症状性出血性卒中病史(脑叶ICH、多发性ICH和cSAH):确定出血性CAA的背景,是基线风险分层因素。
cSS的存在和多灶性:未来CAA相关出血的最强影像学预测因素,即"确凿证据"。播散性cSS(累及≥4个脑沟)使未来ICH风险增加4.28倍(95%CI,2.91-6.30),而局灶性cSS增加2.11倍(95%CI,1.31-2.41)。
脑叶CMB:虽然有助于支持"可能CAA"诊断,因此与无CAA患者相比基线风险升高,但单独而言,它们对增量出血风险的贡献很小。许多广泛脑叶CMB的患者从未出血。
管理提示:
严格的血压控制(目标≤130/80 mmHg)仍然是唯一被证实可降低所有 CAA 表型未来出血并发症的策略。
八

CAA合并房颤患者的卒中预防必须个体化
上述ICH风险分层方法直接指导可能CAA合并房颤患者心源性卒中预防与ICH风险之间的平衡。在等待临床试验结果的同时,一些指导原则是有帮助的。首先,应根据CHA₂DS₂-VASc 评分和患者特征评估主要缺血性血管事件的风险。
操作方法:在高危房颤(CHA₂DS₂-VASc ≥2)患者中
对于出血风险相对较低的可能CAA患者(无既往症状性ICH或cSAH,且无播散性/多灶性cSS),可考虑直接口服抗凝药。
对于高危可能 CAA(如多发性CAA相关性脑叶ICH、症状性cSAH、播散性/多灶性/cSS和血压未控制)患者,应避免抗凝治疗。左心耳封堵是可考虑的选择。虽然缺乏专门针对CAA人群的随机试验数据,但最近的手术改进和更短、强度更低的术后抗血栓方案使左心耳封堵成为越来越有吸引力的替代方案。
对于中等风险可能CAA患者(即无cSS 的单次脑叶 ICH),可考虑直接口服抗凝药或左心耳封堵术。
对于偶发性CAA患者,如在缺血性卒中/TIA检查中发现少数脑叶微出血,通常可应用标准抗凝策略。
九

CAA-ri是一种可治疗的CAA亚型
偶尔,受散发性CAA影响的血管中的Aβ沉积会引发自身炎症反应,导致CAA-ri谱系疾病,其具有独特的临床、影像学和神经病理学特征。临床上,CAA-ri通常表现为急性或亚急性认知功能下降、人格改变、意识模糊、意识状态改变、癫痫发作或持续性新发头痛,这些症状更提示炎症而非出血。急性局灶性神经功能缺损和偶尔的TFNE也会发生。在 MRI 上,CAA-ri的特征通常是大量皮质和皮质下 CMB,较少见的cSS/cSAH,影响皮质下白质的显著血管源性水肿,以及脑沟积液。
影像学诊断要点:
出血性病变与血管源性水肿区域或邻近区域共定位时,应高度怀疑CAA-ri。
关键信息:
快速诊断并启动免疫抑制治疗(通常是皮质类固醇,有时联合其他免疫抑制剂)对于改善预后至关重要。
十

ARIA=医源性CAA-ri
CAA似乎是早期AD淀粉样蛋白靶向治疗期间脑血管炎症并发症(称为ARIA)的主要驱动因素,推测是通过为抗体介导的攻击富含淀粉样蛋白 β 的血管提供靶点,并损害血管周围淀粉样蛋白清除。ARIA与CAA-ri在MRI、临床和神经病理学上具有惊人的相似性。两者在脑部MRI上看起来几乎相同(具有特征性血管源性水肿和浅表出血),均与APOE ε4相关,并在组织病理学上表现出针对血管淀粉样蛋白的炎症反应。
关键信息:
ARIA可被视为CAA-ri的医源性变异型,由Aβ抗体触发。患有早期 AD 且伴有ICH、> 4 个 CMB 或任何 cSS 的患者应排除在治疗之外。
总结
CAA相关临床综合征和MRI表现的完整谱系仍在不断演变,凸显了采用结构化、概念驱动方法的必要性。笔者建议将这10个核心概念作为实用基础,用以解答CAA患者日常诊疗中遇到的多样且细微复杂的问题。
文章来源:Charidimou A. 10 Things You Should Know About Cerebral Amyloid Angiopathy. Stroke. 2026 Feb;57(2):e69-e74. Epub 2026 Jan 26. PMID: 41587285.

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)