
2026年1月7日,中国国家药品监督管理局(NMPA)官网信息显示,由恒瑞医药自主研发的新药瑞拉芙普α注射液(商品名:
瑞拉芙普α注射液是全球首个PD-L1/TGF-βRII双抗领域临床获批的“First in Class”新药,同时抑制PD-L1/TGF-β通路,协同作用于肿瘤免疫治疗的多个环节。在晚期
图1 国家药监局批准瑞拉芙普α注射液上市(图片来源于2026年1月7日中国国家药品监督管理局官网:https://www.nmpa.gov.cn/zhuanti/cxylqx/cxypxx/20260107172725161.html)
抗PD-L1/TGF-βRII双特异性抗体融合蛋白独特结构设计,双靶协同、强效抑瘤
全球胃癌年新发病例近百万,死亡病例逾65.5万例2。而且我国晚期胃癌患者占比高,预后不佳,疾病诊疗形势更为严峻3。免疫治疗是当前晚期胃癌一线标准治疗措施之一,然而目前免疫单抗治疗对于患者长期生存改善有限,尤其在胃癌肝转移等难治性人群中表现不佳,患者亟待革新治疗方案以改善预后。
瑞拉芙普α注射液是恒瑞自主研发的抗PD-L1/TGF-βRII双特异性抗体融合蛋白,将TGF-β通路抑制与免疫检查点阻断相结合,成为突破免疫屏障、提升免疫治疗响应的重要突破口。瑞拉芙普α注射液同时具备优化改造的PD-L1抗体端与N端截短的TGF-βRII端,能够在阻断PD-L1信号,解除免疫刹车的同时,保持对TGF-β的高倍亲和力,改善免疫抑制微环境,双靶协同,提升免疫治疗效果。这种独特的创新结构与作用机制,为后续临床获益奠定深厚根基。
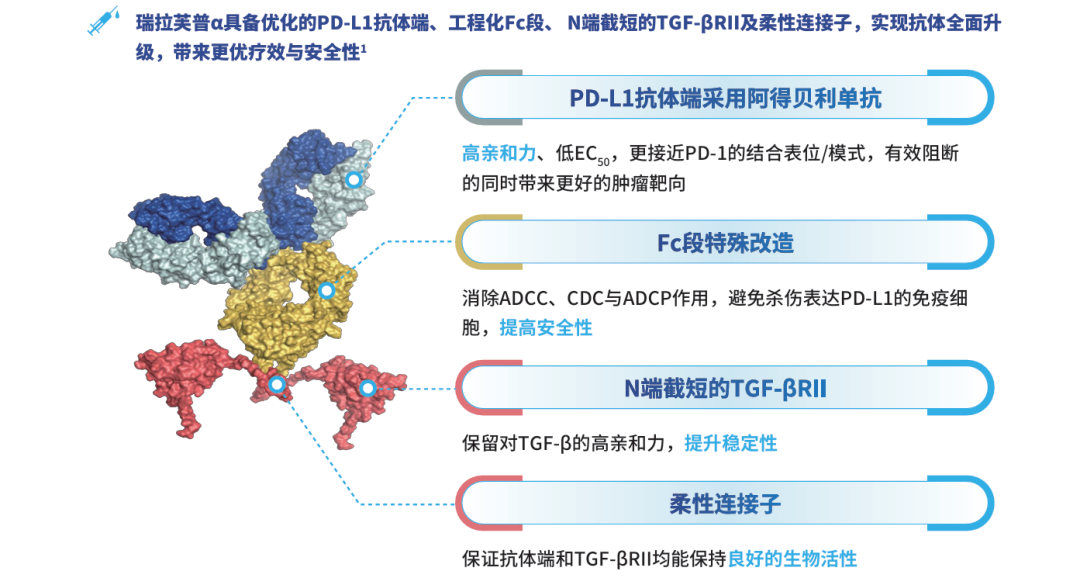
图2 瑞拉芙普α注射液的分子结构特点
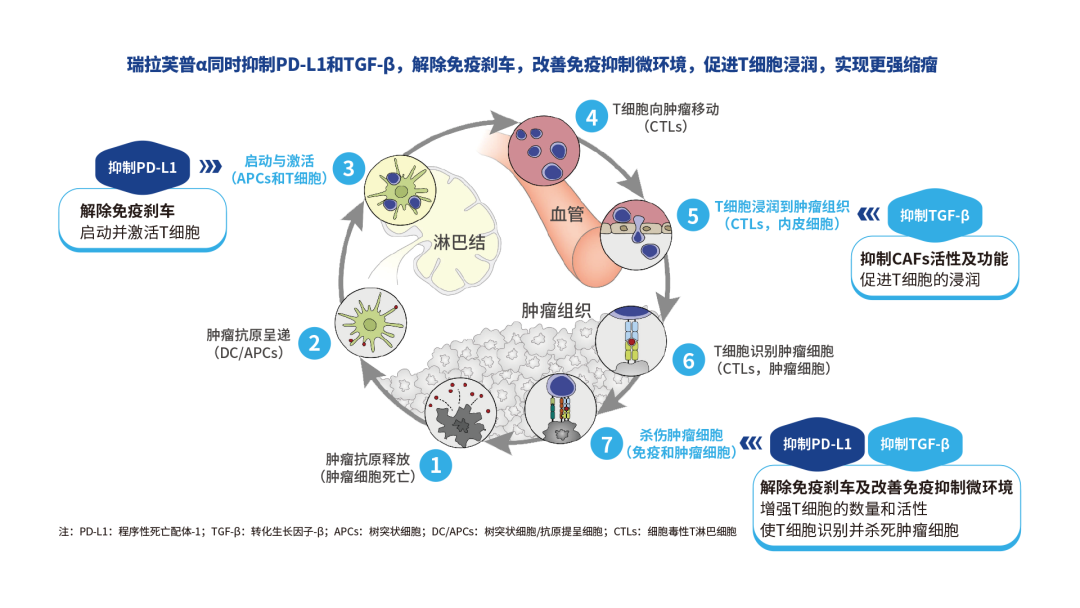
图3 瑞拉芙普α注射液的作用机制
瑞拉芙普α优效守护晚期胃癌患者生存,助力二代免疫新征程
本次获批上市是基于RELIGHT研究(原研究名称为SHR-1701-Ⅲ-307研究)取得的优异成果。RELIGHT研究是一项随机、双盲、多中心的Ⅲ期研究,旨在评估GC/GEJC患者中瑞拉芙普α注射液联合化疗对比安慰剂联合化疗的有效性和安全性。2024年ESMO年会上报道的主要疗效数据结果令人振奋,瑞拉芙普α注射液联合化疗显著改善晚期胃癌患者生存:在意向性治疗(ITT)人群中,瑞拉芙普α注射液联合化疗组的中位OS(mOS)为15.8个月,较对照组安慰剂联合化疗延长了4.6个月,死亡风险降低34%(HR=0.66)4。2025年ESMO Asia大会进一步披露了PD-L1 CPS≥1亚组分析结果,瑞拉芙普α注射液联合化疗的mOS高达16.7个月,较对照组安慰剂联合化疗提升6.4个月,死亡风险降低43%(HR=0.57)5。瑞拉芙普α注射液联合化疗凭借其独特的双靶点机制成功突破传统单抗疗法的疗效瓶颈。Meta分析显示,瑞拉芙普α注射液相较其他各项免疫治疗方案在PD-L1 CPS≥1晚期胃癌患者中展现出更优的OS获益趋势6。
另外,特别值得关注的是,在胃癌肝转移这一难治性人群中,瑞拉芙普α注射液同样展现了其优异疗效:mOS达16.8个月,较对照组安慰剂联合化疗提升6.5个月,HR达0.46,降低死亡风险54%,助力胃癌肝转移患者获得长生存获益,有望成为胃癌肝转移患者的首选免疫方案7。
在取得优异疗效的同时,瑞拉芙普α注射液展现出良好且独特的安全性特征。在ITT人群中,其≥3级治疗相关不良事件(TRAE)、严重TRAE及导致停药TRAE等关键安全性指标均无显著差异4。同时,2025年ASCO GI大会公布的数据显示,在ITT人群中,瑞拉芙普α注射液是首个在Ⅲ期研究中观察到可改善化疗所致血液学毒性(血小板、中性粒细胞、白细胞计数降低)的免疫药物,较对照组血液学毒性发生减少约10%,展现出潜在的骨髓保护作用,有望保障化疗足量足周期进行,保障患者的疗效获益8。
胃癌防治任重道远,双抗疗法引领免疫精准治疗新篇
2025 CSCO胃癌诊疗指南、NCCN胃癌诊疗指南均基于HER2阴性晚期胃癌患者的PD-L1 CPS表达水平,对免疫检查点抑制剂的应用作分层推荐,同时NCCN指南还强调免疫治疗应精准锚定PD-L1 CPS≥1人群,推进免疫“精准”治疗9,10。然而,受限于肿瘤微环境(TME)中的多重免疫逃逸机制,当前单抗疗效仍存在瓶颈,原发或继发性耐药普遍存在。在此背景下,研发同时靶向其他信号通路的双抗能够突破抗PD-1/PD-L1单抗的疗效局限。
2024年,FDA肿瘤药物咨询委员会(ODAC)投票裁定,免疫检查点抑制剂在PD-L1 CPS<1人群中获益有限,“获益人群筛选”已成为提升免疫治疗获益的国际共识,瑞拉芙普α注射液的获批正是这一理念的实践印证,同时标志着我国在胃癌免疫精准治疗领域和创新药物研发领域的里程碑突破。
瑞拉芙普α注射液的上市标志着第二代免疫治疗在胃癌领域迈出关键一步,领航胃癌免疫治疗新时代。相较于传统免疫单抗,瑞拉芙普α注射液同时抑制PD-L1/TGF-β双通路,在二代免疫协同增效的基础上优化分子结构,实现了疗效与安全性的双重提升,有望成为PD-L1 CPS≥1晚期胃癌患者的一线免疫优选方案以及晚期胃癌肝转移患者的一线首选方案,为更多晚期胃癌患者带来长生存希望。
参考文献:
审批编号:TG - 肿瘤-胃肠食管SHR-1701: PD-L1/TGF-βRII - 1387 - 2028-11
撰写:Astra
审校:Amaia、Babel
排版:Leo
执行:Squid
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
