

1肝纤维化的病理机制
肝纤维化的中医学病因病机主要基于脏腑功能失调、气血津液运行失常和病理产物积聚的理论。虽然“肝纤维化”是现代医学概念,但根据其临床表现,如胁痛、腹胀、乏力、
肝纤维化是由多种病因诱导肝损伤引发ECM病理性沉积的复杂过程。生理状态下,HSC定位于肝窦周隙,维持静息表型。当受到炎症因子或氧化应激等损伤信号刺激时,HSC活化并分化为肌成纤维细胞,其特征性标志为表达α-平滑肌肌动蛋白(α-SMA)。活化后的HSC在损伤部位异常增殖、迁移,并大量分泌Ⅰ型及Ⅲ型胶原等ECM组分,从而驱动肝纤维化进程。在此过程中,TGF-β作为HSC活化的核心调控因子,通过介导Smad3磷酸化上调胶原基因表达,被公认为强效的促纤维化细胞因子。
代谢重编程是指细胞为适应特定环境或应激状态,以满足能量、物质和信号需求进而重新分配代谢路径。研究表明,代谢重编程在慢性炎症和纤维化过程中发挥重要作用。肝巨噬细胞和HSC作为关键的两种效应细胞,在活化过程中表现出显著的代谢重编程,包括糖酵解增强、脂质代谢改变和
肝纤维化的发生、发展涉及多条关键信号通路的协同调控,包括TGF-β/Smad、Wnt/β-catenin及PI3K/Akt等。这些信号通路通过激活或抑制下游效应因子,驱动HSC活化,继而促进肝纤维化进程。TGF-β/Smad信号通路作为核心促纤维化途径,通过以下机制发挥主导作用:(1)诱导肌成纤维细胞增殖与分化;(2)抑制ECM降解(如上调金属蛋白酶抑制剂表达)。该信号通路是当前肝纤维化研究中机制较为明确、与病理进程高度相关的调控轴。TGF-β通过结合细胞膜上的TGF-β受体,促使Smad2/3磷酸化,并与Smad4形成复合物入核,启动胶原基因转录,诱导胶原蛋白、纤连蛋白合成。TGF-β还可通过抑制金属蛋白酶,上调金属蛋白酶抑制剂,使ECM降解受阻。Wnt/β-catenin信号通路是调控许多肝脏疾病的关键信号通路之一,可通过调控炎症反应、细胞凋亡、氧化应激干预肝纤维化的进程。Wnt配体通过结合Frizzled受体,促进β-catenin蓄积入核,从而激活靶基因,同时与TGF-β协同增强胶原沉积。PI3K/Akt信号通路是肝纤维化发病的关键信号通路,在调节HSC活化与凋亡、肝脏炎症反应、氧化应激、自噬等机制中发挥核心作用。PI3K主要由催化亚基p110、调节亚基p85构成,当细胞受到生长因子、细胞因子等因素刺激时,p110与p85结合的酶活性抑制被解除,p110促进PIP2(磷脂酰

2中药抗肝纤维化的核心作用机制
HSC的持续活化及ECM过度沉积是肝纤维化向肝硬化发展的核心病理环节。现代医学研究表明,受损肝细胞、肝窦内皮细胞(LSEC)及肝巨噬细胞释放的旁分泌信号直接驱动HSC活化;活化的HSC是肝纤维化/肝硬化阶段ECM的主要产生细胞;HSC分化为肌成纤维细胞,分泌大量促炎因子、促纤维化细胞因子及ECM,直接促进肝纤维化进程。因此,靶向抑制HSC活化与增殖成为抗肝纤维化的关键治疗策略。上海中医药大学团队通过体内外实验证实,扶正化瘀方可显著下调α-SMA表达,其抗纤维化机制涉及多靶点调控,包括调节过氧化物酶体增殖物激活受体γ(PPAR-γ)、CYP4A12(细胞色素P450 4A12)等蛋白,干预TGF-β1/Smad、EGFR信号通路,增强自然杀伤细胞(NK细胞)杀伤功能等。此外,Shao等发现加味桃核承气汤可通过抑制巨噬细胞中Notch信号通路表达,诱导巨噬细胞代谢重编程,进而阻断HSC活化。
慢性炎症是驱动肝纤维化进程的核心因素。肝脏受损时,中性粒细胞被募集至损伤部位清除凋亡肝细胞,同时释放强效促炎介质;受损肝组织产生的炎性因子进一步加剧肝细胞损伤。这种持续存在的“损伤-修复”循环导致结缔组织异常增生,最终进展为肝纤维化乃至肝硬化。研究发现,金银花-连翘药对通过抑制环氧化酶-2阻断前列腺素E2合成,下调促炎因子表达,显著逆转CCl4诱导的肝纤维化。软肝颗粒是一种常见的抗纤维化中成药,由枳壳、茯苓等组成,具有补虚清热、活血化瘀的功效,其通过抑制PI3K/Akt通路活化,调控嘧啶代谢紊乱,改善线粒体动力学,减轻氧化应激与炎症反应,从而减轻肝纤维化。加味柴胡当归汤具有气血双补、养阴柔肝的作用,能够降低血清TNF-α、IL-6、IL-1β水平及肝组织α-SMA、Ⅰ型胶原表达,双重抑制HSC活化与胶原沉积,延缓肝纤维化的进展。
在重度氧化应激微环境下,衰老肝细胞通过旁分泌作用激活HSC,并上调促纤维化分子表达,加速纤维化级联反应。因此,抗氧化和自由基清除是逆转肝纤维化的重要机制。红树莓因其富含生物活性成分,被证实可减弱氧化应激。其提取物能够协同调控以下通路:(1)调节Nrf2/HO-1信号通路,增强细胞抗氧化能力;(2)调节PPAR-γ通路,改善氧化应激相关代谢紊乱;(3)调节Caspase/PARP信号通路,抑制氧化损伤诱导的细胞凋亡。上述机制共同作用,显著降低蛋白质羰基化水平,减轻氧化应激介导的HSC活化。泽泻汤通过抗氧化应激,降低血清活性氧、丙二醛和
特定细胞因子(如TGF-β、IL、TNF-α、PDGF)通过与细胞表面受体结合激活胞内信号级联反应,调控靶基因表达以发挥生物学效应,其中TGF-β作为强效促肝纤维化因子,已成为关键治疗靶标。研究表明,天然活性物质可通过靶向TGF-β网络发挥抗纤维化作用。例如,越橘花青素能显著减轻CCl4诱导的大鼠肝纤维化,其核心机制在于促进肝实质细胞增殖并抑制TGF-β/Smad/ERK通路基因转录,从而减少胶原沉积;辣椒素(香草胺与支链脂肪酸缩合物)作为红辣椒主要活性成分,通过靶向免疫细胞Notch受体抑制M1型巨噬细胞极化,降低TNF-α分泌;柴胡皂苷D通过降低血清ALT/AST水平、抑制TNF-α/IL-1β/IL-18等促纤维化因子表达,实现肝保护与纤维化缓解。上述发现证实,靶向TGF-β及其协同信号网络(如Notch信号通路)可为肝纤维化治疗提供新策略。
ECM是由胶原蛋白、弹性蛋白、糖蛋白及蛋白多糖构成的三维动态网络,其内嵌多种生长因子与基质降解酶(如基质金属蛋白酶)。通过抑制ECM过度合成或增强其降解效率,可显著逆转肝纤维化病理进程。李茜团队研究表明,柔肝方通过显著下调肝纤维化小鼠模型中α-SMA、Ⅰ型胶原、TGF-β1及纤维化相关蛋白表达,抑制HSC活化并减少胶原沉积,其机制与调控纤维化蛋白网络密切相关;进一步研究发现,柔肝方中的丹酚酸B可作为核心活性成分,通过阻断HSC转分化、抑制活化标志物表达及胶原异常沉积发挥抗肝纤维化作用。
TGF-β1/Smad信号通路及其调控蛋白网络在肝纤维化进程中发挥核心驱动作用,其中,TGF-β1通过激活下游磷酸化Smad2/3(p-Smad2/3)直接促进纤维化发展。中药抗纤维化研究证实,多种活性成分可靶向该通路抑制HSC活化与ECM沉积,典型代表包括:
在肝纤维化进程中,Wnt/β-catenin信号通路通过调控炎症反应、细胞凋亡及氧化应激等机制发挥核心作用。基于肝纤维化虚实夹杂的中医病因病机,中药以补虚、解毒、化瘀和标本兼治等治法多靶点、多层次调节Wnt/β-catenin信号通路,从而发挥肝保护作用。孙旭等研究表明,膈下逐瘀汤可显著改善CCl4诱导的肝纤维化小鼠的病理损伤(包括肝细胞坏死、脂肪变性及纤维沉积),其抗纤维化机制与抑制Wnt/β-catenin信号通路的活化有关,具体表现为该方剂可同步下调肝组织中Wnt-1和β-catenin的mRNA转录水平及其蛋白表达。双术抗纤方具有健脾益气、疏肝散结、活血化瘀的功效,可降低肝纤维化大鼠的血清标志物Ⅳ型胶原蛋白、Ⅲ型前胶原、透明质酸、层粘连蛋白水平,减少肝细胞坏死及炎症细胞浸润,减轻肝损伤和肝纤维化程度,其机制可能与抑制Wnt/β-catenin信号通路及上调PPAR-γ表达有关。薯蓣皂苷是多种中药的类固醇皂苷提取物,薯蓣皂苷可通过抑制Wnt/β-catenin信号通路,减轻CCl4诱导的大鼠肝纤维化损伤。
PI3K/Akt信号通路通过介导HSC活化、抑制细胞凋亡、增强炎症反应、加剧氧化应激以及引起自噬失调等多种机制,成为推动肝纤维化进程的关键驱动因素。中药有效成分及复方可通过靶向PI3K/Akt信号通路减轻肝纤维化甚至逆转纤维化。血府逐瘀汤是活血化瘀的经典方剂,具有疏肝理气、活血化瘀的功效,能够改善小鼠肝纤维化,降低肝组织羟脯氨酸含量和Ⅰ型、Ⅲ型胶原蛋白及α⁃SMA表达,减轻肝脏炎症,并下调肝脏组织中PI3K、AKT1、mTOR、HIF⁃1α(缺氧诱导因子-1α)mRNA水平,其机制可能与调控PI3K-AKT1-mTOR/HIF⁃1α通路有关。红花作为传统中药材,其活血通经、散瘀止痛之功效已为临床熟知。近年的研究进一步揭示,其有效成分红花总黄酮具有明确抗肝纤维化作用,可同时下调肝组织及HSC-T6细胞中p-PI3K、PI3K、p-Akt、Akt的蛋白表达量。该结果提示,红花总黄酮通过抑制PI3K/Akt信号通路的激活,进而发挥抗肝纤维化的生物学效应。扶正化纤方由人参、丹参等组成,对改善肝纤维化疗效确切,其作用机制可能是通过PI3K/Akt/BAD信号通路调控下游Bcl-2、Bax蛋白表达,促进活化HSC凋亡,减少ECM及胶原纤维合成,从而改善CCl4诱导的肝纤维化小鼠肝内纤维间质沉积。
肠-肝轴理论的深化揭示了肠道菌群在肝纤维化进程中的核心作用:肠道微生物及其代谢产物(如内毒素、次级胆汁酸)经门静脉系统迁移至肝脏,调控免疫细胞功能;而肝脏通过胆汁酸肠肝循环反向构建菌群结构,形成双向对话网络。研究发现,口服中药复方(大黄䗪虫丸、当归芍药散等)可通过修复肠道屏障、重塑菌群多样性及调节胆汁酸代谢减轻肝纤维化。未来需通过粪菌移植等技术验证菌群介导效应,并基于肠-肝-免疫轴深入解析菌群扰动影响肝脏炎症及免疫稳态的分子机制(如TLR4/NF-κB信号传导)。
在肝纤维化进程中,ECM于Disse间隙的异常沉积导致LSEC发生毛细血管化,表现为连续性基底膜形成与窗孔结构消失,从而阻碍肝细胞与血液间的物质交换。值得注意的是,LSEC毛细血管化是肝损伤的早期事件,其发生先于HSC活化及纤维化形成。研究表明,中药可通过靶向抑制促血管生成通路[如VEGF(血管内皮生长因子)信号级联与Notch信号通路]逆转此病理改变。未来研究可结合活体显微成像技术(如双光子显微镜、光片荧光显微术),实现对中药干预下肝窦微循环动态修复过程的在体可视化观测。从马缨丹中提取的毛蕊花糖苷能够逆转LSEC的衰老进程,修复肝窦网络结构,并改善肝窦充血、空泡化、肝细胞坏死及氧化应激等病理改变。其作用机制是通过靶向调控HMGB1-TLR3/4-IRF1信号通路,从而有效防治肝脏缺血再灌注损伤,为新型治疗药物的研发提供了潜在靶点。清毒调肝方由柴胡、黄芩等组成,可减轻肝损伤,改善肝功能,提升免疫水平,干预LSEC去窗孔化和内皮下基底膜沉积,下调层粘连蛋白、Ⅳ型胶原蛋白、血小板内皮细胞黏附分子1(又称CD31)、血管性血友病因子和VEGF mRNA表达,从而抑制血管生成,改善肝窦毛细血管化,减少肝纤维化发生。芪甲柔肝方及其拆方均能够改善肝纤维化大鼠肝功能,减轻病理损伤,抑制HSC活化,减轻肝纤维化及肝窦毛细血管化,其机制与调控VEGF/SRF/c-FOS信号通路有关。

3总结与展望
中药抗肝纤维化机制研究已取得显著进展,其核心优势在于多靶点、多途径的整体调节作用(图1)。现有研究证实,中药可通过抑制HSC活化、调控炎症免疫反应、拮抗氧化应激、调节促纤维化因子及ECM代谢平衡,有效延缓肝纤维化进程。此外,中药复方能靶向关键信号通路,并通过调节肠道菌群、改善肝窦毛细血管化等途径协同发挥疗效。未来研究需突破以下局限:(1)深化机制解析,明确复方活性成分及多通路协同作用网络;(2)探索新兴靶点,如肠-肝轴、代谢重编程;(3)结合中西医理论,基于辨证分型开发精准方药;(4)加强临床转化,开展多中心随机对照试验验证疗效。通过整合现代技术,如类器官模型、单细胞测序,有望推动抗肝纤维化中药新药的研发与应用。
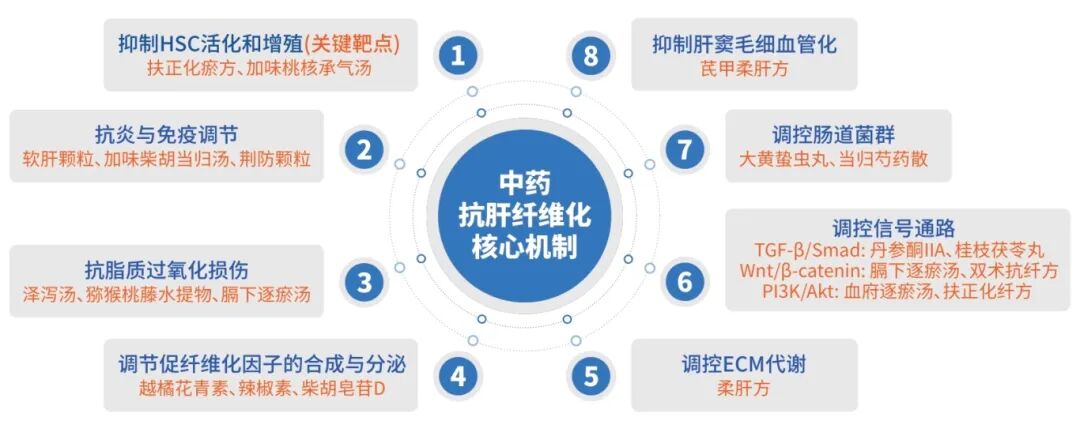
图1 中药抗肝纤维化核心机制

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH251004

潘旭旺, 叶坚虹, 包剑锋 . 中药抗肝纤维化机制研究进展[J]. 临床肝胆病杂志, 2025, 41(10): 1981-1987
来源:临床肝胆病杂志
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)