引言
类风湿关节炎(RA)是一种以侵蚀性关节炎症为典型特征的自身免疫性疾病,治疗核心目标是控制疾病活动、改善生活质量。RA的治疗通常联合多种药物,对于疗效不佳的患者,常需增加药物剂量或联合用药,但这会增加患者不良反应风险与经济负担。
研究基于Ⅲ期临床试验数据,共纳入566名中重度RA患者进行事后分析。患者被随机分为三组:4mg艾玛昔替尼组(n=189)、8mg艾玛昔替尼组(n=189)和安慰剂组(n=188)。所有患者最初24周内,均维持其分配的治疗方案。第24周时,安慰剂组患者转为接受4mg艾玛昔替尼治疗,其余两组患者则持续原方案直至第52周。
在原III期临床试验中,经12周治疗后关节症状改善不足20%患者可调整其RA的合并治疗方案。首选调整方案为非甾体抗炎药(NSAIDs)、
本研究评估了两个治疗周期(0-24周及24-52周)内现有药物的剂量增加或新增联用治疗药物的发生率及累计发生率(0-52周)。
监测药物类别包括:csDMARDs、oral GCs、IV/IM GCs、全身性免疫抑制剂及NSAIDs。
研究使用SPSS 29.0软件(IBM,美国)进行统计分析,分析时间为2024年11月至2025年2月。缺失数据采用无应答者填补法(NRI)处理。采用Kaplan-Meier法结合log-rank检验,分析新增联用药物或剂量上调的累积发生率。所有检验均为双侧,P值<0.05被视为具有统计学意义。
安慰剂组、4mg艾玛昔替尼组和8mg艾玛昔替尼组三组患者平均年龄均约50岁,其中80%以上为女性患者,病程均在9年以上。
在基线合并用药方面:使用csDMARDs的患者比例在安慰剂组为97.9%,4mg艾玛昔替尼组为95.2%,8mg艾玛昔替尼组为97.4%;三组使用NSAIDs的比例分别为44.7%、37.0%和45.5%;使用GCs的比例分别为37.6%、40.2%和30.7%。除艾玛昔替尼4mg组基线使用
表1 人口统计学和疾病基线特征。
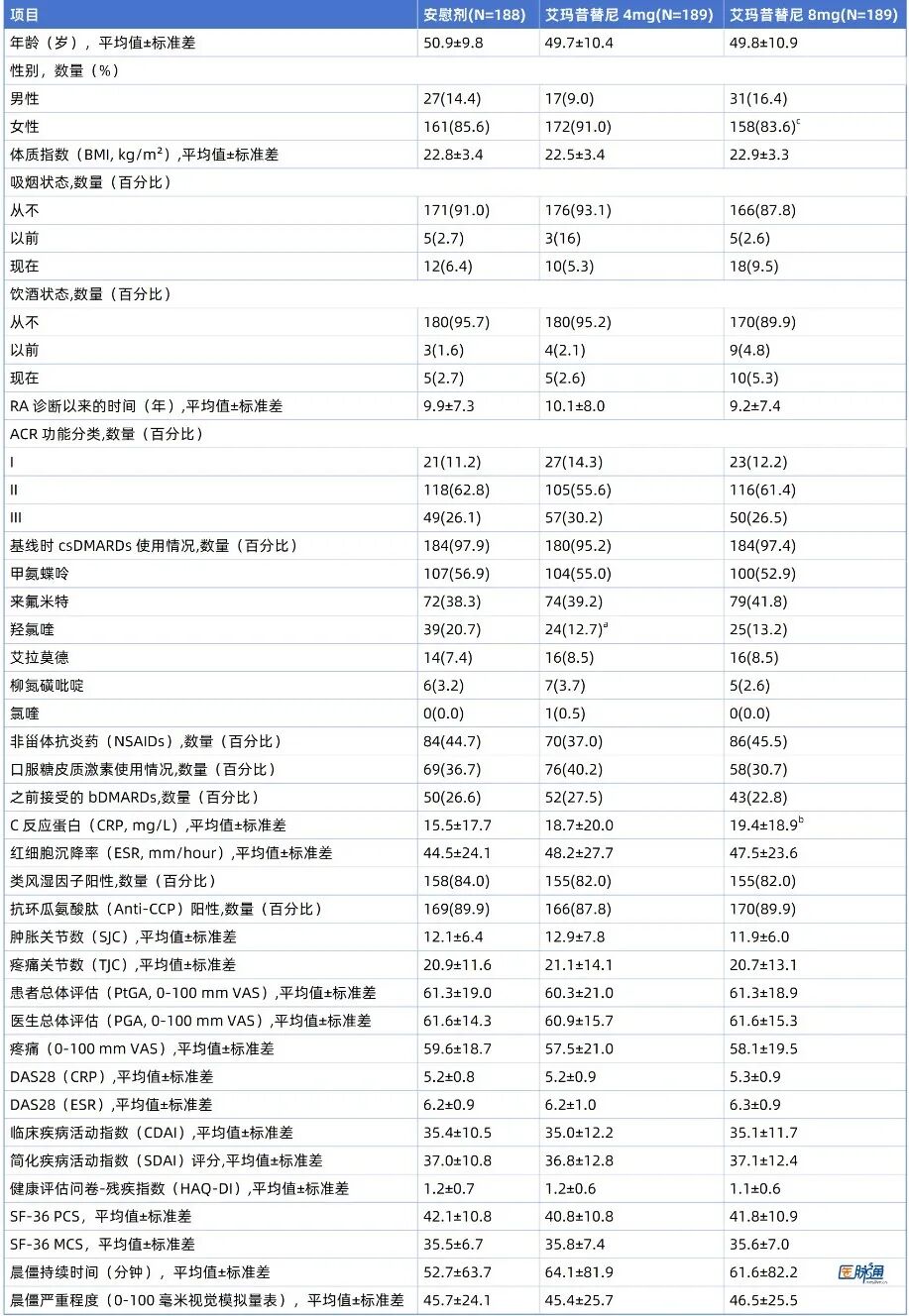
a艾玛昔替尼4mg与安慰剂相比P<0.05。
b艾玛昔替尼8mg与安慰剂相比P<0.05。
c艾玛昔替尼4mg与艾玛昔替尼8mg相比P<0.05。
RA,
0-24周,艾玛昔替尼4mg组和8mg组分别有14名(7.4%)和10名(5.3%)患者经历了新增联用药物或剂量上调,显著低于安慰剂组(42名,22.3%)(均P<0.001)。与安慰剂组相比,两组新增联用药物或剂量上调发生率差异分别为-14.9%(95% CI:-22.1%~-7.6%)和-17.0%(95% CI:-24.0% ~ -10.1%)。
24-52周,艾玛昔替尼4mg组(4.2%)和艾玛昔替尼8mg组(3.2%)的新增联用药物或剂量上调发生率持续保持低水平。此外,安慰剂转为艾玛昔替尼4mg治疗组的新增联用药物或剂量上调发生率为12.2%(图1)。
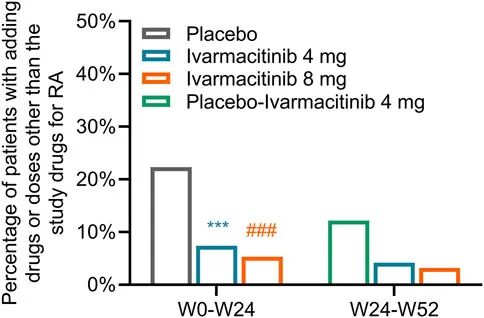
图1 第24周内及第24周至第52周期间新增联用药物或剂量上调的总发生率。
***:与安慰剂组相比,艾玛昔替尼4mg组P < 0.001;###:与安慰剂组相比,艾玛昔替尼8mg组P < 0.001。
总体而言,艾玛昔替尼在24周内显著减少了中重度RA患者的药物新增/加量需求,主要涉及oral GCs和NSAIDs。第24至52周期间,所有组别新增联用药物或剂量上调发生率均保持较低水平。
0-24周,安慰剂组oral GCs及NSAIDs的新增联用或剂量上调发生率显著高于4mg和8mg艾玛昔替尼组。
oral GCs:艾玛昔替尼4mg组、艾玛昔替尼8mg组、安慰剂组新增联用药物或剂量上调发生率分别为1.1%、0.5%,5.9%(均P<0.05)。与安慰剂组相比,艾玛昔替尼4mg组和8mg组oral GCs新增联用或剂量上调发生率的差异分别为-0.05%(95% CI:-0.08% ~ -0.01%)和-0.05%(95% CI:-0.09% ~ -0.02%)。
NSAIDs:艾玛昔替尼4mg组、8mg组,安慰剂组新增联用药物或剂量上调发生率分别为6.9%、4.2%,20.2%(均P<0.001)。与安慰剂组相比,艾玛昔替尼4mg组和8mg组的NSAIDs新增/加量发生率差异分别为−13.3%(95% CI:−20.2% ~ −6.4%)和−16.0%(95% CI:−22.6% ~ −9.4%)。
此外,各组中csDMARDs、IV/IM GCs及全身性免疫抑制剂的新增联用或剂量上调发生率均较低(≤0.5%)且艾玛昔替尼组与安慰剂组间未见差异(均P>0.05)。
24-52周,艾玛昔替尼4mg组与8mg组在csDMARDs、oral GCs、IV/IM GCs、全身性免疫抑制剂及NSAIDs的新增联用或剂量上调发生率均保持低水平。在安慰剂转为艾玛昔替尼4mg治疗组中,csDMARDs、IV/IM GCs及全身性免疫抑制剂药物新增联用或剂量上调的发生率持续保持低水平;值得注意的是,NSAIDs的新增联用或剂量上调发生率为4.3%(表2)。
表2 增加研究药物以外的药物或剂量治疗RA的患者
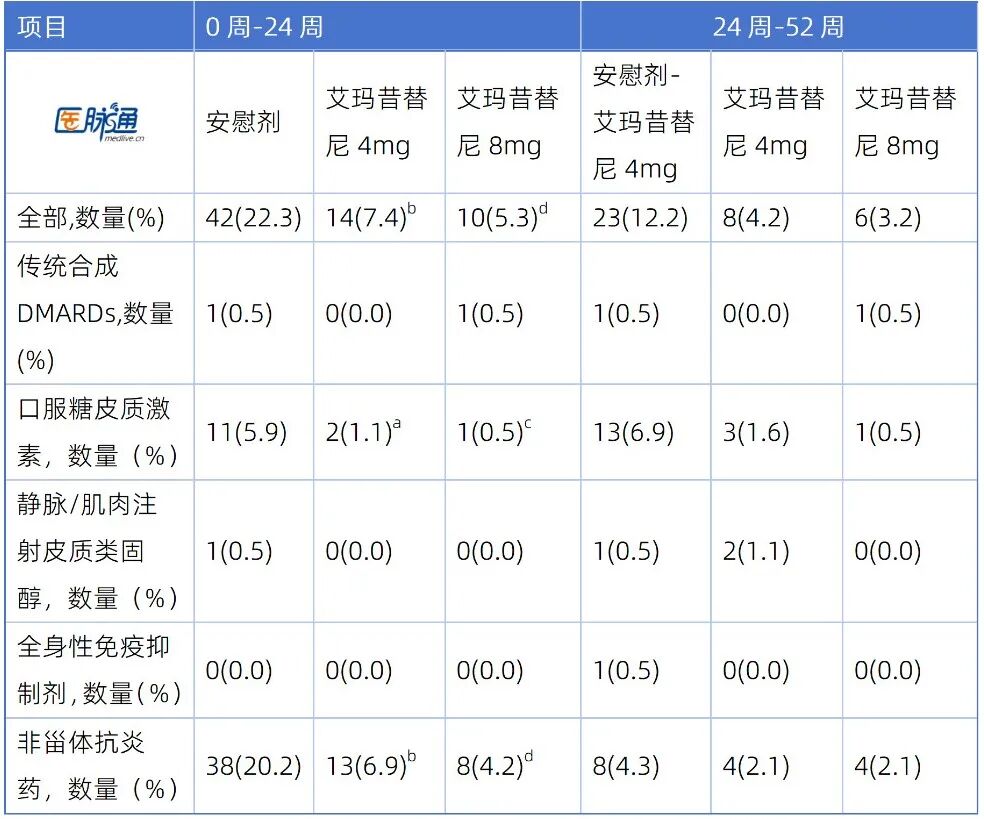
a艾玛昔替尼4mg与安慰剂相比,P<0.05。
b艾玛昔替尼4mg与安慰剂相比,P<0.001。
c艾玛昔替尼8mg与安慰剂相比,P<0.01。
d艾玛昔替尼8mg与安慰剂相比,P<0.001。
DMARDs,改善病情抗风湿药物。
累积新增联用药物或剂量上调发生率在治疗的前24周内,与安慰剂组相比,艾玛昔替尼8mg组在第16、20、24周,以及艾玛昔替尼4mg组在第20、24周,oral GCs的新增联用或剂量上调发生率(自基线算起)均显著更低(均P<0.05),各组在csDMARDs或IV/IM GCs的累积发生率方面未见显著差异。
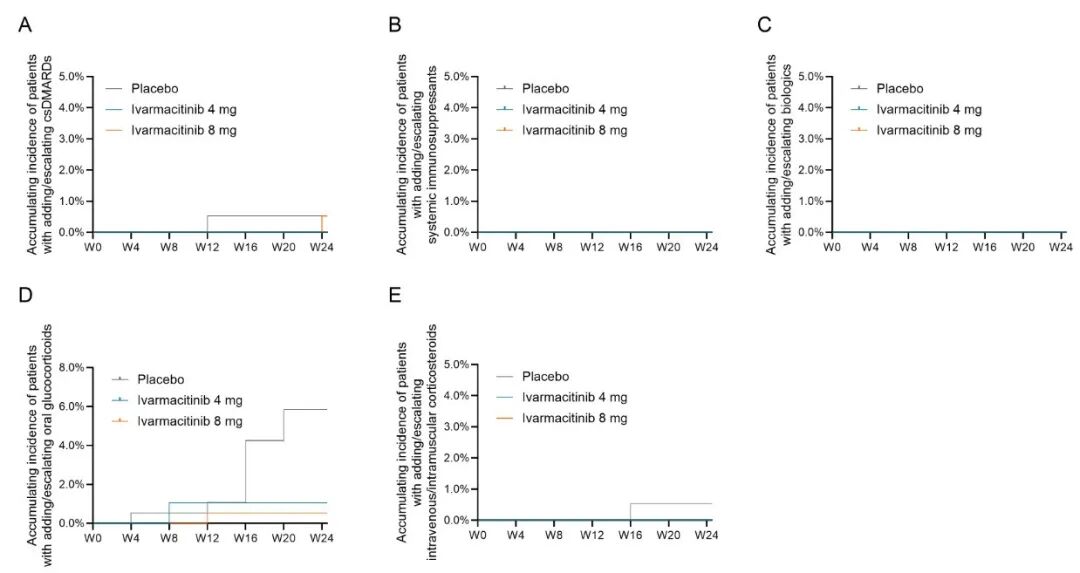
24-52周,三组患者oral GCs、csDMARDs及IV/IM GCs的累积发生率(自基线算起)总体保持稳定(图2A-F)。
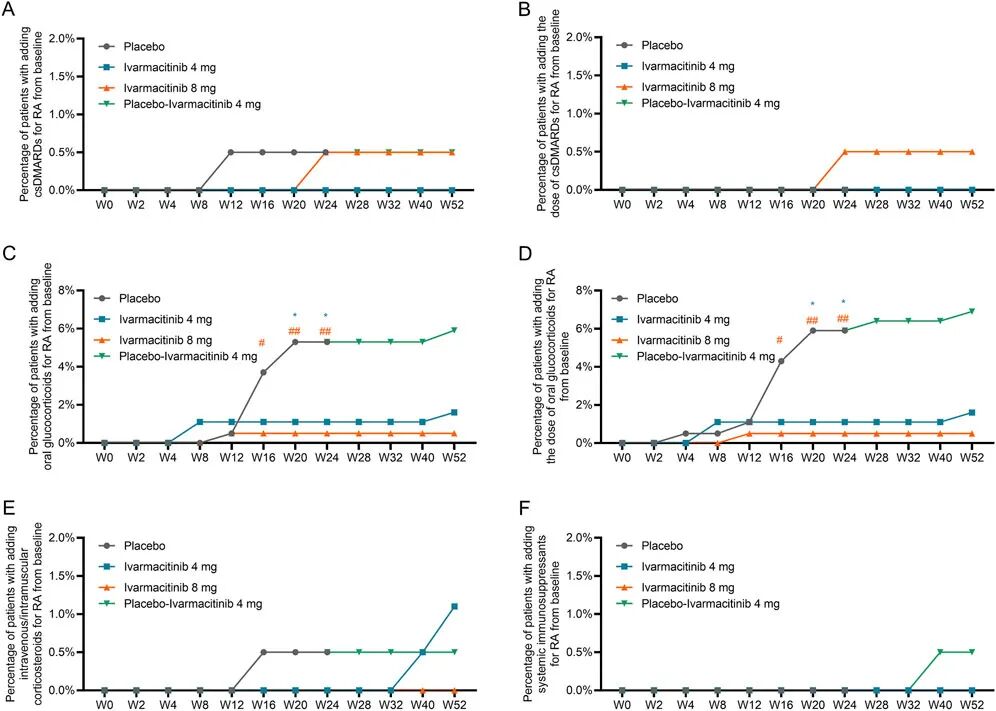
图2 从0至52周新增联用/剂量上调csDMARD、oral GCs和IV/IM GCs的累积发生率。
新增联用csDMARD(A)和剂量上调csDMARD(B)的累积发生率。新增oral GCs(C)和剂量上调oral GCs(D)的累积发生率。新增IV/IM GCs(E)和加量IV/IM GCs(F)的累积发生率。*:艾玛昔替尼4mg组与安慰剂组相比P<0.05;#:P<0.05,##:艾玛昔替尼8mg组与安慰剂组相比P<0.01。
针对csDMARDs或oral GCs联合累积事件的分析(图3A)显示,在前24周内,艾玛昔替尼4mg组和8mg组在第16、20、24周的发生率均显著低于安慰剂组(均P<0.05)。24-52周期间,三组的这一联合累积发生率保持稳定。此外,在治疗24周时,两个艾玛昔替尼组的联合累积发生率均显著低于安慰剂组(均P<0.01,图3B)。
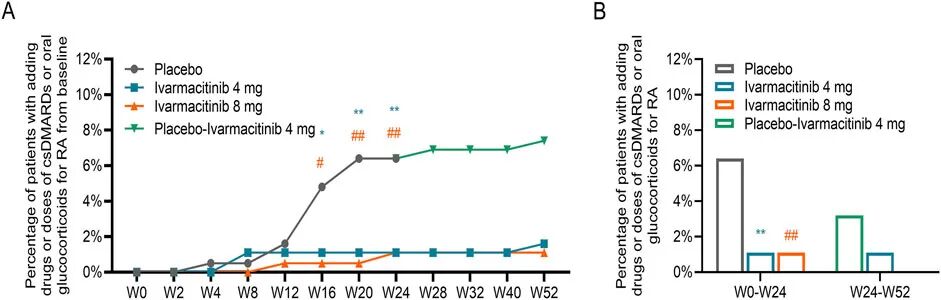
图3 csDMARD或oral GCs的新增联用或剂量上调。
从0至52周新增联用/剂量上调csDMARD或oral GCs的累积发生率(A)。在W24内和从W24至W52新增联用/剂量上调csDMARD或oral GCs的总发生率(B)。*:P<0.05,**:与安慰剂组相比,艾玛昔替尼4mg组P<0.01;#:P<0.05,##:艾玛昔替尼8mg组与安慰剂组相比P<0.01。
Kaplan-Meier生存分析进一步证实,仅在oral GCs的累积新增联用/剂量上调发生率上,艾玛昔替尼4mg组(P=0.011)和8mg组(P=0.003)均显著低于安慰剂组。对于其他类别的药物,各组间的累积发生率无显著差异(图S1A-E)。
图S1 Kaplan-Meier累积发生率分析。
(A)伴 ACR40 应答不足的患者累积发生率;(B)伴类风湿关节炎疾病活动度升高的患者累积发生率;(C)伴≥3 项疾病活动度指标升高的患者累积发生率;(D)伴口服糖皮质激素加量的患者累积发生率;(E)伴甲氨蝶呤(传统合成改善病情抗风湿药)加量的患者累积发生率
具体而言,艾玛昔替尼主要减少了口服GCs和NSAIDs的联用或剂量上调需求,这两种药物是临床最常用且与特定不良反应相关的药物,因此该结果具有重要的临床意义。而对于其他类药物(如csDMARDs、IV/IM GCs等)的联用或剂量上调需求,各组均处于低水平且无显著差异。
此外,研究显示,原先接受安慰剂的患者在第24周转为艾玛昔替尼4mg治疗后,其新增联用药物或剂量上调的需求也随之下降。在整个52周的研究期间,两个艾玛昔替尼治疗组的新增联用药物或剂量上调的发生率均始终维持在较低水平,提示其疗效具有持续性。
参考文献:
[1]Liu, J., Jiang, Y., Zhang, S., Liu, S., Su, J., Lin, C., et al. (2025). Ivarmacitinib, a selectivejanus kinase 1 inhibitor, in patients with moderate-to-severe active rheumatoid arthritisand inadequate response to conventional synthetic DMARDs: results from a phase IIIrandomised clinical trial. Ann. Rheum. Dis. 84, 188–200. doi:10.1136/ard-2024-226385.
[2]Liu H, Li J, Song L. Ivarmacitinib reduces the need for adding/escalating medications in moderate-to-severe rheumatoid arthritis patients: a post hoc analysis from a phase III trial. Front Pharmacol. 2025;16:1683508.
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)